Портал:Физичка хемија
ФИЗИЧКА ХЕМИЈА
Ова страница је портал за википедијанце које занима физичка хемија. Он омогућава лакши приступ као и помоћ у развоју чланака везаних за ову област науке.
Физичка хемија је природна наука која је настала комбиновањем знања из физике, хемије, термодинамике и квантне механике да би се опажене макроскопске појаве описале на атомском и молекулском нивоу. Дакле, физичка хемија се бави везом између микроскопских и макроскопских особина материје. На пример, величина молекула у течности може да се одреди на основу мерења њеног индекса преламања и густине, или на основу топлотног капацитета и површинског напона.
Познати истраживач Гилберт Луис је кратко рекао "Физичка хемија је све што је занимљиво."
Изабрани чланак
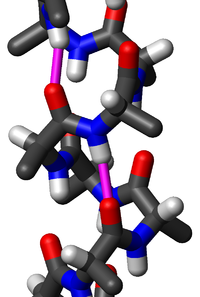
Алфа хеликс (α-хеликс) је десногира завојита конформација која подсећа на опругу, код које свака алфа-амино (N–H) група ствара водоничну везу са алфа-карбосилном (C=O) групом аминокиселине 4 остатка раније ( водонична веза).
Полипептидни ланац може формирати различите врсте хеликса које се разликују по броју увијања ланца и по размаку између увијених сегмената полипептида у хеликсу. Оне се образују спонтано, јер су енергетски најсиромашније, а тиме и најстабилније конформације протеина. Хеликс могу да образују и L- и D-аминокиселине, али само једне или друге јер хеликс не може да се образује од пептидног ланца који садржи смешу остатака L- и D-аминокиселина. Хеликси могу бити десногири и левогири, зависно од тога на коју страну се уврће протеински ланац; десногири хеликс је одређен правцем у коме се окрећу прсти десне руке када се палац постави на осу хеликса у правцу у коме се он гради. L-аминокиселине су чешће у природи и оне могу да образују и левогири и десногири хеликс, али већина познатих хеликса у природи су десногири. Међутим, само једна хеликсна конформација истовремено задовољава оптималне услове увијања која даје основу за лако успостављање интрамолекулских водоничних веза између блиских конституената пептидне везе. Та форма се назива α-хеликс и најчешће је присутна у протеинима живих система.
Слика месеца
Биографија

Ернест Радерфорд, (Ernest Rutherford; Нилсон, Нови Зеланд, 30. август 1871. - Кембриџ, 19. октобар 1937.), британски физичар
Био је професор на факултету у Монтреалу; био је професор физике на универзитету у Манчестеру (од 1907.), а од 1919. директор Кевендиш лабораторије у Кембриџу. Године 1903. изабран за члана (1925-30 за председника) Краљевског друштва. Нобелову награду за хемију добио је 1908. године. У почетку се бавио проучавањем радиоактивних распада. Први је уочио да се зрачење радијума састоји од три врсте, које је назвао α- β- и γ-зрачење.
Категорије физичке хемије
Да ли сте знали...
- ...да постоје четири агрегатна стања: чврсто, течно, гасовито, плазма?
- ...да је Архимедова вага справа за мерeње густине и специфичне тежине течности?
- ...да је деутеријум стабилни изотоп водоника чије атомско језгро садржи по један протон и неутрон, док језгро обичног водоника има само један протон?
- ...да је 1931. године, Харолд Јури, детектовао деутеријум, за шта је 1934. године добио Нобелову награду за хемију?
- ...је пиролиза разлагање супстанције под утицајем високе температуре без утицаја других агенаса?
Потребни чланци

Потребно направити
Потребно проширити

