Фосфат
Фосфат, је у неорганској хемији со фосфорне киселине. У органској хемији, фосфат, или органофосфат, је естар фосфорне киселине. Органски фосфати су важни у биохемији и биогеохемији или екологији. Неорганиски фосфати се ископавају да би се добио фосфор за употребу у агрикултури и индустрији.[5][6][7] На повишеним температурама у чврстом стању, фосфати могу да се кондензују и формирају пирофосфате.
| |||
| |||
| Називи | |||
|---|---|---|---|
| Системски IUPAC назив
Фосфат[1] | |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| Бајлштајн | 3903772 | ||
| ChEBI | |||
| ChemSpider | |||
| Гмелин Референца | 1997 | ||
| МеСХ | Пхоспхатес | ||
| УНИИ | |||
| |||
| Својства | |||
| PO43− | |||
| Моларна маса | 94,9714 g mol−1 | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |||
| Референце инфокутије | |||


Хемијске особине уреди
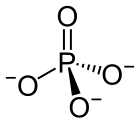
Фосфатни јон је полиатомски јон са емпиријском формулом PO43− и моларном масом од 94.973 г/мол. Он се састоји од једног централног атома фосфора атом окруженог са четири атома кисеоника у тетраедарској конфигурацији. Фосфатни јон носи три негатива формална наелектрисања и он је коњугована база хидроген фосфатног јона, HPO42-, који је коњугована база H2PO4-, дихидроген фосфатног јона, који је коњугована база H3ПО4, фосфорне киселине. Он је хипервалентни молекул (атом фосфора има 10 електрона у својој валентној љуски). Фосфат је такође органофосфорно једињење са формулом OP(OR)3.
Фосфатне соли се формирају кад се позитивно-наелектрисани јон веже за негативно-наелектрисане атоме кисеоника, формирајући јонско једињење. Многи фосфати нису растворни у води на стандардној температури и притиску. Натријум, калијум, рубидијум, цезијум и амонијум фосфати су растворни у води. Већина других фосфата су веома мало растворни или нерастворни у води. Као правило, хидроген и дихидроген фосфати су нешто растворнији од кореспондирајућих фосфата. Пирофосфати су углавном растворни у води.
У разређеним воденим растворима, фосфат постоји у четири облика. У јако-базној средини, фосфатни јон (PO43−) предоминира, док у слабо-базним условима, хидроген фосфатни јон (HPO42−) је превалентан. У слабо-киселим условима, дихидроген фосфатни јон (H2PO4−) је најзаступљенији. У јако-киселој средини, фосфорна киселина (H3PO4) је главна форма.
-
H3PO4 -
H2PO4− -
HPO42− -
PO43−
Прецизнији, полазећи од следеће три равнотежне реакције:
- H3PO4 ⇌ H+ + H2PO4−
- H2PO4− ⇌ H+ + HPO42−
- HPO42− ⇌ H+ + PO43−
кореспондирајуће константе дисоцијације на 25 °C (у мол/L) су:
- (пКа1 2.12)
- (пКа2 7.21)
- (пКа3 12.67)
Референце уреди
- ^ „Пхоспхатес – ПубЦхем Публиц Цхемицал Датабасе”. Тхе ПубЦхем Пројецт. УСА: Натионал Центер оф Биотецхнологy Информатион.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Campbell, Neil A.; Reece, Jane B. (2005). Biology (Seventh изд.). San Francisco, California: Benjamin Cummings. стр. 65. ISBN 978-0-8053-7171-0.
- ^ „Phosphate Primer”. Архивирано из оригинала 20. 06. 2008. г. Приступљено 17. 10. 2010.
- ^ Lynn A. Kuntz (2006). „Figuring Out Phosphates”. Архивирано из оригинала 20. 12. 2008. г. Приступљено 17. 10. 2010.
- ^ Kuntz, Lynn A. (2006). „Food Product Design”. Архивирано из оригинала 20. 12. 2008. г. Приступљено 17. 10. 2010.

