Очна водица
Очна водица се налази иза рожњаче. Њена оптичка густина је већа од ваздуха, тако да омогућује преламање светлости.[1] Очна водица се константно ствара и апсорбује.
| Очна водица | |
|---|---|
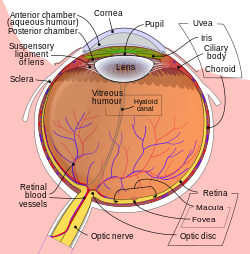 Шематски приказ људског ока. | |
| Детаљи | |
| Идентификатори | |
| Латински | humor aquosus |
| MeSH | D001082 |
| TA | A15.2.06.002 |
| FMA | 58819 |
| Анатомска терминологија | |
Очна водица је бистра, безбојна течност која испуњава простор предње и задње коморе ока, које су одвојене дужицом, а комуницирају помоћу отвора у дужици и зеници. Већа количина, 4/5 очне водице је у предњој и 1/5 у задњој комори ока. Укупна запремина очне водице која је 0,30 мл, производи се из крви цилијарних наставака механизмом ултрафилтрације, дифузије и активним транспортом.[2]
Константна количина коморне течности је важна за елиминацију продуката метаболизма. На основу тога се сматра да значајна редукција стварања очне водице можe да доведе до оштећења структура ока повећањем концентрација штетних материја. Како постојање глаукома доводи до смањења апсорбовања очне водице, он може довести до раста притиска у оку, што последично може довести и до слепила.[3]
Физиологија и анатомија уреди
Физиолошка улога очне водице у оку је вишеструка:
- исхрана неваскуларизованих структура ока (рожњача и сочива)
- дренажа метаболити насталих у неваскуларизованим структурама ока,
- учешће у преламању светлосних зрака,
- одржавање одговарајућег и сталног притисак унутар ока (ИОП), као најважнија улога, које је резултат успостављене равнотеже између брзине формирања очне водице и њеног одлива из ока.[4][5][6]
Проток очне водице код људи прати циркадијални ритам, и зато је он већи ујутру него увече.
Хидродинамика ока уреди
Хидродинамика ока у многоме зависи од опште циркулације као и од срчане функције имајући у виду да се на основу разлике у притисцима између васкуларног система и хидродинамског система обавља отицање или дренажа очне водице из ока.
Највећи утицај на висину притиска унутар ока (ИОП) има отпор у дренажном систему ока. Отицање очне водице највећим делом обавља се преко корнеосклералног трабекулума, Шлемовог канала, еписклералних вена до венског система. Иако је овај конвенционални пут, преко корнеосклералног трабекулума и Шлемовог канала, најзначајнији јер обухвата и највећу количине очне водице, између 83 и 96%, важну улогу имају и неконвенционални путеви отицања који су посебно значајни за разумевање патогенезе глаукома, али још више за неке облике деловања терапије глаукома.
Механизам стварања очне водице уреди
Секреција очне водице се одвија у наставцима цилијарног тела у задњој комори ока и трабекуларној мрежи (ТМ). Процес почиње ултрафилтрацијом плазме у ситним крвним судовима цилијарног тела, на који се надовезује процес активне секреције и дифузије у ћелијама цилијарног епитела. Брзина лучења очне водице је релативно константна и код младе, здраве особе износи просечно 2,75µl/min.
Количина излучен очне водице се не разликује међу половима, а смањује се за око 30% током процеса старења.[7] Најбрже лучење очне водице се дешава током преподнева, док током ноћи долази до редукције од преко 40%.[8]
Секреција очне водице и регулисање њеног одлива су физиолошки важни процеси за одржавање притиска унутар ока (ИОП) у оквиру нормалних вредности. Следећа три механизма укључена су у формирање очне водице:[9]
Ултрафилтрација уреди
Ултрафилтрација подразумева филтрацију воде и у води растворених супстанци кроз ћелијску мембрану и кроз фенестриране капиларе цилијарних наставака тако да ултрафилтрат доспева у строму ових наставака на основу специфичних особина фенестра на капиларима цилијарних наставака. Процес ултрафилтрације плазме одиграва се у строми наставка цилијарног тела, која је добро васкуларизована са великим протоком крви
Овај ултрафилтрат који садржи високе концентрације протеина плазме (која износи и до 60% концентрације у плазми),[10] обавља се услед релативног осмотског и хидростатског градијента притисака који постоји у капиларима и строми цилијарних наставака. Ултрафилтрација кроз цилијарни епител не утиче значајно на количину створене очне водице, али има веома значајно место у целокупном процесу стварања очне водице.
Ултрафилтрација представља важан сегмент у стварању очне водице, захваљујући којој се састојци плазме прелазе у строму цилијарних наставака, а онда се потискују у епител да би се активним транспортом из цилијарног епитела састојци транспортовали у задњу комору.
Дифузија уреди
Дифузија је процес којом се ствара велики део очне течности. Дифузија је пасивно прелажење супстанца кроз ћелијску мембрану према мањем концентрационом градијенту. Захваљујући дифузији кисеоник и глукоза који су неопходни за метаболизам сочива и рожњаче транспортују се кроз хематоокуларну баријеру. Брзина њихове дифузије не зависи од брзине секреције очне водице. Њихов градијент концентрације настаје због утрошка у ткивима сочива и рожњаче и то регулише брзину дифузије.[11]
Активни транспорт уреди
Активним транспортом се ствара веома значајна количина очне водице. Овај транспорт је супротан концентрационом градијенту.
Стварање очне водице почиње ултрафилтрацијом плазме из капилара цилијарних наставака праћеним активним транспортом-секрецијом у задњу очну комору из цилијарног епитела. Секрецијом очне водице ствара се њен највећи део. Овај део зависи од очуваности структура хематоокуларне баријере као и активног транспорта раствора и одржавања осмотског градијента између ћелија непигментног епитела, што подстиче проток воде и других супстанци у задњу комору.[12][13][14][15][16]
Очна водица напушта око пасивним протоком преко два пута - трабекуларне мреже и увеосклералног пута. Код људи, 75% отпорности на изливање очне водице је локализовано унутар трабекуларне мреже, при чему је јукстаканаликуларни део трабекуларне мреже главно место отпора на изливање. Претпоставља се да је одлагање гликозаминогликана у екстрацелуларном матриксу трабекуларне мреже (ЕЦМ) одговорно за повећану отпорност на изливање на овом специфичном месту, док други сугеришу да таложење протеина, као што је кохлин, омета одлив очне водице кроз трабекуларну мрежу.[9]
Пут увеосклералног одлива је релативно независан од интраокуларног притиска и удео очне водице која излази из ока преко увеосклералног пута опада са годинама.[9]
Састав очне водице уреди
Истраживањима је утврђено је да постоје разлике у саставу очне водице и плазме који се огледа у сатаву протеина, највероватније због функције спојева хематоокуларне баријере.[17] То указује да очна водица није ултрафилтрат плазме. Ове разлике потврђују да постоји специфични секреторни активни механизам којим се ствара очна водица. Тако се у очној водици налази ниска концентрација беланчевина и висока концентрација аскорбата. Очна водица садржи:
- Протеини мање од 1%, који се налазе у плазми. Изузетак представља трансферин који је у већој концентрацији у очној водици него у плазми.[18] Концентрација појединих протеина може да указује на одређене патолошке процесе у оку са променама на нивоу крвно - водене баријере.[19]
- угњени хидрети,
- Аминокиселине које транспортују цилијарни мишићи
- 98% вода
- електролити (пХ = 7,4) - натријум 142,09, калијум 2,2 - 4,0, калцијум 1,8, магнезијум 1,1, хлорид 131,6, HCO3 20,15, фосфат 0,62, онкостатин 304
- аскорбинска киселина, која је 30 пута веће концентрације у односу на плазму. Она има значајну улогу у функционисању заштитних, антиоксидационих система на бази глутатиона (GSH).
Клинички значај уреди
Глауком је прогресивна оптичка неуропатија у којој ретиналне ганглијске ћелије и њихови аксони умиру изазивајући одговарајући дефект видног поља. Важан фактор ризика је повећан интраокуларни притисак (ИОП) или притисак унутар ока. било кроз повећану производњу или смањен одлив очне водице.[20]
Повећана отпорност на одлив очне водице може настати због абнормалне трабекуларне мреже или због облитерације мреже која је резултат повреде или болести шаренице. Међутим, повећан интерокуларни притисак није ни довољан ни неопходан за развој примарног глаукома отвореног угла, иако је главни фактор ризика. Неконтролисани глауком обично доводи до губитка видног поља и на крају слепила.
Увеосклерални одлив очне водице може се повећати агонистима простагландина, док трабекуларни одлив повећавају М3 агонисти. Производња течности може да се смањи бета блокаторима, алфа2-агонистима и инхибиторима карбоанхидразе.[21]
Извори уреди
- ^ „Refraction | Definition, Examples, & Facts | Britannica”. www.britannica.com (на језику: енглески). Приступљено 2022-12-16.
- ^ „Aqueous Humor Flow and Function | BrightFocus Foundation”. www.brightfocus.org. Приступљено 2022-12-16.
- ^ Smith, Michael (2017-08-26). „The aqueous humour”. Vision Eye Institute (на језику: енглески). Приступљено 2022-12-16.
- ^ H.P. Rang, M.M. Dale, J.M. Ritter, P.K. Moore, Pharmacology, 5th ed., Churchill Livingstone, Edinburgh 2003
- ^ C. To, C. Kong, C. Chan, M. Shahidullah, C. Do, The mechanism of aqueous humour formation. Clin. Exp. Optom. 2002, 85, 335-349.
- ^ R.K. Griffith, Adrenergic receptors and drugs affecting adrenergic neurotransmission, In: T.L. Lemke, D.A. Wiliams, V.F. Roche, S.W. Zito (Eds), Foy’s principles of medicinal chemistry, 7th ed., Lippincott Wiliams & Wilkins, Philadelphia 2013, 340-365.
- ^ Brubaker RF. Flow of aqueous humor in humans [The Friedenwald Lecture]. Invest Ophthalmol Vis Sci. 1991 Dec;32(13):3145–66
- ^ Reiss GR, Lee DA, Topper JE, Brubaker RF. Aqueous humor flow during sleep. Invest Ophthalmol Vis Sci. 1984;25(6):776–8.
- ^ а б в Goel, Manik; Picciani, Renata G; Lee, Richard K; Bhattacharya, Sanjoy K (2010-09-03). „Aqueous Humor Dynamics: A Review”. The Open Ophthalmology Journal. 4: 52—59. ISSN 1874-3641. PMC 3032230 . PMID 21293732. doi:10.2174/1874364101004010052.
- ^ Bill A. Capillary Permeability to and Extravascular Dynamics of Myoglobin, Albumin and Gammaglobulin in the Uvea. Acta Physiol Scand. 1968 May;73(1-2):204–19.
- ^ Shui YB, Fu JJ, Garcia C, Dattilo LK, Rajagopal R, McMillan S, et al. Oxygen distribution in the rabbit eye and oxygen consumption by the lens. Investig Ophthalmol Vis Sci. 2006;47(4):1571–80
- ^ Bill A, Phillips CI: Uveoscleral drainage of aqueous humour in human eyes, Exp Eye Res 1971;12(3):275-81
- ^ Toris CB. Aqueous humor dynamics in ocular hypertensive patients, J Glaucoma 2002;11:253-8.
- ^ Jocson VL, Sears ML: Experimental aqueous perfusion in enucleated human eyes. Results after obstruction of Schlemm’s canal, Arch Ophthalmol 1971;86:65-71
- ^ Bill A, Phillips CI: Uveoscleral drainage of aqueous humour in human eyes, Exp Eye Res 1971;12:275-81
- ^ Toris CB, et al: Aqueous humor dynamics in the aging human eye, Am J Ophthalmol 1999;127:407-412.
- ^ Farahbakhsh NA, Fain GL. Volume regulation of non-pigmented cells from ciliary epithelium. Investig Ophthalmol Vis Sci. 1987;28(6):934–44.
- ^ Lütjen-Drecoll E, Lönnerholm G, Eichhorn M. Carbonic anhydrase distribution in the human and monkey eye by light and electron microscopy. Graefe’s Arch Clin Exp Ophthalmol = Albr von Graefes Arch für Klin und Exp Ophthalmol. 1983 Jan;220(6):285–91
- ^ Richardson MR, Price MO, Price FW, Pardo JC, Grandin JC, You J, et al. Proteomic analysis of human aqueous humor using multidimensional protein identification technology. Mol Vis. 2009;15(November):2740–50.
- ^ „Glaucoma Medications: Eye Drops, Pills & Side Effects”. eMedicineHealth (на језику: енглески). Приступљено 2022-09-29.
- ^ Tao, Le (2017-11-13). First aid for the USMLE Step 2 CS. Bhushan, Vikas., Lee, Kachiu., Deol, Maniver. (Sixth ed.). New York. ISBN 9781259862441. стр. 505.
Спољашње везе уреди
| Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |