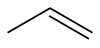
Пропен
Пропилен, такође познат под IUPAC-овим именом као пропен, је органско једињење хемијске формуле C3H6. То је друго по једноставности једињење из групе алкена из класе угљоводоника, од којих је етилен (етен) најједноставнији. Под нормалним условима пропилен је гас без боје и мириса.[5] (У комерцијални гас се додају трагови меркаптана или сличних једињења непријатног и продорног мириса да би се гас, ако процури лако осетио по мирису. Пропилен може да се добије гасификацијом угља али се углавном производи крековањем сирове нафте. Пропилен је једна од најважнијих сировина у петрохемијској индустрији. Најважнија употреба је као мономера у производњи полипропилена.[6]
| |||
| |||
| Називи | |||
|---|---|---|---|
| Преферисани IUPAC назив
Пропен[1] | |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.693 | ||
| KEGG[2] | |||
| RTECS | UC6740000 | ||
| UNII | |||
| UN број | 1077 У течном нафтном гасу: 1075 | ||
| |||
| |||
| Својства | |||
| C3H6 | |||
| Моларна маса | 42,08 g·mol−1 | ||
| Агрегатно стање | Безбојни гас | ||
| Густина | 1,81 kg/m3, гас (1,013 bar, 15 °C) 1,745 kg/m3, гас (1,013 bar, 25 °C) 613,9 kg/m3, течност | ||
| Тачка топљења | −185,2 °C (−301,4 °F; 88,0 K) | ||
| Тачка кључања | −47,6 °C (−53,7 °F; 225,6 K) | ||
| 0,61 g/m3 | |||
| Магнетна сусцептибилност | -31,5·10−6 cm³/mol | ||
| Вискозност | 8,34 µPa·s на 16,7 °C | ||
| Структура | |||
| Диполни момент | 0,366 D (гас) | ||
| Опасности | |||
| Безбедност приликом руковања | External MSDS | ||
ЕУ класификација (DSD)
|
  
| ||
| R-ознаке | 12 | ||
| S-ознаке | 9-16-33 | ||
| NFPA 704 | |||
| Тачка паљења | −108 °C (−162 °F; 165 K) | ||
| Сродна једињења | |||
Сродна алкенска једињења;
сродне групе |
Етилен, изомери бутилена; алил, пропенил | ||
Сродна једињења
|
Пропан, пропин пропадиен, 1-пропанол 2-пропанол | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |||
| Референце инфокутије | |||
Продукција уреди
Парно крековање уреди
Доминантна технологија за производњу пропилена је крековање паром. Иста технологија се примењује од етана до етилена. Ове две конверзије су процеси #2 и #1 у хемијској индустрији, судећи по њиховом опсегу.[7] У овом процесу, пропан се подвргава дехидрогенацији. Нуспроизвод је водоник:
- CH3CH2CH3 → CH3CH=CH2 + H2
Принос пропена је око 85 м%. Нуспроизводи се обично користе као гориво за реакцију дехидрогенације пропана. Парно крековање је један од енергетски најинтензивнијих индустријских процеса.
Сировина је нафта или пропан, посебно на Бликом Истоку, где постоји обиље пропана из нафтних/гасних операција.[8] Пропен се може издвојити фракционом дестилацијом из мешавина угљоводоника добијених крекингом и другим процесима рафинације; пропен за рафинерију је има чисточу од 50 до 70%.[9] У Сједињеним Државама, гас из шкриљаца је главни извор пропана.
Технологија конверзије олефина уреди
У Филипсовој триолефинској или технологији олефинске конверзије пропилен се интерконвертује са етиленом и 2-бутенима. Користе се ренијумски и молибденски катализатори:[10]
- CH2=CH2 + CH3CH=CHCH3 → 2 CH2=CHCH3
Технологија је заснована на реакцији метатезе олефина откривеној у Филипсовој нафтној компанији.[11][12] Постижу се приноси пропена од око 90 теж.%.
Флуидно каталитичко крековање уреди
Флуидно каталитички крекинг (FCC) високе јачине користи традиционалну технологију у оштрим условима (већи однос катализатора и уља, веће брзине убризгавања паре, више температуре, итд) како би се максимизовала количина пропена и других лаких производа. Јединица FCC процеса високе јачине се обично напаја гасним уљима (парафинима) и остацима и производи око 20-25 м% пропена на сировини заједно са већим количинама моторног бензина и дестилационих нуспроизвода. Ови високотемпературни процеси су скупи и имају висок угљични отисак. Из ових разлога, алтернативни путеви за добијање пропилена и даље привлаче пажњу.[13]
Тржиште и истраживање уреди
Производња пропена је остала статична на око 35 милиона тона (само у Европи и Северној Америци) од 2000. до 2008. године, али је у порасту у источној Азији, пре свега у Сингапуру и Кини.[14] Укупна светска производња пропена је тренутно око половине мања од етилена.
Употреба конструисаних ензима је истражена, али нема комерцијалну вредност.[15]
Употребе уреди
Пропен је други најважнији почетни производ у петрохемијској индустрији после етилена. То је сировина за широк спектар производа. Произвођачи полипропилена троше скоро две трећине светске производње.[16] Крајња употреба полипропилена укључује филмове, влакна, контејнере, амбалажу, поклопце и затвараче. Пропен се такође користи за производњу важних хемикалија као што су пропилен оксид, акрилонитрил, кумен, бутиралдехид и акрилна киселина. У 2013. години око 85 милиона тона пропена је прерађено широм света.[16]
Пропен и бензол се куменским процесом претварају у ацетон и фенол.
Пропен се такође користи за производњу изопропанола (пропан-2-ол), акрилонитрила, пропилен оксида и епихлорохидрина.[17] Индустријска производња акрилне киселине укључује каталитичку делимичну оксидацију пропена.[18] Пропен је такође интермедијер у једностепеној селективној оксидацији пропана у акрилну киселину.[19][20][21][22] У индустрији и занатству, пропен се користи као алтернативно гориво ацетилену у заваривању и резању, лемљењу и загревању метала у сврху савијања. Он је постао стандард у Бернзоматик производима и другим заменама за MAPP,[23] сада када прави MAPP гас више није доступан.
Реакције уреди
Пропен подсећа на друге алкене по томе што се релативно лако подвргава реакцијама адиције на собној температури. Релативна слабост његове двоструке везе објашњава њену тенденцију да реагује са супстанцама које могу остварити ову трансформацију. Реакције алкена обухватају: 1) полимеризацију, 2) оксидацију, 3) халогенацију и хидрохалогенацију, 4) алкилацију, 5) хидратацију, 6) олигомеризацију и 7) хидроформилацију.
Комплекси прелазних метала уреди
Основа за хидроформилацију, метатезу алкена и полимеризацију су комплекси метал-пропилен, који су интермедијери у овим процесима. Пропилен је прохиралан, што значи да везивање реагенса (као што је метални електрофил) за C=C групу даје један од два енантиомера.
Полимеризација уреди
Већина пропена се користи за формирање полипропилена, веома важне робе термопластике, кроз полимеризацију ланчаног раста.[16] У присуству одговарајућег катализатора (обично Зиглер-Ната катализатора), пропен ће се полимеризовати. Постоји више начина да се то постигне, као што је коришћење високог притиска за суспендовање катализатора у раствору течног пропена, или пропуштање гасовитог пропена кроз реактор са флуидизованим слојем.[24]
Сагоревање уреди
Пропен гори на сличан начин као и други алкени. У присуству довољног или прекомерног кисеоника, пропен гори и формира воду и угљен-диоксид.
- 2 C3H6 + 9 O2 → 6 CO2 + 6 H2O
Особине уреди
| Особина | Вредност |
|---|---|
| Број акцептора водоника | 0 |
| Број донора водоника | 0 |
| Број ротационих веза | 0 |
| Партициони коефицијент[25] (ALogP) | 1,3 |
| Растворљивост[26] (logS, log(mol/L)) | -0,3 |
| Поларна површина[27] (PSA, Å2) | 0,0 |
Референце уреди
- ^ „Front Matter”. Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. стр. 31. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-FP001.
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Lide David R., ур. (2006). CRC Handbook of Chemistry and Physics (87th изд.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ „Propylene”.
- ^ Giovanni Maggini (2013-04-17). „Technology Economics: Propylene via Propane Dehydrogenation, Part 3”. Slideshare.net. Приступљено 2013-11-12.
- ^ Ashford’s Dictionary of Industrial Chemicals, Third edition, (2011) ISBN 978-0-9522674-3-0, pages 7766-9
- ^ „Product Safety Assessment(PSA): Propylene”. Dow Chemical Co. Архивирано из оригинала 2013-06-22. г. Приступљено 2011-07-11.
- ^ Ghashghaee, Mohammad (2018). „Heterogeneous catalysts for gas-phase conversion of ethylene to higher olefins”. Rev. Chem. Eng. 34 (5): 595—655. S2CID 103664623. doi:10.1515/revce-2017-0003.
- ^ Banks, R. L.; Bailey, G. C. (1964). „Olefin Disproportionation. A New Catalytic Process”. Industrial & Engineering Chemistry Product Research and Development. 3 (3): 170—173. doi:10.1021/i360011a002.
- ^ Lionel Delaude; Alfred F. Noels (2005). „Metathesis”. Kirk-Othmer Encyclopedia of Chemical Technology. Weinheim: Wiley-VCH. ISBN 978-0471238966. doi:10.1002/0471238961.metanoel.a01.
- ^ Schiffer, Zachary J.; Manthiram, Karthish (2017). „Electrification and Decarbonization of the Chemical Industry”. Joule. 1: 10—14. doi:10.1016/j.joule.2017.07.008. hdl:1721.1/124019 .
- ^ Amghizar, Ismaël; Vandewalle, Laurien A.; Van Geem, Kevin M.; Marin, Guy B. (2017). „New Trends in Olefin Production”. Engineering. 3 (2): 171—178. doi:10.1016/J.ENG.2017.02.006 .
- ^ de Guzman, Doris (12. 10. 2012). „Global Bioenergies in bio-propylene”. Green Chemicals Blog. Архивирано из оригинала 04. 11. 2021. г. Приступљено 01. 11. 2021.
- ^ а б в „Market Study: Propylene (2nd edition), Ceresana, December 2014”. ceresana.com. Архивирано из оригинала 02. 12. 2020. г. Приступљено 2015-02-03.
- ^ Budavari, Susan, ур. (1996). „8034. Propylene”. The Merck Index, Twelfth Edition. New Jersey: Merck & Co. стр. 1348—1349.
- ^ J.G.L., Fierro (Ed.) (2006). Metal Oxides, Chemistry and Applications. CRC Press. стр. 414—455.
- ^ Naumann d'Alnoncourt, Raoul; Csepei, Lénárd-István; Hävecker, Michael; et al. (март 2014). „The reaction network in propane oxidation over phase-pure MoVTeNb M1 oxide catalysts”. Journal of Catalysis. 311: 369—385. doi:10.1016/j.jcat.2013.12.008. hdl:11858/00-001M-0000-0014-F434-5 .
- ^ Amakawa, Kazuhiko; Kolen'Ko, Yury V.; Villa, Alberto; et al. (7. 6. 2013). „Multifunctionality of Crystalline MoV(TeNb) M1 Oxide Catalysts in Selective Oxidation of Propane and Benzyl Alcohol”. ACS Catalysis. 3 (6): 1103—1113. doi:10.1021/cs400010q. hdl:11858/00-001M-0000-000E-FA39-1.
- ^ Hävecker, Michael; Wrabetz, Sabine; Kröhnert, Jutta; et al. (јануар 2012). „Surface chemistry of phase-pure M1 MoVTeNb oxide during operation in selective oxidation of propane to acrylic acid”. Journal of Catalysis. 285 (1): 48—60. doi:10.1016/j.jcat.2011.09.012. hdl:11858/00-001M-0000-0012-1BEB-F .
- ^ Csepei, Lénárd-István (2011). Kinetic studies of propane oxidation on Mo and V based mixed oxide catalysts. стр. 3—24, 93. doi:10.14279/depositonce-2972.
- ^ For example, "MAPP-Pro"
- ^ Heggs, T. Geoffrey (2011-10-15), Wiley-VCH Verlag GmbH & Co. KGaA, ур., „Polypropylene”, Ullmann's Encyclopedia of Industrial Chemistry (на језику: енглески), Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA, стр. o21_o04, ISBN 978-3-527-30673-2, doi:10.1002/14356007.o21_o04, Приступљено 2021-07-09
- ^ Ghose, A.K.; Viswanadhan V.N. & Wendoloski, J.J. (1998). „Prediction of Hydrophobic (Lipophilic) Properties of Small Organic Molecules Using Fragment Methods: An Analysis of AlogP and CLogP Methods”. J. Phys. Chem. A. 102: 3762—3772. doi:10.1021/jp980230o.
- ^ Tetko IV, Tanchuk VY, Kasheva TN, Villa AE (2001). „Estimation of Aqueous Solubility of Chemical Compounds Using E-State Indices”. Chem Inf. Comput. Sci. 41: 1488—1493. PMID 11749573. doi:10.1021/ci000392t.
- ^ Ertl P.; Rohde B.; Selzer P. (2000). „Fast calculation of molecular polar surface area as a sum of fragment based contributions and its application to the prediction of drug transport properties”. J. Med. Chem. 43: 3714—3717. PMID 11020286. doi:10.1021/jm000942e.
Литература уреди
- Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th изд.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
Спољашње везе уреди
- „Spacecraft finds propylene on Saturn moon, Titan”. UPI.com. 2013-09-30. Приступљено 2013-11-12.
- „Cassini finds ingredient of household plastic on Saturn moon”. Spacedaily.com. Приступљено 2013-11-12.