Мукополисахаридоза тип I H-S
Мукополисахаридозе тип I H-S (скраћено MPS тип I H-S) позната и као Hurler-Scheie синдром је средње тежак (интермедијерни) облик мукополисахаридозе тип I болести из група наследних поремећаја узрокованих недостатком специфичних лизозомских ензима укључених у деградацију гликозаминогликанa (скраћено GAGs ) или мукополисахарида. Акумулација делимично деградираних продуката ГАГ-а изазива сметње у ћелији, ткиву и нарушава функције појединих органа.
| Мукополисахаридоза тип I H-S | |
|---|---|
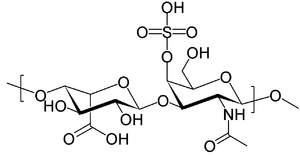 | |
| Молекул дерматан сулфата који се акумулирају у лизозомима пацијената са МПС I | |
| Симптоми | Симптоми су варијабилни, али могу укључивати: блаже пореемећаје у учењу, психијатријске проблеме, визуелне проблеме, скелетне деформације, синдром карпалног тунела, болест аортни залистка и/или апнеју током спавања. |
| Време појаве | Симптоми се могу појавити до 5 године; дијагноза се обично поставља након 10 година |
| Узроци | недостатком ензима алфа-L-идуронидазе |
| Слична обољења | MPS I; Хантеров синдром; остале мукополисахаридозе |
| Лечење | Заменска терапија ензимима; хируршки |
| Прогноза | Смрт се обично јавља пре 12 година (Hurler синдром/ тешки облик); Животни век може бити нормалан (Scheie синдром, одређена форма) |
| Фреквенција | 1 у 115.000[1] |
Недостатак алфа-Л-идуронидазе може довести до широког спектра фенотипског ангажовања са три главна призната клиничка субјекта: Хурлеров синдром (MПС тип I H; 607014), Hurler-Scheie синдром (МПС I H-S; 607015), и Scheie синдром (MPS тип I S). Хурлеров и Scheie синдром представљају два различита фенотипа МПС тип I синдрома — на тежем (МПС I H) и лакшем (MPS тип I S) крају клиничког спектра, док је Hurler-Scheie синдром (MPS тип I H-S) трећи или интермедијерни облик у фенотипској експресији.[2]
Историја уреди
Најтежи облик мукополисахаридозе тип I, који укључује замагљивање рожњаче, абнормалности скелета и менталну ретардацију, добио је назив Хурлеров синдром по немачкој педријатрици Гертруди Хурлер, која је прва описала поремећај 1919. године.[3][4]
Године 1962, амерички лекар Harold Glendon Scheie (1909–1990), идентификово је блажу варијанту Хурлеровог синдрома, МПС тип I S која је по њему названа Scheie синдром.[5]
McKusick, V. A. и сар. (1972) предложили су да се Хурлеров синдром назове — мукополисахаридоза тип I H (скраћено МПС тип I H) а Scheie синдром — мукополисахаридоза тип I S (скраћено МПС тип I S).[6]
Године 1985. Рубичек и сар. приказали су пет пацијената са недостатком алфа-Л-идуронидазе и фенотипом који је атипичан за Хурлеров синдром и Scheie синдром. Међу разним могућим објашњењима за овај фенотип, они су прихватили тумачење која се заснива на постојању генетичких варијанти за неке од случајева, које су узроковане различитим мутацијама.[7]
Епидемиологија уреди
Преваленца синдрома се процењује на 1 случај на 115.000.
Етиологија уреди
MPS тип I H-S је узрокован мутацијама у IDUA гену (4p16.3) што доводи до парцијалног недостатка ензима алфа-Л-идуронидазе и лизозомске акумулације дерматан сулфата и хепаран сулфата.[8]
Клиничка слика уреди
Симптоми се најчешће јављају после 5 година, али су тако благи да се дијагноза често не узима у обзир све до 10 године или одрасле доби.
- Пацијенти су скоро нормалне висине и не показују интелектуални недостатак.
- Замућење рожњаче се одвија прогресивно и дифузно, обично после четврте године живота.
- Глауком је чешћи него код Хурлеровог синдрома
- Пацијенти су благо измењеног изглда лица, укључујући и велика уста са дебелим уснама.
- Често је присутна ринореја и неуросензуални губитак слуха,
- Зглобови су крути (због контрактура), и прате их благе промене скелета и синдром карпалног тунела.
У тежим облицима може се јавити
- болест аортног залистка,
- компресија цервикалне кичмене мождине, изазвана инфилтрацијом гликозаминогликана у дури, што може довести до спастичне паресије, ако се не поправи неурохируршким интервенцијама.
Дијагноза уреди
Рана дијагноза је тешка због првих неспецифичних клиничких симптома, али је од суштинског значаја за хитно иницирање третмана.
Дијагноза се заснива на детекцији повећаног излучивања у мокраћи хепаран сулфата и дерматан сулфата и генетским тестовима. Тестирање са заснива на примени бојења метилен плавим и GAG електрофорези, и доказивању недостатка ензима у леукоцитима и фибробластима.[9]
Пошто је у мукополисахаридози тип I H-S нападнута већина органа који су код деце у фази формирања, важно је пратити све потенцијалне компликације, најмање једном годишње након потврде дијагнозе. Ови прегледи треба да укључују неуролошку процену и процену функција очију, слуха, срца, плућа, скелета и зуба. Понекад су потребни рендгенски снимци или друге додатне дијагностичке методе за извођење ових контролних испитивања.
Пренатална дијагноза уреди
Пренатална дијагноза мукополисахаридоза тип I H-S, данас је могућа уз помоћу амниоцентезе и узорковања слоја ткива у ембриону (биопсијом хорионских ресица). Дијагноза мора бити потврђена пре 11 недеља гестације.
Диференцијална дијагноза уреди
Диференцијално дијагностички треба имати у виду следеће болести:
- Хантеров синдром (Мукополисахаридозу тип II)
- Санфилипов синдром (Мукополисахаридозу тип III)
- Morquio синдром (Мукополисахаридозу тип IV)
- Maroteaux-Lamy синдром (Мукополисахаридозу тип VI)
- Sly синдром (Мукополисахаридозу тип VII)
Терапија уреди
Лечење се спроводи заменском ензимском терапијом - хуманом рекомбинантном алфа-L-идуронидазом уз супортивне мере зависно од врсте присутних симптома, или трансплантацијом коштане сржи Најбољи резултати терапије се постижу уколико је лечење започето рано, пре наступања иреверзибилних промена.[10]
Ензимска терапија уреди
Ензимска заменска терапија се заснива на примени хумане рекомбинантне алфа-L-идуронидазе, у недељној инфузији, како би се осигурала одговарајућа количина ензима потребна организму за побољшање укупног квалитета живота.[11][12][13][14][15][16]
Tретман се показао ефикасним за побољшање фунција зглобова, функцију плућа и побољшање општег здравља. Међутим, не треба очекивати да же заменска терапија ензима да смањењи ефекате поремећаја на очим и срчаним залистцима. Такође нема доказа да се акумулација МПС супстанце у мозгу спречава или смањује, јер ензим не прелази крвно-мождану баријеру. Студије су у току како би се утврдило да ли се акумулације у кичми могу спречити применом лека директним убризгавањем у кичмену течност. Међутим за то су потребне даље студије и дуже праћење за правилну процену ефикасности терапије ензимима директно у крвоток или кичмену течност.
Симптоматска терапија уреди
Симптоматски и подржавајући третман може захтвати координиране напоре тима специјалиста:
- Педијатра (неуролога), који процењују и лечи поремећаје нервног система),
- Ортопдеда који дијагностикују и лече скелетне абнормалности
- Педијатра (кардиолога), који дијагностикују и лече срчане абнормалности
- Физиотерапеута и/или осталих здравствених радника који требају бити систематски и свеобухватно ангажовани у лечењу оболелог детета.
- Медицинске генетске, чије јсаветодавнане услуге могу бити корисне за мајке и породицу.
Прогноза уреди
Прогноза код МПС типа I H-S као средње тешког облика мукополисахаридоза нешто је повољнија од оне код МПС типа I H. Симптоми се развијају током касних тинејџерских година до раних двадесетих и зантно су блажи од симптома који су примећени у Хурлеровом синдрому.[17]
Извори уреди
- ^ „Mucopolysaccharidoses Fact Sheet”. National Institute of Neurological Disorders and Stroke. 15. 11. 2017. Приступљено 25. 6. 2018.
- ^ McKusick, V. A., Howell, R. R., Hussels, I. E., Neufeld, E. F., Stevenson, R. E. Allelism, nonallelism and genetic compounds among the mucopolysaccharidoses. Lancet 299: 993-996, 1972.
- ^ Hurler's syndrome на сајту Who Named It
- ^ Hurler, G. (1919). „Über einen Typ multipler Abartungen, vorwiegend am Skelettsystem”. Zeitschrift für Kinderheilkunde. Berlin. 24: 220—234.
- ^ Moore, David; Connock, Martin J.; Wraith, Ed; Lavery, Christine (1. 1. 2008). „The prevalence of and survival in Mucopolysaccharidosis I: Hurler, Hurler-Scheie and Scheie syndromes in the UK”. Orphanet Journal of Rare Diseases. 3: 24. ISSN 1750-1172. PMC 2553763 . PMID 18796143. doi:10.1186/1750-1172-3-24.
- ^ McKusick, V. A., Howell, R. R., Hussels, I. E., Neufeld, E. F., Stevenson, R. E. Allelism, nonallelism and genetic compounds among the mucopolysaccharidoses. Lancet 299: 993-996, 1972.
- ^ Roubicek M, Gehler J, Spranger J. The clinical spectrum of alpha-L-iduronidase deficiency. Am J Med Genet. 1985 Mar;20(3):471-81.
- ^ Menon, K. P., Tieu, P. T., Neufeld, E. F. Architecture of the canine IDUA gene and mutation underlying canine mucopolysaccharidosis I. Genomics 14: 763-768, 1992.
- ^ „Syndrome de Scheie”. Orphanet, ORPHA:93474. Приступљено 26. 6. 2018.
- ^ Muenzer J and Fisher A. Advances in the Treatment of Mucopolysaccharidosis Type I. New Engl J Med. 2004;350:1932-34.
- ^ Desnick RJ. Enzyme replacement and enhancement therapies for lysosomal diseases. J. Inherit Metab Dis. 2004;27:385-410.
- ^ Wraith JE, Clarke LA, Beck M, et al. Enzyme replacement therapy for mucopolysaccharidosis I: a randomized, double-blinded, placebo-controlled, multinational study of recombinant human alpha-L-iduronidase (laronidase). J Pediatr. 2004;144:581-88.
- ^ Malm G, et al., Mucopolysaccharidoses. New therapeutic possibilities increase the need of early diagnosis. Lakartidningen. 2002;99:1804-9
- ^ Kakkis ED, Enzyme replacement therapy for the mucopolysaccharides storage disorders. Expert Opin Investig Drugs. 2002;11:675-85.
- ^ Wraith JE, Enzyme replacement therapy in mucopolysaccharidosis type I: progress and emerging difficulties. J Inherit Metab Dis. 2001;24:245-50.
- ^ Kakkis ED, et al., Enzyme-replacement therapy in mucopolysaccharidosis I. N Engl J Med. 2001;344:182-8.
- ^ Yano S, Moseley K, Pavlova Z. Postmortem studies on a patient with mucopolysaccharidosis type I: Histopathological findings after one year of enzyme replacement therapy. J Inherit Metab Dis. 2009 Mar 27.
Литература уреди
- Fauci AS, et al., eds. Harrison’s Principles of Internal Medicine, 14th Ed. New York, NY: McGraw-Hill, Inc; 1998:2169-76.
- Beighton P, ed. Mckusick’s Heritable Disorders of Connective Tissue. 5th ed. St. Louis, MO: Mosby-Year Book, Inc; 1993:1118-9.
- Eto Y, Ohashi T, Gene therapy/cell therapy for lysosomal storage disease. J Inherit Metab Dis. 2000;293-8.
- Triggs-Raine B, et al., Mutations in HYAL1, a member of a tandemly distributed multigene family encoding disparate hyaluronidase activities, cause a newly described lysosomal disorder, mucopolysaccharidosis IX. Proc Natl Acad Sci USA. 1999;95:6296-300.
- Natowicz MR, et al., Clinical biochemical manifestations of hyaluronidase deficiency. N Engl J Med. 1996;335:1029-33.
- Herrick IA, et al., The mucopolysaccharidoses and anaesthesia: a report of clinical experience. Can J Anaesth. 1988;35:67-73.
- Sjogren P, et al., Mucopolysaccharidoses and anaesthetic risks. Acta Anaesthesiol Scand. 1987;31:214-8.
- Caruso RC, et al., Electroretinographic findings in the mucopolysaccharidoses. Ophthalmology. 1986;93::1612-6.
Спољашње везе уреди
- Mucopolysaccharidoses Types I-VII (језик: енглески)
- Mucopolysaccharidoses Fact Sheet (језик: енглески)
| Класификација | |
|---|---|
| Спољашњи ресурси |
| Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |