Медицинска хемија
Медицинска хемија или фармацеутска хемија је дисциплина на раскршћу хемије, фармакологије, и биологије која обухвата дизајн, синтезу и развој фармацеутиских лекова. Медицинска хемија се бави идентификацијом, синтезом и развојем нових хемијских ентитета подесних за терапеутску употребу. Она такође обухвата изучавање постојећих лекова, њихових биолошких осовина, и њихових квантитативних односа структуре и активности (QSAR).[1][2][3][4] Медицинска хемија је високо интердисциплинарна наука која комбинује органску хемију са биохемијом, рачунарском хемијом, фармакологијом, фармакогнозијом, молекуларном биологијом, статистиком, и физичком хемијом.
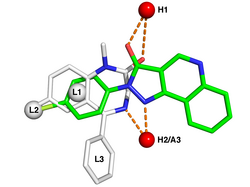
Једињења која се користе као лекови су првенствено органска једињења, која могу да буду мали органски молекули (е.г., аторвастатин, флутиказон, клопидогрел) и биополимери (инфликсимаб, еритропоиетин, инсулин гларгин), од којих су потоњи најчешће протеински лековити препарати (природна и рекомбинантна антитела, хормони итд). Међутим, и за неорганска једињења и једињења која садрже метале је нађено да могу да буду корисни лекови. На пример, цисплатин серија комплекса који садрже платину се користи у третману рака, и литијум базирани медикаменти имају дугу традицију у лечењу низа менталних обољења. Дисциплина медицинске неорганске хемије истражује улогу метала у медицини (металотерапеутика), што укључује проучавање и лечење болести и здравствених стања повезаних са неорганским металима у биолошким системима. Постоји неколико металотерапеутика одобрених за лечење рака (нпр. садрже Пт, Ру, Гд, Ти, Ге, V и Га), антимикробних средстава (нпр. Аг, Цу и Ру), дијабетеса (нпр. V и Цр), антибиотик широког спектра (нпр. Би), биполарног поремећаја (нпр. Ли).[5][6] Остале области студија укључују: металомику, геномику, протеомику, дијагностичке агенсе (нпр. МРИ: Гд, Мн; рендгенски: Ба, I) и радиофармацеутике (нпр. 99мТц за дијагностику, 186Ре за терапију).
Конкретно, медицинска хемија у својој најчешћој пракси – фокусирајући се на мале органске молекуле – обухвата синтетичку органску хемију и аспекте природних производа и компјутерску хемију у блиској комбинацији са хемијском биологијом, ензимологијом и структурном биологијом, заједно са циљем откривања и развоја нових терапеутска средства. Практично говорећи, то укључује хемијске аспекте идентификације, а затим систематску, темељну синтетичку измену нових хемијских ентитета како би се учинили погодним за терапеутску употребу. Она укључује синтетичке и рачунарске аспекте проучавања постојећих лекова и агенаса у развоју у односу на њихове биоактивности (биолошке активности и својства), односно разумевање њихових односа структуре и активности (САР). Фармацеутска хемија је фокусирана на аспекте квалитета лекова и има за циљ да обезбеди њихову погодност за дату намену.[7]
Процес развоја лекова
уредиОткривање
уредиОткривање је идентификација нових активних једињења, која се често називају „погоци“. Они се типично налазе тестирањем великог броја једињења (колекција једињења) за жељене биолошке особине.[8] Док постоје бројни приступи идентификацији погодатака, неке од најуспешнијих техника су засноване на хемијској и биолошкој интуицији која је развијена током година ригорозног хемијско-биолошког тренинга. Иницијална позитивна једињења могу да потичу од налажења нових видова примене постојећих агенаса у новим патолошким процесима,[9] и од запажања биолошких дејстава нових или постојећих природних продуката, као што су биљке,[10] животиње, или гљиве.[11] Погоци могу такође да долазе из синтетичких хемијских колекција, као што су колекције креиране путем комбинаторне хемије, или историјских колекција хемијских једињења, које се масовно тестирају за активност на одређеном биолошком циљу.
Оптимизација
уредиСледећи ступањ у развоју лекова су даље хемијске модификације с циљем побољшања биолошких, ADME и физико-хемијских особина дате колекције једињења. Хемијске модификације могу да побољшају препознавање и геометрију везивања (фармакофоре) кандидата, њихов афинитет и фармакокинетику, или њихову реактивност и стабилност ка метаболичкој деградације. Бројни методи се користе за квалитативно и квантитативно предвиђање метаболичке стабилности[12], као и низа других ADMET особина. Модели квантитативних односа структуре и активности (QSAR) заједно са фармакофорном анализом помажу налажење водећих једињења, која показују највећу потентност и селективност, имају најбоље фармакокинетичке особине и најмању токсичност.
Развој
уредиЗавршни ступањ се састоји од припреме водећих једињења за употребу у клиничким испитивањима. Развој обухвата оптимизацију синтетичког приступа за производњу већих количина материјала, и припрему подесне формулације лека.
Референце
уреди- ^ Тхомас L. Лемке; Давид А. Wиллиамс, ур. (2007). Фоyе'с Принциплес оф Медицинал Цхемистрy (6. изд.). Балтиморе: Липпинцотт Wилламс & Wилкинс. ИСБН 0781768799.
- ^ Хардман ЈГ, Лимбирд ЛЕ, Гилман АГ (2001). Гоодман & Гилман'с Тхе Пхармацологицал Басис оф Тхерапеутицс (10. изд.). Неw Yорк: МцГраw-Хилл. ИСБН 0071354697. дои:10.1036/0071422803.
- ^ Давис А, Wард СЕ, ур. (2015). Хандбоок оф Медицинал Цхемистрy: Принциплес анд Працтице. Роyал Социетy оф Цхемистрy. ИСБН 978-1-78262-419-6. дои:10.1039/9781782621836.
- ^ Баррет Р (2018). Медицинал Цхемистрy: Фундаменталс. Лондон: Елсевиер. ИСБН 978-1-78548-288-5.
- ^ Ханиф M, Yанг X, Тиноцо АД, Плаżук D (2020-05-28). „Едиториал: Неw Стратегиес ин Десигн анд Сyнтхесис оф Инорганиц Пхармацеутицалс”. Фронтиерс ин Цхемистрy. 8: 453. Бибцоде:2020ФрЦх....8..453Х. ПМИД 32548093. дои:10.3389/фцхем.2020.00453 .
- ^ Антхонy ЕЈ, Болитхо ЕМ, Бридгеwатер ХЕ, Цартер ОW, Доннеллy ЈМ, Имберти C, et al. (новембар 2020). „Metallodrugs are unique: opportunities and challenges of discovery and development”. Chemical Science. 11 (48): 12888—12917. doi:10.1039/D0SC04082G.
- ^ Roughley SD, Jordan AM (мај 2011). „The medicinal chemist's toolbox: an analysis of reactions used in the pursuit of drug candidates”. Journal of Medicinal Chemistry. 54 (10): 3451—3479. PMID 21504168. doi:10.1021/jm200187y.
- ^ Hughes, Jp; Rees, S; Kalindjian, Sb; Philpott, Kl (1. 3. 2011). „Principles of early drug discovery”. British Journal of Pharmacology (на језику: енглески). 162 (6): 1239—1249. ISSN 1476-5381. PMC 3058157 . PMID 21091654. doi:10.1111/j.1476-5381.2010.01127.x.
- ^ Johnston, Kelly L.; Ford, Louise; Umareddy, Indira; Townson, Simon; Specht, Sabine; Pfarr, Kenneth; Hoerauf, Achim; Altmeyer, Ralf; Taylor, Mark J. (1. 12. 2014). „Repurposing of approved drugs from the human pharmacopoeia to target Wolbachia endosymbionts of onchocerciasis and lymphatic filariasis”. International Journal for Parasitology: Drugs and Drug Resistance. Includes articles from two meetings: "Anthelmintics: From Discovery to Resistance", pp. 218--315, and "Global Challenges for New Drug Discovery Against Tropical Parasitic Diseases", pp. 316--357. 4 (3): 278—286. PMC 4266796 . PMID 25516838. doi:10.1016/j.ijpddr.2014.09.001.
- ^ Cragg, Gordon M.; Newman, David J. (1. 6. 2013). „Natural products: A continuing source of novel drug leads”. Biochimica et Biophysica Acta (BBA) - General Subjects. 1830 (6): 3670—3695. PMC 3672862 . PMID 23428572. doi:10.1016/j.bbagen.2013.02.008.
- ^ Harvey, Alan L. (1. 10. 2008). „Natural products in drug discovery”. Drug Discovery Today. 13 (19–20): 894—901. PMID 18691670. doi:10.1016/j.drudis.2008.07.004.
- ^ Smith, J.; Stein, V. (2009). „SPORCalc: A development of a database analysis that provides putative metabolic enzyme reactions for ligand-based drug design”. Computational Biology and Chemistry. 33 (2): 149—159. PMID 19157988. doi:10.1016/j.compbiolchem.2008.11.002.
Literatura
уреди- D. Radulović, S. Vladimirov, Farmaceutska hemija I deo, Farmaceutski fakultet, Beograd, 2005.
- S. Vladimirov, D. Živanov-Stakić, Farmaceutska hemija II deo, Farmaceutski fakultet, Beograd, 2006.
- John M. Beale; John Block, ур. (2010). Wilson and Gisvold's Textbook of Organic Medicinal and Pharmaceutical Chemistry (Twelfth изд.). London, Philadelphia, New York,: Lippincott Williams & Wilkins. ISBN 978-0-7817-7929-6.
- Watson, David G. (2005). Pharmaceutical Analysis: A Textbook for Pharmacy Students and Pharmaceutical Chemists (second изд.). Edinburg: Churchill Livingstone. ISBN 978-0-443-07445-5.
- Foreman, John C.; Johansen, Torben; Gibb, Alasdair J. (2009). Textbook of Receptor Pharmacology, Second Edition. CRC Press. ISBN 9781439887578.
- Brunton, Laurence (2011). Brunton, L. L.; Chabner, Bruce; Knollmann, Björn C., ур. Goodman and Gilman's The Pharmacological Basis of Therapeutics (12 изд.). New York: McGraw-Hill. ISBN 978-0-07-162442-8.
- Whalen, Karen (2014). Lippincott Illustrated Reviews: Pharmacology.
- Takács-Novák, K.; Avdeef, A. (август 1996). „Interlaboratory study of log P determination by shake-flask and potentiometric methods”. Journal of Pharmaceutical and Biomedical Analysis. 14 (11): 1405—13. PMID 8877846. doi:10.1016/0731-7085(96)01773-6.
- Luch A, ур. (2009). Molecular, clinical and environmental toxicology. Springer. стр. 20. ISBN 978-3-7643-8335-0. Архивирано из оригинала 6. 8. 2020. г. Приступљено 21. 7. 2020.
- Brater DC, Daly WJ (мај 2000). „Clinical pharmacology in the Middle Ages: principles that presage the 21st century”. Clinical Pharmacology and Therapeutics. 67 (5): 447—50. PMID 10824622. S2CID 45980791. doi:10.1067/mcp.2000.106465.
- Hollinger, Mannfred A. (2003). Introduction to pharmacology. CRC Press. стр. 4. ISBN 0-415-28033-8. Архивирано из оригинала 17. 4. 2021. г. Приступљено 27. 6. 2015.
- Rang HP (јануар 2006). „The receptor concept: pharmacology's big idea”. British Journal of Pharmacology. 147 Suppl 1 (S1): S9—16. PMC 1760743 . PMID 16402126. doi:10.1038/sj.bjp.0706457.
- Maehle AH, Prüll CR, Halliwell RF (август 2002). „The emergence of the drug receptor theory”. Nature Reviews. Drug Discovery. 1 (8): 637—41. PMID 12402503. S2CID 205479063. doi:10.1038/nrd875.
- Rang HP, Dale MM, Ritter JM, Flower RJ (2007). Pharmacology. China: Elsevier. ISBN 978-0-443-06911-6.
- Masood N. Khan; John W. Findlay, ур. (2009). Ligand-binding assays development, validation, and implementation in the drug development arena. Hoboken, N.J.: John Wiley & Sons. ISBN 978-0470541494.
- „Psychopharmacology | Psychology Today International”. www.psychologytoday.com. Архивирано из оригинала 24. 2. 2022. г. Приступљено 2020-07-23.
- „What is Psychopharmacology”. ascpp.org. 29. 11. 2012. Архивирано из оригинала 23. 7. 2020. г. Приступљено 2020-07-23.
- Gomez A, Ingelman-Sundberg M (април 2009). „Pharmacoepigenetics: its role in interindividual differences in drug response”. Clinical Pharmacology and Therapeutics. 85 (4): 426—30. PMID 19242404. S2CID 39131071. doi:10.1038/clpt.2009.2.
- „What is Clinical Pharmacology?”. ascpt.org. Архивирано из оригинала 31. 10. 2021. г. Приступљено 31. 10. 2021.
- „Posology, Factors Influencing Dose, Calculation of Doses”. pharmamad.com. 23. 1. 2019. Архивирано из оригинала 31. 10. 2021. г. Приступљено 31. 10. 2021.
- „The Science of Pharmacology & Toxicology”. Faculty of Medicine, University of Toronto. Архивирано из оригинала 16. 7. 2019. г. Приступљено 16. 7. 2019.
Spoljašnje veze
уреди- „Medicinska hemija”. Приступљено 14. 4. 2011.
- Američko hemijsko društvo, odeljenje medicinske hemije
- Evropska federacija za medicinsku hemiju
- Vodič za razvoj lekova
- Pregled medicinske hemije