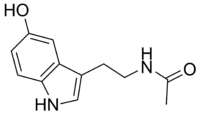
N-Acetilserotonin
N-Ацетилсеротонин (НАС, нормелатонин) је природни интермедијер у ендогеној продукцији мелатонина из серотонина.[3][4] Он се формира из серотонина посредством ензима аралкиламинска N-ацетилтрансфераза (ААНАТ) и конвертује се у мелатонин дејством ацетилсеротонин О-метилтрансферазе (АСМТ). Попут мелатонина, НАС је агонист мелатонинских рецептора МТ1, МТ2, и МТ3, и може се сматрати неуротрансмитером.[5][6][7][8] Осим тога, НАС је присутан у појединим областима мозга где серотонин анд мелатонин нису заступљени, из чега следи да он има једиствене улоге, и да није само прекурзор у синтези мелатонина.[5]
| |

| |
| Називи | |
|---|---|
| IUPAC назив
N-[2-(5-hidroksi-1H-indol-3-il)etil]acetamid
| |
| Други називи
N-ацетил-5-хидрокситриптамин, N-ацетил-5-ХТ
| |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.013.560 |
| МеСХ | Н-Ацетyлсеротонин Н-Ацетyлсеротонин |
| |
| Својства | |
| C12H14N2O2 | |
| Моларна маса | 218,252 g/mol |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |
| Референце инфокутије | |
Референце уреди
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ AXELROD J, WEISSBACH H (1960). „Enzymatic O-methylation of N-acetylserotonin to melatonin”. Science. 131 (3409): 1312. PMID 13795316. doi:10.1126/science.131.3409.1312.
- ^ WEISSBACH H, REDFIELD BG, AXELROD J (1960). „Biosynthesis of melatonin: enzymic conversion of serotonin to N-acetylserotonin”. Biochimica et Biophysica Acta. 43: 352—3. PMID 13784117. doi:10.1016/0006-3002(60)90453-4.
- ^ а б Jang SW; Liu X; Pradoldej S; et al. (2010). „Н-ацетyлсеротонин ацтиватес ТркБ рецептор ин а цирцадиан рхyтхм”. Процеедингс оф тхе Натионал Ацадемy оф Сциенцес оф тхе Унитед Статес оф Америца. 107 (8): 3876. ПМЦ 2840510 . ПМИД 20133677. дои:10.1073/пнас.0912531107.
- ^ Зхао Х, Поон АМ, Панг СФ (2000). „Пхармацологицал цхарацтеризатион, молецулар субтyпинг, анд ауторадиограпхиц лоцализатион оф путативе мелатонин рецепторс ин утерине ендометриум оф естроус ратс”. Лифе Сциенцес. 66 (17): 1581—91. ПМИД 11261588. дои:10.1016/С0024-3205(00)00478-1.
- ^ Нонно Р, Паннацци M, Луцини V, Ангелони D, Фрасцхини Ф, Станков БМ (1999). „Лиганд еффицацy анд потенцy ат рецомбинант хуман МТ2 мелатонин рецепторс: евиденце фор агонист ацтивитy оф соме мт1-антагонистс”. Бритисх Јоурнал оф Пхармацологy. 127 (5): 1288—94. ПМЦ 1566130 . ПМИД 10455277. дои:10.1038/сј.бјп.0702658.
- ^ Паул П, Лахаyе C, Делагранге П, Ницолас ЈП, Цанет Е, Боутин ЈА (1999). „Цхарацтеризатион оф 2-[125И]иодомелатонин биндинг ситес ин Сyриан хамстер перипхерал органс”. Тхе Јоурнал оф Пхармацологy анд Еxпериментал Тхерапеутицс. 290 (1): 334—40. ПМИД 10381796. Архивирано из оригинала 15. 12. 2019. г. Приступљено 01. 11. 2012.