Стирен
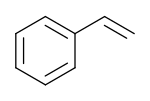
Стирен (винил-бензен, цинамен, стирол, етенбензен, фенетилен, стиропол) је органски једињење које припада групи ароматичних угљоводоника.[4][5] Његова хемијска формула је C6H5CH=CH2. Под нормалним условима, он је уљаста течност која лако испарава. Има слаткаст мирис ако је чист, мада због примјеса његов мирис може да буде неугодан. Стирен је међупроизвод у производњи важног синтетичког материјала полистирена (стиропора).[6]
| |

| |
| Називи | |
|---|---|
| Преферисани IUPAC назив
Пхенyлетхене | |
| Системски IUPAC назив
Етхенyлбензене | |
| Други називи
Винил бензен; цинамен; стирол; фенилетен; диарекс ХФ 77; стиролен; стиропол; винилбензен
| |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.002.592 |
| КЕГГ[1] | |
| RTECS | WЛ3675000 |
| УНИИ | |
| |
| Својства | |
| C8H8 | |
| Моларна маса | 104,15 g/mol |
| Агрегатно стање | безбојна уљаста течност |
| Густина | 0,909 g/cm³ |
| Тачка топљења | −30 °C (−22 °F; 243 K) |
| Тачка кључања | 145 °C (293 °F; 418 K) |
| < 1% | |
| Индекс рефракције (nD) | 1.5469 |
| Вискозност | 0.762 cP at 20°C |
| Структура | |
| Диполни момент | 0.13 D |
| Опасности | |
| Опасност у току рада | запаљив, токсичан |
| Безбедност приликом руковања | MSDS |
| R-oznake | R10 R36 |
| S-oznake | S38 S20 S23 |
| NFPA 704 | |
| Tačka paljenja | 31 °C |
| Сродна једињења | |
Сродне стирени
ароматична једињења |
Полистирен, Стилбен Етхилбензен |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |
| Референце инфокутије | |
Историја уреди
Мање количине стирена се могу природно наћи у неким биљкама, као и многим прехрамбеним производима попут воћа, поврћа, ораха, пића и меса. Производи се у великим количинама из бензена и етена преко међупроизвода етилбензена. У Америци током Другог свјетског рата драматично је повећана његова производња стирена за потребе војне индустрије, услед пораста потражње за синтетичком гумом. Пошто молекул стирена има винилну функционалну групу са двоструком везом, он има способност формирања полимера.
Референце уреди
- ^ Јоанне Wиxон; Доуглас Келл (2000). „Wебсите Ревиеw: Тхе Кyото Енцyцлопедиа оф Генес анд Геномес — КЕГГ”. Yеаст. 17 (1): 48—55. дои:10.1002/(СИЦИ)1097-0061(200004)17:1<48::АИД-YЕА2>3.0.ЦО;2-Х.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th изд.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
- ^ Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. 2005.
