Таутомер
Таутомери су изомери (конституциони изомери) органских једињења који се лако конвертују из једног у други облик хемијском реакцијом званом таутомеризација.[1][2] Та реакција обично доводи до формалне миграције атома водоника или протона, што се остварује заменом једноструке везе и суседне двоструке везе. Концепт таутомеризације се назива таутомеризам. Због брзе интерконверзије, таутомери се генерално сматрају истим хемијским једињењем. Таутомеризам је специјални случај структурног изомеризма и може да има важну улогу у неканоничком базном спаривању у ДНК, а посебно РНК молекулима.
Хемија уреди
У растворима у којима је таутомеризација могућа, остварује се хемијска равнотежа таутомера. Прецизан однос таутомера зависи од неколико фактора, укључујући температуру, растварач, и pH.[3]
Уобичајени таутомерни парови су:
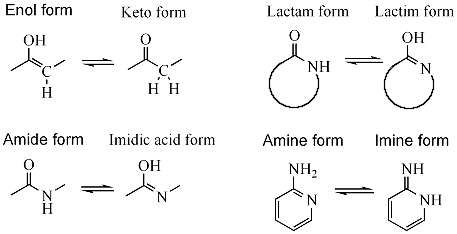
- кетон - енол, е.г., за ацетон (кето-енолни таутомеризам)
- кетен - инол, е.г., фор етенон
- амид - имидинска киселина, е.г., током реакције нитрилне хидролизе
- лактам - лактим, таутомеризам амид - имидинска киселина у хетероцикличним прстеновима, е.г., у нуклеобаза гуанин, тимин, и цитозин
- енамин - имин
- аномери редукујућих шећера у раствору се интерконвертују путем интермедијарног облика отвореног ланца.
Прототропија уреди
Прототропија је најчешчи облик таутомерије. Он се односи се на премештање протона.[4] Прототропни таутомеризам се може сматрати подскупом кисело-базног понашања. Прототропни таутомери су скупови изомерних протонационих стања са истом емпиријском формулом и тоталним наелектрисањем.
Таутомеризације се катализују:
- Базама (1. депротонација; 2. формирање делокализованог ањон (е.г., енолата); 3. протонација на различитој позицији ањона).
- Киселинама (1. протонација; 2. формирање делокализованог катјона; 3. депротонација на различитој позицији поред катјона).
- Ануларни таутомеризам
- тип прототропног таутомеризма, где протон може да заузима две или више позиција на хетероцикличном систему, на пример, 1H- и 3H-имидазол; 1H-, 2H- и 4H- 1,2,4-триазол; 1H- и 2H- изоиндол.[3]
Референце уреди
- ^ Смитх, Мицхаел Б.; Марцх, Јеррy (2007). Адванцед Органиц Цхемистрy: Реацтионс, Мецханисмс, анд Струцтуре (6тх изд.). Неw Yорк: Wилеy-Интерсциенце. ИСБН 0-471-72091-7.
- ^ Катритзкy А.Р.; Позхарскии А.Ф. (2000). Хандбоок оф Хетероцyцлиц Цхемистрy (Сецонд изд.). Ацадемиц Пресс. ИСБН 0080429882.
- ^ а б Балабин, Роман M. (2009). „Таутомериц еqуилибриум анд хyдроген схифтс ин тетразоле анд триазолес: Фоцал-поинт аналyсис анд аб инитио лимит”. Јоурнал оф Цхемицал Пхyсицс. 131 (15): 154307. Бибцоде:2009ЈЦхПх.131о4307Б. дои:10.1063/1.3249968.
- ^ ИУПАЦ Голд Боок таутомерисм