Тромбоемболизам у преткоморској фибрилацији
Тромбоемболизам у преткоморској фибрилацији приписује се емболији тромбом који потиче из леве срчане преткоморе. Преткоморска фибрилација најчешћа је аритмија у клиничкој пракси, одговорна за око трећину хоспитализација због поремечаја срчаног ритма. Патогенеза тромбоемболизма као узрока преткоморске фибрилацијије јако је сложена и биће делимично објашњена на овој страници.[1]
| Тромбоемболизам у преткоморској фибрилацији | |
|---|---|
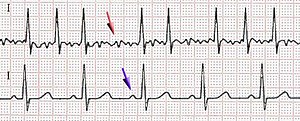 | |
| ЕКГ болесника са АФ на коме је црвеном стрелицом означено место где се уместо постојаних Р-таласа, на снимку бележе брзе осцилације или фибрилаторни таласи (горе) и физиолошки ЕКГ са нормалним изгледом Р-таласа (доле) | |
| Класификација и спољашњи ресурси | |
| МКБ-10 | И48 |
| МКБ-9-CM | 427.31 |
| ДисеасесДБ | 1065 |
| МедлинеПлус | 000184 |
| еМедицине | мед/184 емерг/46 |
| МеСХ | Д001281 |
Основни појмови
уреди- Преткоморска фибрилација
Преткоморска фибрилација или атријална фибрилација је тахиаритмија преткомора коју одликује неусклађеена деполаризација преткомора, што има за последицу поремећај механиåке функције преткомора. Електрокардиографски се, током преткоморске фибрилације, уместо постојаних П-таласа, бележе брзе осцилације или фибрилаторни таласи који варирају у величини, облику и времену појављивања.
- Тромбоемболизам
Блокада крвних судова изазвана угрушком крви, који се одвојио од свог првобитног места формирања.
Епидемиологија
уредиДо 25% можданих удара код болесника са преткоморском фибрилацијом може настати услед основне цереброваскуларне болести, других срчаних извора емболизма или атероматозе лука аорте.[2][3]
Учесталост можданог удара код болесника са преткоморском фибрилацијом увећава се са староћу становништва на чак 36% код болесника старијих од 80 до 89 година. Половина старијих болесника са преткоморском има хроничну артеријску хипертензију (која је основни фактор ризика за цереброваскуларну болест), а приближно 12% има клинички скривену стенозу каротидне артерије.[4]
Атеросклероза каротидних артерија нема знатно већу преваленцију код болесника са преткоморском фибрилацијом и можданим ударом, у поређењу са болесницима са можданим ударом без преткоморске фибрилације, и релативно је мање значајан фактор.
Патофизиологија настанка тромба
уредиФормирање тромба у левој преткомори почиње Вирховљевом тријадом коју чине; застој (стаза), ендотелна дисфункција и хиперкоагулабилно стање. Хемодинамски и хемостатски механизми одговорни за клиничке тромбоемболијске догађеје у преткоморској фибрилацији делимично су разјашњени испитивањем поремећаја коагулације крви код ових болесника.
Тромб, који је непосредно повезан са преткоморском фибрилацијом, најчешће се ствара у аурикули леве преткоморе, која се не може у потпуности приказати трансторакалним ехокардиограмом.[5] Трансезофагеална Доплер ехокардиографија је сензитиван и специфична метод за процену функције аурикуле леве преткоморе и за откривање тромботичког материјала. Тромби се чешће срећу код болесника са преткоморском фибрилацијом и исхемијским можданим ударом него код оних без можданог удара.[6]
- Застој у циркулацији
Серијска трансезофагеална испитивања леве преткоморе и њене аурикуле, током конверзије преткоморске фибрилације у синусни ритам, показала су смањење брзине протока у левој аурикули услед губитка организоване механичке контракције у преткоморској фибрилацији.
Смањење брзине протока у левој преткомори и њеној аурикули удружено је са појавом спонтаног ехоконтраста, са стварањем тромба и емболијским догађајима. Брзина протока у левој аурикули је мања код болесника са преткоморским флатером у поређењу са брзином протока код нормалног синусног ритма, али је већа него при преткоморској фибрилацији. Непозаница је да ли је због тога преваленца тромба у левој аурикули и стопа тромбоемболијских догађаја нешто ниже код преткоморског флатера. Иако се општеприхваћени терапијски приступ заснива на претпоставци да настанак тромба захтева непрекидно трајање преткоморске фибрилације, око 48 сати, трансезофагеалним ехокардиограмом су откривени тромби и у краћем временском периоду.[7][8][9][10][11][12]
- Ендотелна дисфункција
Тешко је доказати да је поремећај функције ендотела засебан механизам, одговоран за настанак тромба код болесника са преткоморском фибрилацијом, иако је концентрација вон Willebrandovog фактора у серуму и преткоморском ткиву повећана код неких болесника. Слично томе, преткоморска фибрилација је удружена и са биохемијским маркерима коагулације и активације тромбоцита, који можда одражвају системско хиперкоагулабилно стање.[13][14]
- Хиперкоагулабилно стање
Перзистентна и пароксизмална преткоморска фибрилација удружене су са повећењем серумских концентрација фибриногена и фибринског D-димера, који указују на активну интраваскуларну тромбогенезу. Повећање концентрације тромбоглобулина и тромбоцитног фактора IV, код одабраних болесника са преткоморском фибрилацијом, указују на активацију тромбоцита, али су ови подаци мање поуздани, у складу са мањом ефикасношћу антитромбоцитне терапије у превенцији тромбоемболијских компликација, ãто је доказано у клиничким студијама.[15] Ови биохемијски маркери коагулације и активације тромбоцита не омогућавају разликовање секундарног реактивног процеса услед интраваскуларног згрушавања од примарног хиперкоагулабилног стања. Неки од ових маркера коагулације нормализују се током антикоагулантне терапије, а неки се повећавају непосредно након конверзије у синусни ритам и затим враћају на нормалу.
Код болесника са реуматском митралном стенозом, који су били подвргнути транссепталној катетеризацији ради митралне балон-валвулопластике, доказан је регионални облик коагулопатије у левој преткомори. Концентрације фибринопептида А, комплекса тромбин-антитромбин III, и протромбинског фрагмента Ф1,2, биле су повећане у левој преткомори у односу на концентрације ових маркера у десној преткомори и бутној вени, што указује на регионалну активацију каскадних реакција коагулације.
Још увек није утврођено да ли је ова појава у преткоморској фибрилацији хемодинамски посредована високим притиском у левој преткомори, или су одговорни неки други механизми, али је доказано да је регионална коагулопатија удружена са налазом спонтаног ехо контраста у левој преткомори.
Супротно томе, инсуфицијенција митралног залистка валвуле умањује стазу у левој аурикули и удружена је са нижим степеном активације коагулациј. Спонтани ехо контраст је сложен феномен који ин витро зависи од брзине крвног протока, хематокрита и серумских протеина, укључујући фибриноген.
Код болесника са преткоморском фибрилацијом, независни предсказатељи појаве спонтаног ехо контраста јесу:
- величина леве преткоморе,
- брзина протока у левој аурикули,
- дисфункција леве коморе,
- концентрација фибриногена,
- хематокрит и
- атеросклероза аорте.[16][17]
Овај хемореолошки феномен представља ехокардиографски одраз регионалне коагулопатије и има клинички значај при откривању болесника са преткоморском фибрилацијом који су под високим ризиком од тромбоемболијских компликација.[18] Међутим још увек није утврђеена предност овог налаза у односу на уобичајену клиничку процену при проспективној стратификацији ризика од тромбоемболије.
Насупрот распрострањеном схватању да системска антикоагулантна терапија током четири недеље доводи до ендокардијалне адхеренције и организације тромба у левој аурикули, трансезофагеална проучавања су потврдила нестанак тромба код већине болесника.[19]
Готово иста запажања указала су на динамичну природу поремећаја функције леве преткоморе и њене аурикуле током конверзије преткоморске фибрилације, што логично узрокује потребу за антикоагулантном терапијом, неколико недеља пре и после успешне кардиоверзије.
Супротно томе, повећан проток у левој преткомори код болесника са митралном регургитацијом удружен је са мањом преваленцијом спонтаног ехо контраста у левој преткомори и мањом учесталошћу тромбоемболијских догђаја, чак и када је лева преткомора увећана.[20]
Клиничке последице
уредиКако поуздана патофизиологија тромбоемболизма код болесника са преткоморском фибрилацијом није са сигурношћу утврђена, механизми који повезују факторе ризика са исхемијским можданим ударом у преткоморској фибрилацији, такође, нису потпуно разјашњени.
Чврста повезаност између хипертензије и можданог удара код преткоморске фибрилације вероватно је посредована пре свега емболијом која потиче из леве срчане аурикуле,[21] али хипертензија такође повећава ризик од неемболијских мжданих удара у преткоморској фибрилацији.[22] Хипертензија код ових болесника повезана је са смањеном брзином протока у левој аурикули, појавом спонтаног ехо контраста, и настанком тромба.[23] Утицај хипертензије на хемодинамику леве преткоморе може бити последица поремећене дијастолне коморске функције, али овака повезаност је још увек је у разматрању јер је на нивоу претпоставке.[24] Основно питање је да ли дуготрајно лечење хипертензије смањује ризик од емболијских можданих удара при преткоморској фибрилацији, зато што су коморске дијастолне абнормалности које прате хипертензију код старих особа често мултифакторијалне и тешко су реверзибилне.[25]
Одмакло животно доба има вишеструки утицај на повећање ризика од можданог удара. Код болесника са преткоморском фибрилацијом, процес старења је удружен са појавом феномена који предиспонирају стварању тромба,[26] као што су увећање леве преткоморе, смањење брзине протока у левој аурикули и појава спонтаног ехо контраста. Поред тога, старије животно доба је фактор ризика за атеросклерозу, са настанком сложених атеросклеротских плакова на луку аорте, а удружено је и са можданим ударом независно од преткоморске фибрилације.[27]
Концентрација протромбинског активацијског фрагмента Ф1.2, показатеља стварања тромбина, повећава се са животним добом у општој популацији[160–162], као и код болесника са преткоморском фибрилацијом,[28] што указује на протромбинску дијатезу у старијем животном добу.
Поремећај функције леве коморе, на који указују анамнестички подаци о срчаном попуштању или трансторакалниехокардиографски преглед, повећава ризик од исхемијскогможданог удара код болесника са атријалном фибрилацијом,а који не узимају антитромботску терапију,[29] али не икод болесника са преткоморском фибрилацијом и умеренимризиком, који узимају аспирин.[30][31][32][33] Изведени закључци суконтрадикторни; дисфункција леве коморе је удружена и санастанком тромба у левој преткомори и са неемболијскимможданим ударима код болесника са преткоморском фибрилацијом.[34]
Укратко речено, током преткоморске фибрилације делују сложени тромбоемболијски механизми, који укључују међудејство фактора који се односе на стазу крви у левој преткомори и левој аурикули, поремећај функције ендотела и системску, а могуће је и локалну, хиперкоагулабилност.
Извори
уреди- ^ Халперин, Ј. L.; Харт, Р. Г. (1988). „Атриал фибриллатион анд строке: Неw идеас, персистинг дилеммас”. Строке. 19 (8): 937—41. ПМИД 3041652. С2ЦИД 14213519. дои:10.1161/01.СТР.19.8.937.
- ^ Богоусславскy, Ј.; Ван Мелле, Г.; Регли, Ф.; Каппенбергер, L. (1990). „Патхогенесис оф антериор цирцулатион строке ин патиентс wитх нонвалвулар атриал фибриллатион: Тхе Лаусанне Строке Регистрy”. Неурологy. 40 (7): 1046—50. ПМИД 2356005. С2ЦИД 9953973. дои:10.1212/WНЛ.40.7.1046.
- ^ Миллер, V. Т.; Ротхроцк, Ј. Ф.; Пеарце, L. А.; Феинберг, W. M.; Харт, Р. Г.; Андерсон, D. C. (1993). „Исцхемиц строке ин патиентс wитх атриал фибриллатион: Еффецт оф аспирин аццординг то строке мецханисм. Строке Превентион ин Атриал Фибриллатион Инвестигаторс”. Неурологy. 43 (1): 32—6. ПМИД 8423907. С2ЦИД 24134218. дои:10.1212/WНЛ.43.1_Парт_1.32.
- ^ Кантер, M. C.; Тегелер, C. Х.; Пеарце, L. А.; Wеинбергер, Ј.; Феинберг, W. M.; Андерсон, D. C.; Гомез, C. Р.; Ротхроцк, Ј. Ф.; Хелгасон, C. M.; Харт, Р. Г. (1994). „Царотид стеносис ин патиентс wитх атриал фибриллатион. Преваленце, риск фацторс, анд релатионсхип то строке ин тхе Строке Превентион ин Атриал Фибриллатион Студy”. Арцх Интерн Мед. 154 (12): 1372—7. ПМИД 8002689. дои:10.1001/арцхинте.1994.00420120100011.
- ^ Асцхенберг, W.; Сцхлüтер, M.; Кремер, П.; Сцхрöдер, Е.; Сиглоw, V.; Блеифелд, W. (1986). „Трансесопхагеал тwо-дименсионал ецхоцардиограпхy фор тхе детецтион оф лефт атриал аппендаге тхромбус”. Ј Ам Цолл Цардиол. 7 (1): 163—6. ПМИД 3941205. С2ЦИД 40967091. дои:10.1016/С0735-1097(86)80275-3.
- ^ Мüгге, А.; Кüхн, Х.; Никутта, П.; Гроте, Ј.; Лопез, Ј. А.; Даниел, W. Г. (1994). „Ассессмент оф лефт атриал аппендаге фунцтион бy биплане трансесопхагеал ецхоцардиограпхy ин патиентс wитх нонрхеуматиц атриал фибриллатион: идентифицатион оф а субгроуп оф патиентс ат инцреасед емболиц риск.”. Ј Ам Цолл Цардиол. 23 (3): 599—607. ПМИД 8113541. дои:10.1016/0735-1097(94)90743-9.
- ^ Фаткин, D.; Келлy, Р. П.; Фенелеy, M. П. (1994). „Релатионс бетwеен лефт атриал аппендаге блоод флоw велоцитy, спонтанеоус ецхоцардиограпхиц цонтраст анд тхромбоемболиц риск ин виво”. Ј АмЦолл Цардиол. 23 (4): 961—9. ПМИД 8106703. дои:10.1016/0735-1097(94)90644-0.
- ^ Даниел WГ, Неллессен У, Сцхродер Е ет ал. Лефт атриалспонтанеоус ецхо цонтраст ин митрал валве дисеасе: ан индицаторфор ан инцреасед тхромбоемболиц риск. Ј Ам Цолл Цардиол1988. . 11: 1204—11. Недостаје или је празан параметар
|титле=(помоћ). - ^ Хwанг ЈЈ, Ко ФН, Ли YХ ет ал. Цлиницал имплицатионс андфацторс релатед то лефт атриал спонтанеоус ецхо цонтраст инцхрониц нонвалвулар атриал фибриллатион. Цардиологy 1994; 85:69–75.
- ^ Поп, Г. А.; Меедер, Х. Ј.; Роеландт, Ј. Р.; Ван Оуденаарден, W.; Буленс, C.; Верwеиј, W.; Гијсберс, C.; Ван Домбург, Р.; Коудстаал, П. Ј. (1994). „Транстхорациц ецхо/Допплер ин тхе идентифицатион оф патиентс wитх цхрониц нон-валвулар атриал фибриллатион ат риск фор тхромбоемболиц евентс”. Еуропеан Хеарт Јоурнал. 15 (11): 1545—51. ПМИД 7835370. дои:10.1093/оxфордјоурналс.еурхеартј.а060428..
- ^ Ли, Y. Х.; Лаи, L. П.; Схyу, К. Г.; Хwанг, Ј. Ј.; Куан, П.; Лиен, W. П. (1994). „Цлиницал имплицатионс оф лефт атриал аппендаге флоw паттернс ин нонрхеуматиц атриал фибриллатион”. Цхест. 105 (3): 748—52. ПМИД 8131536. дои:10.1378/цхест.105.3.748..
- ^ Mitusch R, Lange V, Stierle U, Maurer B, Sheikhzadeh A.Transesophageal echocardiographic determinants of embolismin nonrheumatic atrial fibrillation. Int J Card Imaging1995. . 11: 27—34. Недостаје или је празан параметар
|title=(помоћ). - ^ Lip, G. Y. (1997). „Hypercoagulability and haemodynamic abnormalities in atrial fibrillation”. Heart. 77 (5): 395—6. PMC 484756 . PMID 9196404. doi:10.1136/hrt.77.5.395..
- ^ Al-Saady NM, Davies MJ, Luddington LA et al. Tissuefactor and von Willebrand factor expressions increased in theatrial tissue of the fibrillating atrium (Abstr). Circulation2000; 100 (Suppl I): I-285.
- ^ Asakura, H.; Hifumi, S.; Jokaji, H.; Saito, M.; Kumabashiri, I.; Uotani, C.; Morishita, E.; Yamazaki, M.; Shibata, K.; Mizuhashi, K. (1992). „Prothrombin fragment F1 + 2 and thrombin-antithrombin III complex are useful markers of the hypercoagulable state in atrial fibrillation”. Blood Coagul Fibrinolysis. 3 (4): 469—73. PMID 1420823. doi:10.1097/00001721-199203040-00015.
- ^ Asinger, R. W.; Koehler, J.; Pearce, L. A.; Zabalgoitia, M.; Blackshear, J. L.; Fenster, P. E.; Strauss, R.; Hess, D.; Pennock, G. D.; Rothbart, R. M.; Halperin, J. L. (1999). „Pathophysiologic correlates of thromboembolism in nonvalvular atrial fibrillation: II. Dense spontaneous echocardiographic contrast (The Stroke Prevention in Atrial Fibrillation SPAF-III study)”. J Am Soc Echocardiogr. 12 (12): 1088—96. PMID 10588785. doi:10.1016/S0894-7317(99)70106-9.
- ^ Blackshear, J. L.; Pearce, L. A.; Hart, R. G.; Zabalgoitia, M.; Labovitz, A.; Asinger, R. W.; Halperin, J. L. (1999). „Aortic plaque in atrial fibrillation: Prevalence, predictors, and thromboembolic implications”. Stroke. 30 (4): 834—40. PMID 10187888. S2CID 12099699. doi:10.1161/01.STR.30.4.834.
- ^ Asinger RW, Koehler J, Pearce LA et al. Pathophysiologic correlates of thromboembolism in nonvalvular atrial fibrillation, II: dense spontaneous echocardiographic contrast (The Stroke Prevention in Atrial Fibrillation BRACESPAFIIIBRACEO study). J Am Soc Echocardiogr. . 12. 1999: 1088—96. Недостаје или је празан параметар
|title=(помоћ) - ^ Collins, L. J.; Silverman, D. I.; Douglas, P. S.; Manning, W. J. (1995). „Cardioversion of nonrheumatic atrial fibrillation. Reduced thromboembolic complications with 4 weeks of precardioversion anticoagulation are related to atrial thrombus resolution”. Circulation. 92 (2): 160—3. PMID 7600646. doi:10.1161/01.CIR.92.2.160..
- ^ Blackshear, J. L.; Pearce, L. A.; Asinger, R. W.; Dittrich, H. C.; Goldman, M. E.; Zabalgoitia, M.; Rothbart, R. M.; Halperin, J. L. (1993). „Mitral regurgitation associated with reduced thromboembolic events in high-risk patients with nonrheumatic atrial fibrillation”. Am J Cardiol. 72 (11): 840—3. PMID 8213525. doi:10.1016/0002-9149(93)91079-W.
- ^ Miller, V. T.; Rothrock, J. F.; Pearce, L. A.; Feinberg, W. M.; Hart, R. G.; Anderson, D. C. (1993). „Ischemic stroke in patients with atrial fibrillation: Effect of aspirin according to stroke mechanism. Stroke Prevention in Atrial Fibrillation Investigators”. Neurology. 43 (1): 32—6. PMID 8423907. S2CID 24134218. doi:10.1212/WNL.43.1_Part_1.32..
- ^ Hart, R. G.; Pearce, L. A.; Miller, V. T.; Anderson, D. C.; Rothrock, J. F.; Albers, G. W.; Nasco, E. (2000). „Cardioembolic vs. Noncardioembolic strokes in atrial fibrillation: Frequency and effect of antithrombotic agents in the stroke prevention in atrial fibrillation studies”. Cerebrovasc Dis. 10 (1): 39—43. PMID 10629345. S2CID 25791875. doi:10.1159/000016023..
- ^ Zabalgoitia, M.; Halperin, J. L.; Pearce, L. A.; Blackshear, J. L.; Asinger, R. W.; Hart, R. G. (1998). „Transesophageal echocardiographic correlates of clinical risk of thromboembolism in nonvalvular atrial fibrillation. Stroke Prevention in Atrial Fibrillation III Investigators”. J Am Coll Cardiol. 31 (7): 1622—6. PMID 9626843. doi:10.1016/S0735-1097(98)00146-6..
- ^ Frohlich ED, Apstein C, Chobanian AV et al. The heart in hypertension [published erratum appears in N Engl J Med 1992; 327: 1768]. N Engl J Med. . 327. 1992: 998—1008. Недостаје или је празан параметар
|title=(помоћ). - ^ Schmieder, R. E.; Martus, P.; Klingbeil, A. (1996). „Reversal of left ventricular hypertrophy in essential hypertension. A meta-analysis of randomized double-blind studies”. JAMA. 275 (19): 1507—13. PMID 8622227. doi:10.1001/jama.1996.03530430051039..
- ^ Dittrich, H. C.; Pearce, L. A.; Asinger, R. W.; McBride, R.; Webel, R.; Zabalgoitia, M.; Pennock, G. D.; Safford, R. E.; Rothbart, R. M.; Halperin, J. L.; Hart, R. G. (1999). „Left atrial diameter in nonvalvular atrial fibrillation: An echocardiographic study. Stroke Prevention in Atrial Fibrillation Investigators”. Am Heart J. 137 (3): 494—9. PMID 10047632. doi:10.1016/S0002-8703(99)70498-9..
- ^ Blackshear, J. L.; Pearce, L. A.; Hart, R. G.; Zabalgoitia, M.; Labovitz, A.; Asinger, R. W.; Halperin, J. L. (1999). „Aortic plaque in atrial fibrillation: Prevalence, predictors, and thromboembolic implications”. Stroke. 30 (4): 834—40. PMID 10187888. S2CID 12099699. doi:10.1161/01.STR.30.4.834..
- ^ Hart, R. G.; Pearce, L. A.; McBride, R.; Rothbart, R. M.; Asinger, R. W. (1999). „Factors associated with ischemic stroke during aspirin therapy in atrial fibrillation: Analysis of 2012 participants in the SPAF I-III clinical trials. The Stroke Prevention in Atrial Fibrillation (SPAF) Investigators”. Stroke. 30 (6): 1223—9. PMID 10356104. S2CID 6147968. doi:10.1161/01.STR.30.6.1223..
- ^ Stroke Prevention in Atrial Fibrillation Investigators. Predictors of thromboembolism in atrial fibrillation, I: clinical features of patients at risk. „Predictors of thromboembolism in atrial fibrillation: I. Clinical features of patients at risk. The Stroke Prevention in Atrial Fibrillation Investigators”. Ann Intern Med. 116 (1): 1—5. 1992. PMID 1727091. S2CID 26916836. doi:10.7326/0003-4819-116-1-1..
- ^ Stroke Prevention in Atrial Fibrillation Investigators. Predictors of thromboembolism in atrial fibrillation, II: echo- cardiographic features of patients at risk. „Predictors of thromboembolism in atrial fibrillation: II. Echocardiographic features of patients at risk. The Stroke Prevention in Atrial Fibrillation Investigators”. Ann Intern Med. 116 (1): 6—12. 1992. PMID 1727097. S2CID 20894266. doi:10.7326/0003-4819-116-1-6..
- ^ Echocardiographic predictors of stroke in patients with atrial fibrillation: a prospective study of 1066 patients from 3 clinical trials. „Echocardiographic predictors of stroke in patients with atrial fibrillation: A prospective study of 1066 patients from 3 clinical trials”. Arch Intern Med. 158 (12): 1316—20. 1998. PMID 9645825. doi:10.1001/archinte.158.12.1316..
- ^ Yoshida, M.; Nakamura, Y.; Higashikawa, M.; Kinoshita, M. (1996). „Predictors of ischemic stroke in non-rheumatic atrial fibrillation”. Int J Cardiol. 56 (1): 61—70. PMID 8891806. doi:10.1016/0167-5273(96)02726-X..
- ^ Stöllberger, C.; Chnupa, P.; Kronik, G.; Brainin, M.; Finsterer, J.; Schneider, B.; Slany, J. (1998). „Transesophageal echocardiography to assess embolic risk in patients with atrial fibrillation. ELAT Study Group. Embolism in Left Atrial Thrombi”. Ann Intern Med. 128 (8): 630—8. PMID 9537936. S2CID 26092143. doi:10.7326/0003-4819-128-8-199804150-00004..
- ^ Tsai, L. M.; Lin, L. J.; Teng, J. K.; Chen, J. H. (1997). „Prevalence and clinical significance of left atrial thrombus in nonrheumatic atrial fibrillation”. Int J Cardiol. 58 (2): 163—9. PMID 9049681. doi:10.1016/S0167-5273(96)02862-8..
Literatura
уреди- Fuster, V.; Rydén, L. E.; Asinger, R. W.; Cannom, D. S.; Crijns, H. J.; Frye, R. L.; Halperin, J. L.; Kay, G. N.; Klein, W. W.; Lévy, S.; McNamara, R. L.; Prystowsky, E. N.; Wann, L. S.; Wyse, D. G.; American College of Cardiology; American Heart Association; European Society of Cardiology; North American Society of Pacing and Electrophysiology (2001). „Guidelines for the management of patients with atrial fibrillation. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines and Policy Conferences (Committee to develop guidelines for the management of patients with atrial fibrillation) developed in collaboration with the North American Society of Pacing and Electrophysiology”. European Heart Journal. 22 (20): 1852—1923. PMID 11601835. doi:10.1053/euhj.2001.2983.
Spoljašnje veze
уреди| Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |