Tromboembolizam u pretkomorskoj fibrilaciji
Tromboembolizam u pretkomorskoj fibrilaciji pripisuje se emboliji trombom koji potiče iz leve srčane pretkomore. Pretkomorska fibrilacija najčešća je aritmija u kliničkoj praksi, odgovorna za oko trećinu hospitalizacija zbog poremečaja srčanog ritma. Patogeneza tromboembolizma kao uzroka pretkomorske fibrilacijije jako je složena i biće delimično objašnjena na ovoj stranici.[1]
| Tromboembolizam u pretkomorskoj fibrilaciji | |
|---|---|
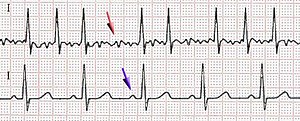 | |
| EKG bolesnika sa AF na kome je crvenom strelicom označeno mesto gde se umesto postojanih R-talasa, na snimku beleže brze oscilacije ili fibrilatorni talasi (gore) i fiziološki EKG sa normalnim izgledom R-talasa (dole) | |
| Klasifikacija i spoljašnji resursi | |
| MKB-10 | I48 |
| MKB-9-CM | 427.31 |
| DiseasesDB | 1065 |
| MedlinePlus | 000184 |
| eMedicine | med/184 emerg/46 |
| MeSH | D001281 |
Osnovni pojmovi уреди
- Pretkomorska fibrilacija
Pretkomorska fibrilacija ili atrijalna fibrilacija je tahiaritmija pretkomora koju odlikuje neusklađeena depolarizacija pretkomora, što ima za posledicu poremećaj mehaniåke funkcije pretkomora. Elektrokardiografski se, tokom pretkomorske fibrilacije, umesto postojanih P-talasa, beleže brze oscilacije ili fibrilatorni talasi koji variraju u veličini, obliku i vremenu pojavljivanja.
- Tromboembolizam
Blokada krvnih sudova izazvana ugruškom krvi, koji se odvojio od svog prvobitnog mesta formiranja.
Epidemiologija уреди
Do 25% moždanih udara kod bolesnika sa pretkomorskom fibrilacijom može nastati usled osnovne cerebrovaskularne bolesti, drugih srčanih izvora embolizma ili ateromatoze luka aorte.[2][3]
Učestalost moždanog udara kod bolesnika sa pretkomorskom fibrilacijom uvećava se sa staroću stanovništva na čak 36% kod bolesnika starijih od 80 do 89 godina. Polovina starijih bolesnika sa pretkomorskom ima hroničnu arterijsku hipertenziju (koja je osnovni faktor rizika za cerebrovaskularnu bolest), a približno 12% ima klinički skrivenu stenozu karotidne arterije.[4]
Ateroskleroza karotidnih arterija nema znatno veću prevalenciju kod bolesnika sa pretkomorskom fibrilacijom i moždanim udarom, u poređenju sa bolesnicima sa moždanim udarom bez pretkomorske fibrilacije, i relativno je manje značajan faktor.
Patofiziologija nastanka tromba уреди
Formiranje tromba u levoj pretkomori počinje Virhovljevom trijadom koju čine; zastoj (staza), endotelna disfunkcija i hiperkoagulabilno stanje. Hemodinamski i hemostatski mehanizmi odgovorni za kliničke tromboembolijske događeje u pretkomorskoj fibrilaciji delimično su razjašnjeni ispitivanjem poremećaja koagulacije krvi kod ovih bolesnika.
Tromb, koji je neposredno povezan sa pretkomorskom fibrilacijom, najčešće se stvara u aurikuli leve pretkomore, koja se ne može u potpunosti prikazati transtorakalnim ehokardiogramom.[5] Transezofagealna Dopler ehokardiografija je senzitivan i specifična metod za procenu funkcije aurikule leve pretkomore i za otkrivanje trombotičkog materijala. Trombi se češće sreću kod bolesnika sa pretkomorskom fibrilacijom i ishemijskim moždanim udarom nego kod onih bez moždanog udara.[6]
- Zastoj u cirkulaciji
Serijska transezofagealna ispitivanja leve pretkomore i njene aurikule, tokom konverzije pretkomorske fibrilacije u sinusni ritam, pokazala su smanjenje brzine protoka u levoj aurikuli usled gubitka organizovane mehaničke kontrakcije u pretkomorskoj fibrilaciji.
Smanjenje brzine protoka u levoj pretkomori i njenoj aurikuli udruženo je sa pojavom spontanog ehokontrasta, sa stvaranjem tromba i embolijskim događajima. Brzina protoka u levoj aurikuli je manja kod bolesnika sa pretkomorskim flaterom u poređenju sa brzinom protoka kod normalnog sinusnog ritma, ali je veća nego pri pretkomorskoj fibrilaciji. Nepozanica je da li je zbog toga prevalenca tromba u levoj aurikuli i stopa tromboembolijskih događaja nešto niže kod pretkomorskog flatera. Iako se opšteprihvaćeni terapijski pristup zasniva na pretpostavci da nastanak tromba zahteva neprekidno trajanje pretkomorske fibrilacije, oko 48 sati, transezofagealnim ehokardiogramom su otkriveni trombi i u kraćem vremenskom periodu.[7][8][9][10][11][12]
- Endotelna disfunkcija
Teško je dokazati da je poremećaj funkcije endotela zaseban mehanizam, odgovoran za nastanak tromba kod bolesnika sa pretkomorskom fibrilacijom, iako je koncentracija von Willebrandovog faktora u serumu i pretkomorskom tkivu povećana kod nekih bolesnika. Slično tome, pretkomorska fibrilacija je udružena i sa biohemijskim markerima koagulacije i aktivacije trombocita, koji možda odražvaju sistemsko hiperkoagulabilno stanje.[13][14]
- Hiperkoagulabilno stanje
Perzistentna i paroksizmalna pretkomorska fibrilacija udružene su sa povećenjem serumskih koncentracija fibrinogena i fibrinskog D-dimera, koji ukazuju na aktivnu intravaskularnu trombogenezu. Povećanje koncentracije tromboglobulina i trombocitnog faktora IV, kod odabranih bolesnika sa pretkomorskom fibrilacijom, ukazuju na aktivaciju trombocita, ali su ovi podaci manje pouzdani, u skladu sa manjom efikasnošću antitrombocitne terapije u prevenciji tromboembolijskih komplikacija, ãto je dokazano u kliničkim studijama.[15] Ovi biohemijski markeri koagulacije i aktivacije trombocita ne omogućavaju razlikovanje sekundarnog reaktivnog procesa usled intravaskularnog zgrušavanja od primarnog hiperkoagulabilnog stanja. Neki od ovih markera koagulacije normalizuju se tokom antikoagulantne terapije, a neki se povećavaju neposredno nakon konverzije u sinusni ritam i zatim vraćaju na normalu.
Kod bolesnika sa reumatskom mitralnom stenozom, koji su bili podvrgnuti transseptalnoj kateterizaciji radi mitralne balon-valvuloplastike, dokazan je regionalni oblik koagulopatije u levoj pretkomori. Koncentracije fibrinopeptida A, kompleksa trombin-antitrombin III, i protrombinskog fragmenta F1,2, bile su povećane u levoj pretkomori u odnosu na koncentracije ovih markera u desnoj pretkomori i butnoj veni, što ukazuje na regionalnu aktivaciju kaskadnih reakcija koagulacije.
Još uvek nije utvrođeno da li je ova pojava u pretkomorskoj fibrilaciji hemodinamski posredovana visokim pritiskom u levoj pretkomori, ili su odgovorni neki drugi mehanizmi, ali je dokazano da je regionalna koagulopatija udružena sa nalazom spontanog eho kontrasta u levoj pretkomori.
Suprotno tome, insuficijencija mitralnog zalistka valvule umanjuje stazu u levoj aurikuli i udružena je sa nižim stepenom aktivacije koagulacij. Spontani eho kontrast je složen fenomen koji in vitro zavisi od brzine krvnog protoka, hematokrita i serumskih proteina, uključujući fibrinogen.
Kod bolesnika sa pretkomorskom fibrilacijom, nezavisni predskazatelji pojave spontanog eho kontrasta jesu:
- veličina leve pretkomore,
- brzina protoka u levoj aurikuli,
- disfunkcija leve komore,
- koncentracija fibrinogena,
- hematokrit i
- ateroskleroza aorte.[16][17]
Ovaj hemoreološki fenomen predstavlja ehokardiografski odraz regionalne koagulopatije i ima klinički značaj pri otkrivanju bolesnika sa pretkomorskom fibrilacijom koji su pod visokim rizikom od tromboembolijskih komplikacija.[18] Međutim još uvek nije utvrđeena prednost ovog nalaza u odnosu na uobičajenu kliničku procenu pri prospektivnoj stratifikaciji rizika od tromboembolije.
Nasuprot rasprostranjenom shvatanju da sistemska antikoagulantna terapija tokom četiri nedelje dovodi do endokardijalne adherencije i organizacije tromba u levoj aurikuli, transezofagealna proučavanja su potvrdila nestanak tromba kod većine bolesnika.[19]
Gotovo ista zapažanja ukazala su na dinamičnu prirodu poremećaja funkcije leve pretkomore i njene aurikule tokom konverzije pretkomorske fibrilacije, što logično uzrokuje potrebu za antikoagulantnom terapijom, nekoliko nedelja pre i posle uspešne kardioverzije.
Suprotno tome, povećan protok u levoj pretkomori kod bolesnika sa mitralnom regurgitacijom udružen je sa manjom prevalencijom spontanog eho kontrasta u levoj pretkomori i manjom učestalošću tromboembolijskih dogđaja, čak i kada je leva pretkomora uvećana.[20]
Kliničke posledice уреди
Kako pouzdana patofiziologija tromboembolizma kod bolesnika sa pretkomorskom fibrilacijom nije sa sigurnošću utvrđena, mehanizmi koji povezuju faktore rizika sa ishemijskim moždanim udarom u pretkomorskoj fibrilaciji, takođe, nisu potpuno razjašnjeni.
Čvrsta povezanost između hipertenzije i moždanog udara kod pretkomorske fibrilacije verovatno je posredovana pre svega embolijom koja potiče iz leve srčane aurikule,[21] ali hipertenzija takođe povećava rizik od neembolijskih mždanih udara u pretkomorskoj fibrilaciji.[22] Hipertenzija kod ovih bolesnika povezana je sa smanjenom brzinom protoka u levoj aurikuli, pojavom spontanog eho kontrasta, i nastankom tromba.[23] Uticaj hipertenzije na hemodinamiku leve pretkomore može biti posledica poremećene dijastolne komorske funkcije, ali ovaka povezanost je još uvek je u razmatranju jer je na nivou pretpostavke.[24] Osnovno pitanje je da li dugotrajno lečenje hipertenzije smanjuje rizik od embolijskih moždanih udara pri pretkomorskoj fibrilaciji, zato što su komorske dijastolne abnormalnosti koje prate hipertenziju kod starih osoba često multifaktorijalne i teško su reverzibilne.[25]
Odmaklo životno doba ima višestruki uticaj na povećanje rizika od moždanog udara. Kod bolesnika sa pretkomorskom fibrilacijom, proces starenja je udružen sa pojavom fenomena koji predisponiraju stvaranju tromba,[26] kao što su uvećanje leve pretkomore, smanjenje brzine protoka u levoj aurikuli i pojava spontanog eho kontrasta. Pored toga, starije životno doba je faktor rizika za aterosklerozu, sa nastankom složenih aterosklerotskih plakova na luku aorte, a udruženo je i sa moždanim udarom nezavisno od pretkomorske fibrilacije.[27]
Koncentracija protrombinskog aktivacijskog fragmenta F1.2, pokazatelja stvaranja trombina, povećava se sa životnim dobom u opštoj populaciji[160–162], kao i kod bolesnika sa pretkomorskom fibrilacijom,[28] što ukazuje na protrombinsku dijatezu u starijem životnom dobu.
Poremećaj funkcije leve komore, na koji ukazuju anamnestički podaci o srčanom popuštanju ili transtorakalniehokardiografski pregled, povećava rizik od ishemijskogmoždanog udara kod bolesnika sa atrijalnom fibrilacijom,a koji ne uzimaju antitrombotsku terapiju,[29] ali ne ikod bolesnika sa pretkomorskom fibrilacijom i umerenimrizikom, koji uzimaju aspirin.[30][31][32][33] Izvedeni zaključci sukontradiktorni; disfunkcija leve komore je udružena i sanastankom tromba u levoj pretkomori i sa neembolijskimmoždanim udarima kod bolesnika sa pretkomorskom fibrilacijom.[34]
Ukratko rečeno, tokom pretkomorske fibrilacije deluju složeni tromboembolijski mehanizmi, koji uključuju međudejstvo faktora koji se odnose na stazu krvi u levoj pretkomori i levoj aurikuli, poremećaj funkcije endotela i sistemsku, a moguće je i lokalnu, hiperkoagulabilnost.
Izvori уреди
- ^ Halperin, J. L.; Hart, R. G. (1988). „Atrial fibrillation and stroke: New ideas, persisting dilemmas”. Stroke. 19 (8): 937—41. PMID 3041652. S2CID 14213519. doi:10.1161/01.STR.19.8.937.
- ^ Bogousslavsky, J.; Van Melle, G.; Regli, F.; Kappenberger, L. (1990). „Pathogenesis of anterior circulation stroke in patients with nonvalvular atrial fibrillation: The Lausanne Stroke Registry”. Neurology. 40 (7): 1046—50. PMID 2356005. S2CID 9953973. doi:10.1212/WNL.40.7.1046.
- ^ Miller, V. T.; Rothrock, J. F.; Pearce, L. A.; Feinberg, W. M.; Hart, R. G.; Anderson, D. C. (1993). „Ischemic stroke in patients with atrial fibrillation: Effect of aspirin according to stroke mechanism. Stroke Prevention in Atrial Fibrillation Investigators”. Neurology. 43 (1): 32—6. PMID 8423907. S2CID 24134218. doi:10.1212/WNL.43.1_Part_1.32.
- ^ Kanter, M. C.; Tegeler, C. H.; Pearce, L. A.; Weinberger, J.; Feinberg, W. M.; Anderson, D. C.; Gomez, C. R.; Rothrock, J. F.; Helgason, C. M.; Hart, R. G. (1994). „Carotid stenosis in patients with atrial fibrillation. Prevalence, risk factors, and relationship to stroke in the Stroke Prevention in Atrial Fibrillation Study”. Arch Intern Med. 154 (12): 1372—7. PMID 8002689. doi:10.1001/archinte.1994.00420120100011.
- ^ Aschenberg, W.; Schlüter, M.; Kremer, P.; Schröder, E.; Siglow, V.; Bleifeld, W. (1986). „Transesophageal two-dimensional echocardiography for the detection of left atrial appendage thrombus”. J Am Coll Cardiol. 7 (1): 163—6. PMID 3941205. S2CID 40967091. doi:10.1016/S0735-1097(86)80275-3.
- ^ Mügge, A.; Kühn, H.; Nikutta, P.; Grote, J.; Lopez, J. A.; Daniel, W. G. (1994). „Assessment of left atrial appendage function by biplane transesophageal echocardiography in patients with nonrheumatic atrial fibrillation: identification of a subgroup of patients at increased embolic risk.”. J Am Coll Cardiol. 23 (3): 599—607. PMID 8113541. doi:10.1016/0735-1097(94)90743-9.
- ^ Fatkin, D.; Kelly, R. P.; Feneley, M. P. (1994). „Relations between left atrial appendage blood flow velocity, spontaneous echocardiographic contrast and thromboembolic risk in vivo”. J AmColl Cardiol. 23 (4): 961—9. PMID 8106703. doi:10.1016/0735-1097(94)90644-0.
- ^ Daniel WG, Nellessen U, Schroder E et al. Left atrialspontaneous echo contrast in mitral valve disease: an indicatorfor an increased thromboembolic risk. J Am Coll Cardiol1988. . 11: 1204—11. Недостаје или је празан параметар
|title=(помоћ). - ^ Hwang JJ, Ko FN, Li YH et al. Clinical implications andfactors related to left atrial spontaneous echo contrast inchronic nonvalvular atrial fibrillation. Cardiology 1994; 85:69–75.
- ^ Pop, G. A.; Meeder, H. J.; Roelandt, J. R.; Van Oudenaarden, W.; Bulens, C.; Verweij, W.; Gijsbers, C.; Van Domburg, R.; Koudstaal, P. J. (1994). „Transthoracic echo/Doppler in the identification of patients with chronic non-valvular atrial fibrillation at risk for thromboembolic events”. European Heart Journal. 15 (11): 1545—51. PMID 7835370. doi:10.1093/oxfordjournals.eurheartj.a060428..
- ^ Li, Y. H.; Lai, L. P.; Shyu, K. G.; Hwang, J. J.; Kuan, P.; Lien, W. P. (1994). „Clinical implications of left atrial appendage flow patterns in nonrheumatic atrial fibrillation”. Chest. 105 (3): 748—52. PMID 8131536. doi:10.1378/chest.105.3.748..
- ^ Mitusch R, Lange V, Stierle U, Maurer B, Sheikhzadeh A.Transesophageal echocardiographic determinants of embolismin nonrheumatic atrial fibrillation. Int J Card Imaging1995. . 11: 27—34. Недостаје или је празан параметар
|title=(помоћ). - ^ Lip, G. Y. (1997). „Hypercoagulability and haemodynamic abnormalities in atrial fibrillation”. Heart. 77 (5): 395—6. PMC 484756 . PMID 9196404. doi:10.1136/hrt.77.5.395..
- ^ Al-Saady NM, Davies MJ, Luddington LA et al. Tissuefactor and von Willebrand factor expressions increased in theatrial tissue of the fibrillating atrium (Abstr). Circulation2000; 100 (Suppl I): I-285.
- ^ Asakura, H.; Hifumi, S.; Jokaji, H.; Saito, M.; Kumabashiri, I.; Uotani, C.; Morishita, E.; Yamazaki, M.; Shibata, K.; Mizuhashi, K. (1992). „Prothrombin fragment F1 + 2 and thrombin-antithrombin III complex are useful markers of the hypercoagulable state in atrial fibrillation”. Blood Coagul Fibrinolysis. 3 (4): 469—73. PMID 1420823. doi:10.1097/00001721-199203040-00015.
- ^ Asinger, R. W.; Koehler, J.; Pearce, L. A.; Zabalgoitia, M.; Blackshear, J. L.; Fenster, P. E.; Strauss, R.; Hess, D.; Pennock, G. D.; Rothbart, R. M.; Halperin, J. L. (1999). „Pathophysiologic correlates of thromboembolism in nonvalvular atrial fibrillation: II. Dense spontaneous echocardiographic contrast (The Stroke Prevention in Atrial Fibrillation SPAF-III study)”. J Am Soc Echocardiogr. 12 (12): 1088—96. PMID 10588785. doi:10.1016/S0894-7317(99)70106-9.
- ^ Blackshear, J. L.; Pearce, L. A.; Hart, R. G.; Zabalgoitia, M.; Labovitz, A.; Asinger, R. W.; Halperin, J. L. (1999). „Aortic plaque in atrial fibrillation: Prevalence, predictors, and thromboembolic implications”. Stroke. 30 (4): 834—40. PMID 10187888. S2CID 12099699. doi:10.1161/01.STR.30.4.834.
- ^ Asinger RW, Koehler J, Pearce LA et al. Pathophysiologic correlates of thromboembolism in nonvalvular atrial fibrillation, II: dense spontaneous echocardiographic contrast (The Stroke Prevention in Atrial Fibrillation BRACESPAFIIIBRACEO study). J Am Soc Echocardiogr. . 12. 1999: 1088—96. Недостаје или је празан параметар
|title=(помоћ) - ^ Collins, L. J.; Silverman, D. I.; Douglas, P. S.; Manning, W. J. (1995). „Cardioversion of nonrheumatic atrial fibrillation. Reduced thromboembolic complications with 4 weeks of precardioversion anticoagulation are related to atrial thrombus resolution”. Circulation. 92 (2): 160—3. PMID 7600646. doi:10.1161/01.CIR.92.2.160..
- ^ Blackshear, J. L.; Pearce, L. A.; Asinger, R. W.; Dittrich, H. C.; Goldman, M. E.; Zabalgoitia, M.; Rothbart, R. M.; Halperin, J. L. (1993). „Mitral regurgitation associated with reduced thromboembolic events in high-risk patients with nonrheumatic atrial fibrillation”. Am J Cardiol. 72 (11): 840—3. PMID 8213525. doi:10.1016/0002-9149(93)91079-W.
- ^ Miller, V. T.; Rothrock, J. F.; Pearce, L. A.; Feinberg, W. M.; Hart, R. G.; Anderson, D. C. (1993). „Ischemic stroke in patients with atrial fibrillation: Effect of aspirin according to stroke mechanism. Stroke Prevention in Atrial Fibrillation Investigators”. Neurology. 43 (1): 32—6. PMID 8423907. S2CID 24134218. doi:10.1212/WNL.43.1_Part_1.32..
- ^ Hart, R. G.; Pearce, L. A.; Miller, V. T.; Anderson, D. C.; Rothrock, J. F.; Albers, G. W.; Nasco, E. (2000). „Cardioembolic vs. Noncardioembolic strokes in atrial fibrillation: Frequency and effect of antithrombotic agents in the stroke prevention in atrial fibrillation studies”. Cerebrovasc Dis. 10 (1): 39—43. PMID 10629345. S2CID 25791875. doi:10.1159/000016023..
- ^ Zabalgoitia, M.; Halperin, J. L.; Pearce, L. A.; Blackshear, J. L.; Asinger, R. W.; Hart, R. G. (1998). „Transesophageal echocardiographic correlates of clinical risk of thromboembolism in nonvalvular atrial fibrillation. Stroke Prevention in Atrial Fibrillation III Investigators”. J Am Coll Cardiol. 31 (7): 1622—6. PMID 9626843. doi:10.1016/S0735-1097(98)00146-6..
- ^ Frohlich ED, Apstein C, Chobanian AV et al. The heart in hypertension [published erratum appears in N Engl J Med 1992; 327: 1768]. N Engl J Med. . 327. 1992: 998—1008. Недостаје или је празан параметар
|title=(помоћ). - ^ Schmieder, R. E.; Martus, P.; Klingbeil, A. (1996). „Reversal of left ventricular hypertrophy in essential hypertension. A meta-analysis of randomized double-blind studies”. JAMA. 275 (19): 1507—13. PMID 8622227. doi:10.1001/jama.1996.03530430051039..
- ^ Dittrich, H. C.; Pearce, L. A.; Asinger, R. W.; McBride, R.; Webel, R.; Zabalgoitia, M.; Pennock, G. D.; Safford, R. E.; Rothbart, R. M.; Halperin, J. L.; Hart, R. G. (1999). „Left atrial diameter in nonvalvular atrial fibrillation: An echocardiographic study. Stroke Prevention in Atrial Fibrillation Investigators”. Am Heart J. 137 (3): 494—9. PMID 10047632. doi:10.1016/S0002-8703(99)70498-9..
- ^ Blackshear, J. L.; Pearce, L. A.; Hart, R. G.; Zabalgoitia, M.; Labovitz, A.; Asinger, R. W.; Halperin, J. L. (1999). „Aortic plaque in atrial fibrillation: Prevalence, predictors, and thromboembolic implications”. Stroke. 30 (4): 834—40. PMID 10187888. S2CID 12099699. doi:10.1161/01.STR.30.4.834..
- ^ Hart, R. G.; Pearce, L. A.; McBride, R.; Rothbart, R. M.; Asinger, R. W. (1999). „Factors associated with ischemic stroke during aspirin therapy in atrial fibrillation: Analysis of 2012 participants in the SPAF I-III clinical trials. The Stroke Prevention in Atrial Fibrillation (SPAF) Investigators”. Stroke. 30 (6): 1223—9. PMID 10356104. S2CID 6147968. doi:10.1161/01.STR.30.6.1223..
- ^ Stroke Prevention in Atrial Fibrillation Investigators. Predictors of thromboembolism in atrial fibrillation, I: clinical features of patients at risk. „Predictors of thromboembolism in atrial fibrillation: I. Clinical features of patients at risk. The Stroke Prevention in Atrial Fibrillation Investigators”. Ann Intern Med. 116 (1): 1—5. 1992. PMID 1727091. S2CID 26916836. doi:10.7326/0003-4819-116-1-1..
- ^ Stroke Prevention in Atrial Fibrillation Investigators. Predictors of thromboembolism in atrial fibrillation, II: echo- cardiographic features of patients at risk. „Predictors of thromboembolism in atrial fibrillation: II. Echocardiographic features of patients at risk. The Stroke Prevention in Atrial Fibrillation Investigators”. Ann Intern Med. 116 (1): 6—12. 1992. PMID 1727097. S2CID 20894266. doi:10.7326/0003-4819-116-1-6..
- ^ Echocardiographic predictors of stroke in patients with atrial fibrillation: a prospective study of 1066 patients from 3 clinical trials. „Echocardiographic predictors of stroke in patients with atrial fibrillation: A prospective study of 1066 patients from 3 clinical trials”. Arch Intern Med. 158 (12): 1316—20. 1998. PMID 9645825. doi:10.1001/archinte.158.12.1316..
- ^ Yoshida, M.; Nakamura, Y.; Higashikawa, M.; Kinoshita, M. (1996). „Predictors of ischemic stroke in non-rheumatic atrial fibrillation”. Int J Cardiol. 56 (1): 61—70. PMID 8891806. doi:10.1016/0167-5273(96)02726-X..
- ^ Stöllberger, C.; Chnupa, P.; Kronik, G.; Brainin, M.; Finsterer, J.; Schneider, B.; Slany, J. (1998). „Transesophageal echocardiography to assess embolic risk in patients with atrial fibrillation. ELAT Study Group. Embolism in Left Atrial Thrombi”. Ann Intern Med. 128 (8): 630—8. PMID 9537936. S2CID 26092143. doi:10.7326/0003-4819-128-8-199804150-00004..
- ^ Tsai, L. M.; Lin, L. J.; Teng, J. K.; Chen, J. H. (1997). „Prevalence and clinical significance of left atrial thrombus in nonrheumatic atrial fibrillation”. Int J Cardiol. 58 (2): 163—9. PMID 9049681. doi:10.1016/S0167-5273(96)02862-8..
Literatura уреди
- Fuster, V.; Rydén, L. E.; Asinger, R. W.; Cannom, D. S.; Crijns, H. J.; Frye, R. L.; Halperin, J. L.; Kay, G. N.; Klein, W. W.; Lévy, S.; McNamara, R. L.; Prystowsky, E. N.; Wann, L. S.; Wyse, D. G.; American College of Cardiology; American Heart Association; European Society of Cardiology; North American Society of Pacing and Electrophysiology (2001). „Guidelines for the management of patients with atrial fibrillation. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines and Policy Conferences (Committee to develop guidelines for the management of patients with atrial fibrillation) developed in collaboration with the North American Society of Pacing and Electrophysiology”. European Heart Journal. 22 (20): 1852—1923. PMID 11601835. doi:10.1053/euhj.2001.2983.
Spoljašnje veze уреди
| Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |