Akcioni potencijal
U fiziologiji, akcioni potencijal (AP) nastaje kada membranski potencijal određene ćelijske lokacije brzo raste i opada.[1] Ova depolarizacija zatim uzrokuje depolarizaciju susednih lokacija. Akcioni potencijali se javljaju u nekoliko tipova životinjskih ćelija, zvanih ekscitabilne ćelije, koje uključuju neurone, mišićne ćelije, endokrine ćelije i u nekim biljnim ćelijama.
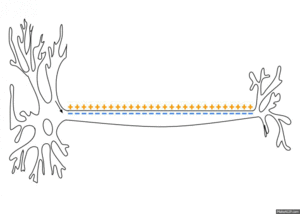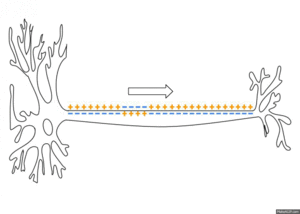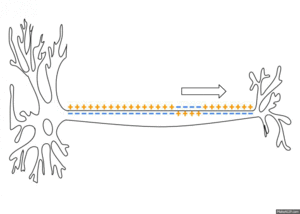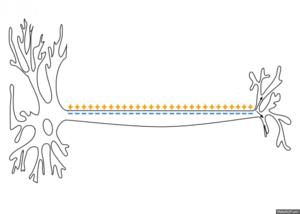
Ovo stvara promenu polarizacionog odnosa između ekstracelularnog i unutarćelijskog medija.
Impuls putuje niz akson samo u jednom smeru, do aksonskog terminala, gde prenosi signal drugim neuronima.
U neuronima, akcioni potencijali igraju centralnu ulogu u komunikaciji od ćelije do ćelije tako što obezbeđuju – ili u pogledu skokovitog prostiranja, pomažu – propagaciju signala duž aksona neurona ka sinaptičkim proširenjima koji se nalaze na krajevima aksona; ovi signali se zatim mogu povezati sa drugim neuronima u sinapsama, ili sa motornim ćelijama ili žlezdama. U drugim vrstama ćelija, njihova glavna funkcija je aktiviranje intracelularnih procesa. U mišićnim ćelijama, na primer, akcioni potencijal je prvi korak u lancu događaja koji dovode do kontrakcije. U beta ćelijama pankreasa, one izazivaju oslobađanje insulina. Akcioni potencijali u neuronima su takođe poznati kao „nervni impulsi“ ili „šiljci“, a vremenska sekvenca akcionih potencijala koju generiše neuron naziva se njegovim „šiljastim vozom“. Za neuron koji emituje akcioni potencijal, ili nervni impuls, često se kaže da se "pali".
Akcioni potencijali se generišu specijalnim tipovima jonskih kanala regulisanih naponom ugrađenih u ćelijsku membranu. Ovi kanali se zatvaraju kada je membranski potencijal blizu (negativnog) potencijala mirovanja ćelije, ali brzo počinju da se otvaraju ako se otvaraju ako membranski potencijal počne da se povećava do tačno definisanog graničnog napona, depolarizujući transmembranski potencijal. Kada se kanali otvore, dozvoljavaju unutrašnji tok natrijumovih jona, što menja elektrohemijski gradijent, što zauzvrat proizvodi dalji porast membranskog potencijala, prema nuli. Ovo onda uzrokuje otvaranje više kanala, proizvodeći veću električnu struju kroz ćelijsku membranu i tako dalje. Proces se odvija eksplozivno dok se svi dostupni jonski kanali ne otvore, što rezultira velikim porastom membranskog potencijala. Brzi priliv natrijumovih jona uzrokuje da se polaritet plazma membrane preokrene, a jonski kanali se zatim brzo inaktiviraju. Kako se natrijumovi kanali zatvaraju, joni natrijuma više ne mogu da uđu u neuron, i oni se zatim aktivno transportuju nazad iz plazma membrane. Zatim se aktiviraju kalijumovi kanali i dolazi do spoljašnje struje kalijumovih jona, vraćajući elektrohemijski gradijent u stanje mirovanja. Nakon što se pojavi akcioni potencijal, dolazi do prolaznog negativnog pomeranja, nazvanog naknadna hiperpolarizacija.
U životinjskim ćelijama postoje dva primarna tipa akcionih potencijala. Jedan tip se generiše naponskim natrijumskim kanalima, a drugi naponskim kalcijumskim kanalima. Akcioni potencijali zasnovani na natrijumu obično traju manje od jedne milisekunde, ali akcioni potencijali zasnovani na kalcijumu mogu trajati 100 milisekundi ili duže. Kod nekih tipova neurona, spori skokovi kalcijuma obezbeđuju pokretačku snagu za dugi nalet brzo emitovanih natrijumovih šiljaka. U ćelijama srčanog mišića, s druge strane, početni brzi skok natrijuma obezbeđuje "prajmer" da izazove brzi početak skoka kalcijuma, koji zatim proizvodi mišićnu kontrakciju.[2]
Struktura neurona uredi
Neuroni se sastoje od:
- tela (soma) ili perikariona (od gr. peri = oko; karyon = jedro) sa koga polaze
- dve vrste nastavaka (neurita):
Dendriti su kratki, razgranati nastavci koji nadražaj dovode do tela neurona. Broj dendrita može biti manji ili veći ili mogu i potpuno da odsustvuju. Oni se dalje mogu granati i na ograncima se uočavaju bojni dendritski trnići. Dendriti su kratki i razgranati protoplazmatični nastavci koji se pružaju oko ćelijskog tela. Grane dendrita, prema blizini u odnosu na ćelijsko telo, mogu biti primarne, sekundarne i tercijalne. Područje koje pokrivaju svi ogranci jednog dendrita naziva se dendritska zona. Dendriti su po pravilu tanji od aksona, a njihov prečnik se smanjuje idući prema terminalnim grananjima. Kod mnogih neurona, na površini najsitnijih dendritskih grana nalaze se ispupčenja pečurkastog oblika, trnoliki izraštaji, koji su prekriveni brojnim sinaptičkim završecima drugih ćelija. Stoga, dendriti sa trnolikim izraštajima predstavljaju glavni prijemni region nervne ćelije. Trnoliki izraštaji oduvek su fascinirali neurobiologe, od kada ih je, 1888. godine, prvi put opisao Ramon Kahal. Danas je poznato da broj dendritskih grana i trnolikih izraštaja zavise od kvaliteta sredine u kojoj se čovek razvija, kako u detinjstvu, tako i tokom života.
Akson (grč. axon=osovina) ili neurit (nervno vlakno) je neparan nastavak koji se samo na kraju grana. Akson nadražaj odvodi od tela neurona ka sledećem neuronu. Nervne ćelije po pravilu poseduju jedno nervno vlakno ili akson. Izuzetak predstavljaju amakrine ćelije mrežnjače, koje pored brojnih dendrita nemaju ni jedan akson, kao i pseudounipolarni neuroni, koji poseduju jedan akson koji se na samom početku grana na dva ogranka. Dužina aksona kod različitih tipova neurona, varira od manje od milimetra do preko jednog metra, a prečnik aksona od 0.3 μm do oko 25 μm kod čoveka.
Sam početak aksona, mesto gde akson započinje pružajući se od ćelijskog tela, nešto je deblji od ostatka aksona i naziva se aksonski brežuljak. Kod većine aksona, aksonski brežuljak ima ulogu zone u kojoj nastaju akcioni potencijali, pa se naziva i inicijalni segment aksona (izuztetak od ovog pravila predstavljaju pomenuti pseudounipolarni neuroni, koji imaju ulogu senzitivnih neurona). Na samom kraju, nervno vlakno se grana na veći broj protoplazmatičnih končića sa zadebljalim krajevima. To su sinaptička proširenja. Akson, između aksonskog brežuljka i sinaptičkog proširenja ima konstantan dijametar, što je važna odlika aksona, od značaja za njegova električna i nadražljiva svojstva. Taj deo aksona naziva se pravi akson (axon proper). Sinaptičko proširenje nervnog vlakna je glavni predajni deo nervne ćelije, jer tim delom nerva ćelija ostvaruje kontakt sa drugom ćelijom. U sinaptičkom proširenju nalaze se sinaptičke vezikule sa neurotransmiterom, koji posreduje u komunikaciji nervne ćelije sa drugim ćelijama.
Sa svim delovima nervne ćelije, dakle telom, dendritima i aksonom uspostavljaju vezu mnogobrojni kako neuroni tako i nastavci glijalnih ćelija pa se svi ti nastavci zajedno nazivaju neuropila (od gr. pilos= svaljana vuna, filc).
Faze akcionog potencijala uredi
Mirovni membranski potencijal nervnih vlakana iznosi oko -90 mV, što znači da je potencijal u citosolu 90 milivolti negativniji u odnosu na potencijal ekstracelularne tečnosti. Akcioni potencijal predstavlja brzu promenu mirovnog membranskog potencijala koja se brzo širi duž nervnog vlakna. Mirovni membranski potencijal označava se kao prvi stadijum nastanka akcionog potencijala, tzv. stadijum mirovanja. Njega sledi stadijum depolarizacije. Tada membrana iznenada postane vrlo propustljiva za natrijumove jone, dozvoljavajući tok ogromnog broja pozitivno naelektrisanih Na+ jona u unutrašnjost ćelije. To izaziva rast MMP od uobičajenih -90 mV prema prema pozitivnom smeru. Kod debelih nervnih vlakana, ogromna količina Na+ jona dovodi do prebacivanja MMP preko nultog nivoa u nešto malo pozitivnu vrednost, dok se potencijal u tanjim vlaknima i mnogobrojnim neuronima CNS samo približava nultom nivou, ali ga ne prelazi. Tokom nekoliko 10.000-tih delova sekunde pošto je membrana postala visokopermeabilna za Na+ jone, natrijumski kanali počinju da se zatvaraju, dok se kalijumski otvaraju više nego normalno. Brza difuzija K+ iz citosola u ekstracelularnu sredinu uspostavlja normalan mirovni membranski potencijal, što se naziva stadijum repolarizacije. Jasno je, dakle, da u nastajanju i nestajanju akcionih potencijala nervnih vlakana ključnu ulogu imaju voltažno-zavisni natrijumski kanali i voltažno-zavisni kalijumski kanali. Akcioni potencijal nastaje mehanizmom pozitivne povratne sprege circulus vitiosusa: rastuća voltaža uzrokuje otvaranje voltažno-zavisnih natrijumskih kanala. To omogućava brzu difuziju ogromne količine Na+ u ćeliju, što dodatno povećava vrednost MMP, otvarajući tako još voltažno zavisnih natrijumskih kanala i još veću difuziju Na+ jona. Akcioni potencijali prenose se po principu sve-ili-ništa, što znači da se, ako su ispunjeni svi uslovi, prostire bez gubitka, sa konstantnom amplitudom, dok se, ako uslovi nisu ispunjeni, uopšte ne prostire. Formiraju se samo na inicijalnom segmentu neurona jer se tu nalazi sedam puta više Na+ jona nego drugde.
Saltatorna kondukcija akcionog potencijala u nervnom vlaknu uredi
Centralni deo aksona ispunjen je aksoplazmom, koja je žitka intracelularna tečnost. Većinu aksona okružuje mijelinski omotač koji ima ulogu izolatora. Ovaj omotač je često znatno deblji od samog aksona, a za njegovo stvaranje u CNS su odgovorni oligodendroctit, dok tu funkciju u perifernim nervnim vlaknima obavljaju Švanove ćelije. Pritom, jedan oligodendrocit stvara mijelin za i do 40 aksona, doj jedna Švanova ćelija oblaže samo jedan segment perifernog aksona. Membrana Švanove ćelije obavije se oko aksona, a zatim se ćelija rotira oko njega, oblažući ga izolatorom koji smanjuje tok jona kroz membranu i do 5.000 puta. Na spoju dve sukcesivne Švanove ćelije nalaze se mala neizolovana područja, dugačka svega 2-3 mikrometra, koja se zovu Ranvijerovi čvorovi. Iako joni skoro ne mogu teći kroz mijelinski omotač mijelisanih nerava, oni sa lakoćom teku kroz Ranvijerove čvorove. Način na koji se akcioni potencijal provodi od čvora do čvora naziva se saltatorna kondukcija. To znači da naelektrisanje teče kroz okolnu ekstracelularnu tečnost koja okružuje mijelinsku opnu, kao i kroz aksoplazmu unutar aksona, ekscitirajući sukcesivne čvorove jedan za drugim, tj. 'skačući' od jednog čvora do drugog, ekscitirajući ih. Saltatorna kondukcija uzrokuje da proces depolarizacije skače duge intervale duž osovine nervnog vlakna, pa tako povećava brzinu nervne transmisije u mijelisanim vlaknima 5-50 puta. Takođe, ovakav način provođenja akcionog potencijala jer čuva energiju za akson, tako što se depolarišu samo Ranvijerovi čvorovi, omogućavajući i do 100 puta manji gubitak jona. Brzina kondukcije u nervnim vlaknima varira od tako malih kao što je 0,25 m/s u malim nemijelisanim nervnim vlaknima, do tako velike, kao što je 120 m/s u veoma debelim mijelisanim vlaknima.
Voltažno-zavisni natrijumski kanali uredi
Voltažno-zavisni Na+ kanal ima dvoja vrata: jedna na spoljašnjem delu ćelije- zvana aktivaciona vrata, i druga, inaktivaciona vrata, u kontaktu sa citosolom. Pri normalnom mirovnom membranskom potencijalu od -90 mV aktivaciona vrata su zatvorena, što onemogućuje ulazak natrijumovih jona kroz ove kanale. Međutim, kada MMP počne da gubi negativnost i raste prema pozitivnom nivou, i kada, u tom procesu, dostigne voltažu između -70 i -50 mV, to izaziva konformacionu promenu u aktivacionim vratima, koja se odmah otvaraju. Ovo stanje povećava propustljivost membrane za Na+ jone od 500 do 5.000 puta. To predstavlja stadijum depolarizacije.
Međutim, nekoliko 10.000-tih delova sekundi nakon otvaranja aktivacionih vrata, zatvaraju se inaktivaciona vrata, a njihovo zatvaranje uzrokuje ista konformacion promena koja je i dovela do otvaranja aktivacionih. Kada dođe do zatvaranja inaktivacionih vrata, membranski potencijal počinje da se obnavlja nazad prema normalnih -90 mV, što predstavlja proces repolarizacije. Ponovno otvaranje natrijumovih kanala neće se dogoditi ako se prethodno MMP ne vrati na normalan nivo od -90 mV ili na približnu vrednost, tj. ako se vlakno ne repolarizuje.
Voltažno-zavisni kalijumovi kanali uredi
Kalijumski kanal poseduje vrata na citosolskom delu membrane, koja su tokom MMP zatvorena i sprečavaju difuziju K+ jona u ekstracelilarnu tečnost. Porast MMP ka nuli uzrokuje konformaciono otvaranje vrata i povećan tok kalijuma ka spolja. Međutim, zbog neznatno odloženog otvaranja kalijumovih kanala, oni se otvaraju u isto vreme kada se natrijumski počnu zatvarati zbog inaktivacije. Tako istovremeno dolazi do smanjenog ulaska Na+ u ćeliju i povećanog izlaska K+ iz ćelije, što smanjuje naelektrisanje i dovodi do obnavljanja normalnog mirovnog membranskog potencijala.
Reference uredi
- ^ Hodgkin, A. L.; Huxley, A. F. (1952). „A quantitative description of membrane current and its application to conduction and excitation in nerve”. The Journal of Physiology. 117 (4): 500—44. PMC 1392413 . PMID 12991237. doi:10.1113/jphysiol.1952.sp004764.
- ^ „Cardiac Muscle Contraction”. www.zoology.ubc.ca. Pristupljeno 2022-08-15.
Literatura uredi
- Guyton, A., Hall, J. (2008). Textbook of Medical Physiology (Eleventh Edition) [Medicinska fiziologija]. Beograd: Savremena administracija.
- Mujović, V. (2004). Medicinska fiziologija: compendium po ukusu studenata. Beograd: A-Z Book.
- Anderson JA, Rosenfeld E, ur. (1988). Neurocomputing: Foundations of Research . Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-01097-9. LCCN 87003022. OCLC 15860311.
- Bernstein J (1912). Elektrobiologie, die Lehre von den elektrischen Vorgängen im Organismus auf moderner Grundlage dargestellt [Electric Biology, the study of the electrical processes in the organism represented on a modern basis]. Braunschweig: Vieweg und Sohn. LCCN 12027986. OCLC 11358569.
- Bower JM, Beeman D (1995). The Book of GENESIS: Exploring Realistic Neural Models with the GEneral NEural SImulation System. Santa Clara, Calif.: TELOS. ISBN 978-0-387-94019-9. LCCN 94017624. OCLC 30518469.
- Brazier MA (1961). A History of the Electrical Activity of the Brain. London: Pitman. LCCN 62001407. OCLC 556863.
- Bullock TH, Horridge GA (1965). Structure and Function in the Nervous Systems of Invertebrates . A series of books in biology. San Francisco: W. H. Freeman. LCCN 65007965. OCLC 558128.
- Bullock TH, Orkand R, Grinnell A (1977). Introduction to Nervous Systems . A series of books in biology. San Francisco: W. H. Freeman. ISBN 978-0-7167-0030-2. LCCN 76003735. OCLC 2048177.
- Field J, ur. (1959). Handbook of Physiology: a Critical, Comprehensive Presentation of Physiological Knowledge and Concepts: Section 1: Neurophysiology. 1. Washington, DC: American Physiological Society. LCCN 60004587. OCLC 830755894.
- Ganong, WF (1991). Review of Medical Physiology. Ganong's Review of Medical Physiology (15th izd.). Norwalk, Conn.: Appleton and Lange. ISBN 978-0-8385-8418-7. ISSN 0892-1253. LCCN 87642343. OCLC 23761261.
- Guckenheimer J, Holmes P, ur. (1986). Nonlinear Oscillations, Dynamical Systems and Bifurcations of Vector Fields. Applied Mathematical Sciences. 42 (2nd izd.). New York: Springer Verlag. ISBN 978-0-387-90819-9. OCLC 751129941.
- Hoppensteadt FC (1986). An Introduction to the Mathematics of Neurons. Cambridge studies in mathematical biology. 6. Cambridge: Cambridge University Press. ISBN 978-0-521-31574-6. LCCN 85011013. OCLC 12052275.
- Junge D (1981). Nerve and Muscle Excitation (2nd izd.). Sunderland, Mass.: Sinauer Associates. ISBN 978-0-87893-410-2. LCCN 80018158. OCLC 6486925.
- Kettenmann H, Grantyn R, ur. (1992). Practical Electrophysiological Methods: A Guide for in Vitro Studies in Vertebrate Neurobiology. New York: Wiley. ISBN 978-0-471-56200-9. LCCN 92000179. OCLC 25204689.
- Keynes RD, Aidley DJ (1991). Nerve and Muscle (2nd izd.). Cambridge: Cambridge University Press. ISBN 978-0-521-41042-7. LCCN 90015167. OCLC 25204483.
- Koch C, Segev I, ur. (1989). Methods in Neuronal Modeling: From Synapses to Networks. Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-11133-1. LCCN 88008279. OCLC 18384545.
- Lavallée M, Schanne OF, Hébert NC, ur. (1969). Glass Microelectrodes. New York: Wiley. ISBN 978-0-471-51885-3. LCCN 68009252. OCLC 686.
- McCulloch WS (1988). Embodiments of Mind. Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-63114-3. LCCN 88002987. OCLC 237280.
- McHenry LC, Garrison FH (1969). Garrison's History of Neurology. Springfield, Ill.: Charles C. Thomas. OCLC 429733931.
- Silverthorn DU (2010). Human Physiology: An Integrated Approach (5th izd.). San Francisco: Pearson. ISBN 978-0-321-55980-7. LCCN 2008050369. OCLC 268788623.
- Spanswick RM, Lucas WJ, Dainty J, ur. (1980). Plant Membrane Transport: Current Conceptual Issues. Developments in Plant Biology. 4. Amsterdam: Elsevier Biomedical Press. ISBN 978-0-444-80192-0. LCCN 79025719. OCLC 5799924.
- Purves D, Augustine GJ, Fitzpatrick D, Hall WC, Lamantia AS, McNamara JO, Williams SM (2001). „Release of Transmitters from Synaptic Vesicles”. Neuroscience (2nd izd.). Sunderland, MA: Sinauer Associates. ISBN 978-0-87893-742-4. LCCN 00059496. OCLC 806472664.
- Purves D, Augustine GJ, Fitzpatrick D, Hall WC, Lamantia AS, McNamara JO, White LE (2008). Neuroscience (4th izd.). Sunderland, MA: Sinauer Associates. ISBN 978-0-87893-697-7. LCCN 2007024950. OCLC 144771764.
- Reeke GN, Poznanski RR, Sporns O, Rosenberg JR, Lindsay KA, ur. (2005). Modeling in the Neurosciences: from Biological Systems to Neuromimetic Robotics. Boca Raton, Fla.: Taylor & Francis. ISBN 978-0-415-32868-5. LCCN 2005298022. OCLC 489024131.
- Schmidt-Nielsen K (1997). Animal Physiology: Adaptation and Environment (5th izd.). Cambridge: Cambridge University Press. ISBN 978-0-521-57098-5. LCCN 96039295. OCLC 35744403.
- Schwann HP, ur. (1969). Biological Engineering. Inter-University Electronics Series. 9. New York: McGraw-Hill. ISBN 978-0-07-055734-5. LCCN 68027513. OCLC 51993.
- Stevens CF (1966). Neurophysiology: A Primer . New York: John Wiley and Sons. ISBN 9780471824367. LCCN 66015872. OCLC 1175605.
- Waxman SG, ur. (2007). Molecular Neurology. Burlington, Mass.: Elsevier Academic Press. ISBN 978-0-12-369509-3. LCCN 2008357317. OCLC 154760295.
- Worden FG, Swazey JP, Adelman G, ur. (1975). The Neurosciences, Paths of Discovery. Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-23072-8. LCCN 75016379. OCLC 1500233.
- Aidley DJ, Stanfield PR (1996). Ion Channels: Molecules in Action. Cambridge: Cambridge University Press. ISBN 978-0-521-49882-1.
- Bear MF, Connors BW, Paradiso MA (2001). Neuroscience: Exploring the Brain. Baltimore: Lippincott. ISBN 0-7817-3944-6.
- Clay JR (maj 2005). „Axonal excitability revisited”. Progress in Biophysics and Molecular Biology. 88 (1): 59—90. PMID 15561301. doi:10.1016/j.pbiomolbio.2003.12.004 .
- Deutsch S, Micheli-Tzanakou E (1987). Neuroelectric Systems. New York: New York University Press. ISBN 0-8147-1782-9.
- Hille B (2001). Ion Channels of Excitable Membranes (3rd izd.). Sunderland, MA: Sinauer Associates. ISBN 978-0-87893-321-1.
- Johnston D, Wu SM (1995). Foundations of Cellular Neurophysiology. Cambridge, Massachusetts: Bradford Book, The MIT Press. ISBN 0-262-10053-3.
- Kandel ER, Schwartz JH, Jessell TM (2000). Principles of Neural Science (4th izd.). New York: McGraw-Hill. ISBN 0-8385-7701-6.
- Miller C (1987). „How ion channel proteins work”. Ur.: Kaczmarek LK, Levitan IB. Neuromodulation: The Biochemical Control of Neuronal Excitability. New York: Oxford University Press. str. 39–63. ISBN 978-0-19-504097-5.
- Nelson DL, Cox MM (2008). Lehninger Principles of Biochemistry (5th izd.). New York: W. H. Freeman. ISBN 978-0-7167-7108-1.
Spoljašnje veze uredi
- Ionic flow in action potentials at Blackwell Publishing
- Action potential propagation in myelinated and unmyelinated axons at Blackwell Publishing
- Generation of AP in cardiac cells and generation of AP in neuron cells
- Resting membrane potential from Life: The Science of Biology, by WK Purves, D Sadava, GH Orians, and HC Heller, 8th edition, New York: WH Freeman, ISBN 978-0-7167-7671-0.
- Ionic motion and the Goldman voltage for arbitrary ionic concentrations at The University of Arizona
- A cartoon illustrating the action potential
- Action potential propagation
- Production of the action potential: voltage and current clamping simulations[mrtva veza]
- Open-source software to simulate neuronal and cardiac action potentials at SourceForge.net
- Introduction to the Action Potential, Neuroscience Online (electronic neuroscience textbook by UT Houston Medical School)
- Khan Academy: Electrotonic and action potential Arhivirano 2 jul 2014 na sajtu Wayback Machine