Metabolizam gvožđa kod čoveka
Metabolizam gvožđa kod čoveka je set hemijskih reakcija koje održavaju ljudsku homeostazu gvožđa na sistemskom i ćelijskom nivou. Gvožđe je neophodno telu, ali je isto tako potencijalno toksično, i kontrolisanje nivoa gvožđa u telu je od kritične važnosti za mnoge aspekte ljudskog zdravlja i sprečavanje bolesti. Hematolozi imaju poseban interest u sistemski metabolizam gvožđa jer je ono esencijalno za crvena krvna zrnca, u kojima je najveći deo gvožđa u ljudskom telu sadržan. Razumevanje metabolizma gvožđa je isto tako važno za razumevanje bolesti usled prezasićenosti gvožđem, kao što je nasledna hemohromatoza, i deficijencije gvožđa, kao što je anemija deficijencije gvožđa.
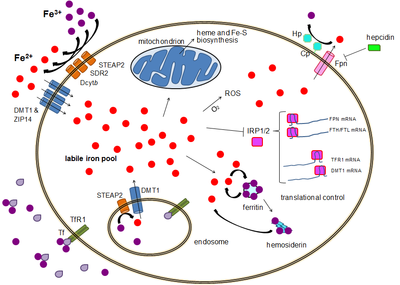
Značaj regulacije gvožđa
уредиGvožđe je esencijalni bioelement za većinu formi života, od bakterija do sisara. Njegov značaj leži u njegovoj sposobnosti da posreduje transfer elektrona. U svom fero stanju, gvožđe deluje kao donor elektrona, dok u feri stanju deluje kao akceptor. Stoga, gvožđe ima vitalnu ulogu u katalizi enzimatskih reakcija u kojima dolazi do elektronskog transfera (redukciji i oksidaciji, redoks). Proteini mogu da sadrže gvožđe kao deo različitih kofaktora, kao što su gvožđe sumporni klasteri (Fe-S) i hem grupe, koji se formiraju u mitohondrijama.
Ćelijska respiracija
уредиLjudskim ćelijama je neophodno gvožđe da bi mogle da dobijaju energiju u vidu ATP molekula u višestepnom procesu poznatom kao ćelijska respiracija, specifičnije iz oksidativne fosforilacije u mitohondrijskim kristama. Gvožđe je prisutno u gvozdeno-sumpornim klusterima i hem grupama u proteinima lanca transporta elektrona koji generišu protonski gradijent čime se omogućava ATP sintazi da sintetiše ATP (hemiosmoza).
Hem grupe su deo hemoglobina, proteina prisutnog u crvenim krvnim zrncima koji učestvuje u transportu kiseonika od pluća do tkiva. Hem grupe su isto tako prisutne u mioglobinu kojim se skladiđti i difuzno prenosi kiseonik u mišićnim ćelijama.
Kiseonikčni transport
уредиLjudskom telu je neophodno gvožđe za transport kiseonika. Kiseonik (O2) je potreban radi funkcionisanja i opstanka skoro svih ćelijskih tipova. Kiseonik se transportuje iz pluća do ostatka tela vezan za hem grupu hemoglobina u eritrocitima. U mišićnim ćelijama, gvožđe je vezano u mioglobinu, koji reguliše njegovo oslobađanje.
Toksičnost
уредиGvožđe je isto tako potencijalno toksično. Njegova sposobnost da donira i prima elektrone znači da ono može da katalizuje konverziju vodonik peroksida u slobodne radikale. Slobodni radikali mogu da naprave štetu u raznim ćelijskim struktura, i ultimatno da dovedu do smrti ćelije.[1]
Gvožđe vezano za proteine ili kofaktore kao što je hem je bezbedno. Takođe, virtualno ne postoje potpuno slobodni joni gvožđa u ćeliji, pošto oni s lakoćom formiraju komplekse sa organskim molekulima. Međutim, deo intraćelijskih jona je vezan u niskoafinitetnim kompleksima, i naziva se labilnim gvožđem ili „slobodnim” gvožem. Gvožđe u takvim kompleksima može da urokuje štetu kao što je gore opisano.[2]
Da bi se sprečila takva vrsta štete, sve životne forme koje koriste gvožđe vezuju atome gvožđa za proteine. Ovo vezivanje omogućava ćelijama da koriste gvožđe uz istovremeno ograničavanje njegove sposobnosti da nanosi povrede.[1][3] Tipično su intraćelijske koncentracije labilnog gvožđa kod bakterija na nivou od 10-20 mikromola,[4] mada one mogu da budu deset puta veće u anaerobnom okruženju,[5] gde su slobodni radikali i reaktivne kiseonične vrste ređe. U ćelijama sisara, koncentracije intraćelijskog labilnog gvožđa su tipično manje od 1 mikromola, što je manje od 5 procenata ukupnog ćelijskog gvožđa.[2]
Reference
уреди- ^ а б Conrad ME, Umbreit JN (april 2000). „Disorders of iron metabolism”. The New England Journal of Medicine. 342 (17): 1293—4. PMID 10787338. doi:10.1056/NEJM200004273421716.
- ^ а б Kakhlon O, Cabantchik ZI (2002). „The labile iron pool: characterization, measurement, and participation in cellular processes”. Free Radical Biology and Medicine. 33 (8): 1037—1046. doi:10.1016/s0891-5849(02)01006-7.
- ^ Andrews NC (decembar 1999). „Disorders of iron metabolism”. The New England Journal of Medicine. 341 (26): 1986—95. PMID 10607817. doi:10.1056/NEJM199912233412607.
- ^ Yan Y, Waite-Cusic JG, Kuppusamy P, Yousef AE (januar 2013). „Intracellular free iron and its potential role in ultrahigh-pressure-induced inactivation of Escherichia coli”. Applied and Environmental Microbiology. 79 (2): 722—724. PMC 3553779 . PMID 23124235. doi:10.1128/aem.02202-12.
- ^ Yamamoto Y, Fukui K, Koujin N, Ohya H, Kimura K, Kamio Y (2004). „Regulation of the intracellular free iron pool by Dpr provides oxygen tolerance to Streptococcus mutans.”. Journal of Bacteriology. 186 (18): 5997—6002. PMC 515136 . PMID 15342568. doi:10.1128/jb.186.18.5997-6002.2004.
Literatura
уреди- Andrews S, Norton I, Salunkhe AS, Goodluck H, Aly WS, Mourad-Agha H, Cornelis P (2013). „Chapter 7, Control of Iron Metabolism in Bacteria”. Ур.: Banci L. Metallomics and the Cell. Metal Ions in Life Sciences. 12. Springer. ISBN 978-94-007-5560-4. doi:10.1007/978-94-007-5561-1_7. electronic-book ISBN 978-94-007-5561-1 ISSN 1559-0836 electronic{issn|1868-0402}
- Andrews NC (maj 2004). „Anemia of inflammation: the cytokine-hepcidin link”. The Journal of Clinical Investigation. 113 (9): 1251—3. PMC 398435 . PMID 15124013. doi:10.1172/JCI21441.
- Camaschella C (decembar 2005). „Understanding iron homeostasis through genetic analysis of hemochromatosis and related disorders”. Blood. 106 (12): 3710—7. PMID 16030190. doi:10.1182/blood-2005-05-1857.
- Frazer DM, Anderson GJ (oktobar 2005). „Iron imports. I. Intestinal iron absorption and its regulation”. American Journal of Physiology. Gastrointestinal and Liver Physiology. 289 (4): G631—5. PMID 16160078. doi:10.1152/ajpgi.00220.2005.
- Insel P, Ross D, McMahon K, Bernstein M (2011). „Iron”. Nutrition (4th изд.). Sudbury, Massachusetts: Jones and Bartlett Publishers. стр. 510—514. ISBN 978-0-7637-7663-3. Приступљено 25. 6. 2012. See espp. 513-514
- Lammi-Keef CJ, Couch SC, Philipson EH, ур. (2008). „Dietary diversification and modification of iron”. Handbook of Nutrition and Pregnancy. Nutrition & Health. Totowa, New Jersey: Humana Press. стр. 350—351. ISBN 978-1-59745-112-3. doi:10.1007/978-1-59745-112-3. Приступљено 25. 6. 2012.
- Micronutrients, Panel on; Subcommittees on Upper Reference Levels of Nutrients and of Interpretation and Uses of Dietary Reference Intakes; the Standing Committee on the Scientific Evaluation of Dietary Reference Intakes (2001). „Iron”. Dietary Reference Intakes for Vitamin A, Vitamin K, Arsenic, Boron, Chromium, Copper, Iodine, Iron, Manganese, Molybdenum, Nickel, Silicon, Vanadium, and Zinc. Washington, D.C: Food and Nutrition Board, Institute of Medicine. стр. 290—393. ISBN 978-0-309-07279-3. Приступљено 25. 6. 2012.
- Reilly, C. (2004). „Iron”. The Nutritional Trace Metals. Oxford, UK & Ames, Iowa: Blackwell Publishing. стр. 35—81. ISBN 978-1-4051-1040-2. Приступљено 25. 6. 2012.