Гликоген
Гликоген је полисахарид и полимер глукозе који представља примарну складишну форму угљених хидрата код животиња,[2] гљива, и бактерија.[3] Настаје првенствено у јетри и мишићима, мада готово све телесне ћелије имају способност складиштења мањих количина гликогена.[4] Депои гликогена у јетри представљају резерве глукозе које се, у случају пада концентрације глукозе у крви, веома брзо могу мобилисати и тај пад компензовати. Гликоген депонован у мишићима представља извор енергије током интензивних физичких напора, при чему ослобођена глукоза никада не прелази у крвоток.[5] Иако далеко мање заступљене од резерви липида, резерве гликогена су веома важне и у енергетски суфицитарним стањима, при повећаним концентрацијама глукозе, прве се попуњавају.


Гликоген функционише као један од два облика резерве енергије, при чему је гликоген краткорочан, а други облик је складиштење триглицерида у масном ткиву (тј. телесна маст) за дугорочно чување. Код људи се гликоген производи и складишти превасходно у ћелијама јетре и скелетних мишића.[6][7] У јетри гликоген може да чини 5–6% свеже масе органа, а јетра одрасле особе масе 1,5 kg може да складишти око 100–120 грама гликогена.[6][8] У скелетним мишићима налази се гликоген у ниској концентрацији (1–2% мишићне масе), а скелетни мишићи одрасле особе тежине 70 kg складиште приближно 400 грама гликогена.[6] Количина гликокогена који се чува у телу - посебно у мишићима и јетри - највише зависи од физичког тренинга, стопе базалног метаболизма и прехрамбених навика. Мале количине гликогена налазе се и у другим ткивима и ћелијама, укључујући бубреге, црвена крвна зрнца,[9][10][11] бела крвна зрнца,[12] и глијалне ћелије у мозгу.[13] Материца такође складишти гликоген током трудноће да би хранила ембрион.[14]
Приближно 4 грама глукозе је присутно је у крви људи у сваком тренутку;[6] код појединаца који су постили глукоза у крви се одржава константном на овом константном нивоу на штету складишта гликогена у јетри и скелетним мишићима.[6] Складишта гликогена у скелетним мишићима служе као облик складиштења енергије за саме мишиће;[6] међутим, распад мишићног гликогена омета мишићни унос глукозе из крви, чиме се повећава количина глукозе у крви која је доступна за употребу у другим ткивима.[6] Залихе гликогена из јетре служе као резерве глукозе за употребу у целом телу, посебно у централном нервном систему.[6] Људски мозак троши приближно 60% глукозе у крви код седентарних особа које посте.[6]
Гликоген је аналог скроба, полимера глукозе који делује као складиште енергије у биљкама. Он има структуру сличну амилопектину (састојку скроба), али је разгранатији и компактнији од скроба. Обе материје су бели прахови у сувом стању. Гликоген се налази у облику гранула у цитосолу/цитоплазми у многим типовима ћелија и игра важну улогу у циклусу глукозе. Гликоген формира резерву енергије која се може брзо мобилисати да задовољи изненадну потребу за глукозом, али је то мање компактан облик енергетских резерви у односу на триглицериде (липида). Као такав се такође налази као резерва у многим паразитским протозоима.[15][16][17]
Структура
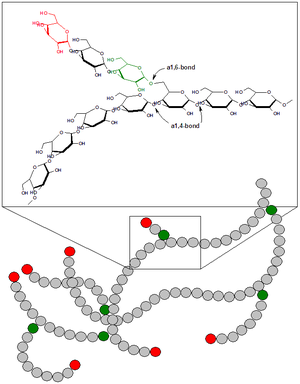
уредиГликоген је разгранати хомополисахарид (хомогликан) чију моносахаридну јединицу чине молекули α-D-глукозе.[18] Садржи до 50.000 остатака овог моносахарида, при чему молекулска маса варира између 106 и 1.6×107 далтона. Молекули глукозе су у највећој мери повезани α-(1→4)-гликозидним везама чиме се формирају дужи ланци, да би се они даље гранали, формирајући бочне ланце преко α-(1→6)-гликозидних веза. Разгранатост молекула је варијабилна, па се у средишту молекула бочни ланци одвајају на свака четири остатка глукозе (бочни ланци никада нису ближи од 4 остатка, услед специфичности ензима гранања), док су бочне гране на периферији молекула ређе, тек на сваких 6-10 молекула глукозе.[5] Оваква организација молекула условљава постојање великог броја нередукујућих крајева, што је битно за брзу хидролизу молекула јер се разградња гликогена одвија управо са нередукујућих крајева. Поред тога, нелинеарност молекула омогућава и његово густо паковање, секундарна структура је углавном глобуларна и заузима веома мало простора (у поређењу са молекулском масом). Редукујући крај гликогена лоциран је у унутрашњости и не налази се слободан. За њега је ковалентно, преко остатка тирозинске групе, везан специфичан протеин — гликогенин.[19] Гликогенин има улогу прајмера у биосинтези гликогена, у условима када она почиње од прекурсора са мање од 7 остатака глукозе.
Заступљеност и улога у организму
уредиУкупне резерве гликогена у организму су примарно сконцентрисане у јетри и мишићима.[20] Код одрасле особе, до 100g гликогена налази се у јетри, а додатних 200g у мишићном ткиву.[21] Гликоген се депонује у виду гранула лоцираних у цитосолу ћелија. Ћелије јетре могу складиштити гликоген максимално у уделу од 5-8% своје масе, док је код мишића овај проценат нижи, и износи око 1-3%.[4] У којој мери су ове ћелије засићене гликогеном, зависи првенствено од дужине трајања гладовања, физичке активности али и удела угљених хидрата у исхрани појединца. Уз мировање, депои гликогена могу да задовоље енергетске потребе организма током периода од око 12 сати интензивног гладовања.[22]
Гликоген се не депонује у ткивима у већој мери од споменуте јер не представља најрационалнији складишни облик енергије — везује два пута већу количину воде од своје масе, а даје 2,5 пута мање енергије од исте масе неутралних масти.
Резерве гликогена подлежу сталној деплецији и обнављању. По уносу и апсорпцији хране богате угљеним хидратима, долази до повећања нивоа глукозе у крви што утиче на лучење инсулина из панкреаса. Инсулин, низом комплексних регулаторних улога у метаболизму које обавља, утиче на повећан улаз глукозе у ћелије. Како је глукоза осмотски веома активна, нормално се не складишти у ћелији већ брзо подлеже гликолизи. У ћелијама јетре и мишића инсулин истовремено активира процес стварања гликогена — гликогенезу — што омогућава конвертовање преузете глукозе у гликоген. По засићењу ћелија гликогеном, сувишна глукоза низом метаболичких процеса бива претворена у липиде, и сувишна енергија ускладиштена у виду триацилглицерола.
Судбина гликогена у јетри
уредиПо престанку прилива глукозе из гастроинтестиналног тракта, нивои инсулина опадају. За хомеостазу глукозе у крви одговоран је још један хормон — глукагон. Како је глукоза најнепосреднији извор енергије за ћелије, а за неуроне и једини (осим током периода дуготрајног гладовања), ниво глукозе у крви последично почиње да опада. Глукагон смањује степен преузимања глукозе из крвотока, инхибира невиталне анаболичке процесе, и регулаторно утиче на мобилизацију резерви гликогена. Ослобођена глукоза из хепатоцита затим прелази у крвоток. Суштински, гликоген јетре представља депо глукозе који, између оброка, обезбеђује константан прилив овог шећера периферним органима и ткивима. Ова улога се назива и пуферском улогом јетре за глукозу.[4]
Судбина гликогена у мишићима
уредиГликоген у мишићима не учествује у хомеостази глукозе, већ служи искључиво као резерва енергије у самим мишићима. Под условима мировања или умерене физичке активности, енергетске потребе за одржавање мишићног тонуса и умереног мишићног рада подмирују се аеробним метаболизмом — масне киселине, глукоза и кисеоник се у довољном обиму допремају до мишићног ткива, разграђују и коначно укључују у респираторни ланац чиме се, оксидативном фосфорилацијом, обезбеђује знатна количина енергије која задовољава 95% енергетских потреба мишића под наведеним условима.[4] Током интензивног физичког рада, потребе за енергијом се јако повећавају па релативно спор аеробни метаболизам није довољан да их подмири. По деплецији креатин-фосфата, као најнепосредније резерве енергије депоноване у мишићима, започиње гликогенолиза. Овим се брзо ослобађају велике количине ускладиштене глукозе која се разграђује до пирувата, а затим и редукује до лактата, уз стварање АТП. Анаеробни пут стварања АТП је око 100 пута бржи од аеробног.[5]
Метаболизам
уредиКатаболизам гликогена
уредиПроцес разградње гликогена до глукозе назива се гликогенолиза. То је процес који катализују три ензима, и којим се одваја по један молекул глукозе, у виду глукозе-6-фосфата, са нередукујућих крајева гликогена. Процес је под контролом бројних фактора, али се суштински заснива на алостерној модулацији и ковалентној модификацији ензима који га катализују. Настала глукоза-6-фосфат (G6P) у хепотоцитима подлеже дефосфорилацији под дејством специфичне фосфатазе, након чега глукоза дифундује у крвоток. Један део G6P улази и у фосфоглуконатни пут. G6P у мишићима се првенствено укључује у гликолитички пут.[23]
Анаболизам гликогена
уредиПроцес биосинтезе гликогена назива се гликогенеза. То је, такође, процес који катализује три ензима, при чему је прва реакција — реакција формирања УДП-глукозе, ендергонска. Њена суштина је активација гликозидних јединица које се затим везују у растући ланац гликогена, при чему се везана енергија троши за формирање гликозидне везе. У ћелијама где је дошло до потпуне деплеције гликогена, за његову синтезу је неопходан гликогенин као прајмер који омогућава и аутокатализује везивање првих 7 остатака глукозе. И гликогенеза је строго контролисан, посебно хормонима посредованом ковалентном модификацијом гликоген-синтазе.
Поремећаји
уредиКако је централни хормон метаболизма гликогена првенствено инсулин, већина стечених поремећаја метаболизма гликогена везана је за патолошки смањене или повишене нивое инсулина. Један део поремећаја је и урођене природе, и последица је недостатка или дисфункције ензима укључених у метаболизам гликогена. Овакви поремећаји се једним именом називају поремећаји складиштења гликогена.
Хипогликемија, узрокована вишком инсулина спречава одвијање гликогенолизе, инхибирајући гликоген-фосфорилазу, и самим тим спречава ослобађање резерви глукозе. Дефицит инсулина пак спречава улазак глукозе у ћелије, па и формирање резерви у виду гликогена. Нормализација метаболизма глукозе углавном нормализује и метаболизам гликогена.
Референце
уреди- ^ McArdle, William D.; Katch, Frank I.; Katch, Victor L. (2007). Exercise Physiology: Energy, Nutrition, and Human Performance. Lippincott Williams & Wilkins. ISBN 978-0-7817-4990-9.
- ^ Sadava; et al. (2011). Life (9th, International изд.). W. H. Freeman. ISBN 9781429254311.
- ^ Berg, Jeremy M. (Jeremy Mark) (8. 4. 2015). Biochemistry. Tymoczko, John L., 1948-, Gatto, Gregory J., Jr. (Gregory Joseph), Stryer, Lubert. (Eighth изд.). New York. ISBN 9781464126109. OCLC 913469736.
- ^ а б в г Arthur C. Guyton, John E. Hall: Textbook of Medicinal Physiology, превод једанаестог издања, Савремена администрација, Београд, 2008.
- ^ а б в Славица Спасић, Зорана Јелић-Ивановић, Весна Спасојевић-Калимановска: Општа биохемија, ауторско издање, Београд, 2002.
- ^ а б в г д ђ е ж з Wasserman DH (јануар 2009). „Four grams of glucose”. American Journal of Physiology. Endocrinology and Metabolism. 296 (1): E11—21. PMC 2636990 . PMID 18840763. doi:10.1152/ajpendo.90563.2008. „Four grams of glucose circulates in the blood of a person weighing 70 kg. This glucose is critical for normal function in many cell types. In accordance with the importance of these 4 g of glucose, a sophisticated control system is in place to maintain blood glucose constant. Our focus has been on the mechanisms by which the flux of glucose from liver to blood and from blood to skeletal muscle is regulated. ... The brain consumes ∼60% of the blood glucose used in the sedentary, fasted person. ... The amount of glucose in the blood is preserved at the expense of glycogen reservoirs (Fig. 2). In postabsorptive humans, there are ∼100 g of glycogen in the liver and ∼400 g of glycogen in muscle. Carbohydrate oxidation by the working muscle can go up by ∼10-fold with exercise, and yet after 1 h, blood glucose is maintained at ∼4 g.”
- ^ Kreitzman SN, Coxon AY, Szaz KF (1992). „Glycogen storage: illusions of easy weight loss, excessive weight regain, and distortions in estimates of body composition” (PDF). The American Journal of Clinical Nutrition. 56 (1 Suppl): 292s—93s. PMID 1615908. doi:10.1093/ajcn/56.1.292S.
- ^ Guyton, Arthur C.; John Edward Hall (2011). Guyton and Hall Textbook of Medical Physiology. New York, New York: Saunders/Elsevier. ISBN 978-5-98657-013-6.
- ^ Moses SW, Bashan N, Gutman A (децембар 1972). „Glycogen metabolism in the normal red blood cell”. Blood. 40 (6): 836—43. PMID 5083874. doi:10.1182/blood.V40.6.836.836 .
- ^ Ingermann RL, Virgin GL (1987). „Glycogen content and release of glucose from red blood cells of the sipunculan worm themiste dyscrita” (PDF). J Exp Biol. 129: 141—9.
- ^ Miwa I, Suzuki S (новембар 2002). „An improved quantitative assay of glycogen in erythrocytes”. Annals of Clinical Biochemistry. 39 (Pt 6): 612—13. PMID 12564847. doi:10.1258/000456302760413432.
- ^ Scott, RB (јун 1968). „The Role of Glycogen in Blood Cells”. New England Journal of Medicine. 278 (26): 1436—1439. PMID 4875345. doi:10.1056/NEJM196806272782607.Шаблон:Mcn
- ^ Oe Y, Baba O, Ashida H, Nakamura KC, Hirase H (јун 2016). „Glycogen distribution in the microwave-fixed mouse brain reveals heterogeneous astrocytic patterns”. Glia. 64 (9): 1532—45. PMC 5094520 . PMID 27353480. doi:10.1002/glia.23020.
- ^ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston: Pearson Prentice Hall. ISBN 978-0-13-250882-7.
- ^ Ryley, JF (март 1955). „Studies on the metabolism of the protozoa. 5. Metabolism of the parasitic flagellate Trichomonas foetus.”. The Biochemical Journal. 59 (3): 361—9. PMC 1216250 . PMID 14363101. doi:10.1042/bj0590361.
- ^ Benchimol, Marlene; Elias, Cezar Antonio; De Souza, Wanderley (децембар 1982). „Tritrichomonas foetus: Ultrastructural localization of calcium in the plasma membrane and in the hydrogenosome”. Experimental Parasitology. 54 (3): 277—284. ISSN 0014-4894. PMID 7151939. doi:10.1016/0014-4894(82)90036-4.
- ^ Mielewczik, Michael; Mehlhorn, Heinz; Al-Quraishy, Saleh; Grabensteiner, E.; Hess, M. (1. 9. 2008). „Transmission electron microscopic studies of stages of Histomonas meleagridis from clonal cultures”. Parasitology Research (на језику: енглески). 103 (4): 745—50. ISSN 0932-0113. PMID 18626664. doi:10.1007/s00436-008-1009-1.
- ^ David L. Nelson; Michael M. Cox (2005). Principles of Biochemistry (IV изд.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ^ Jan Koolman, Klaus-Heinrich Roehm: Color Atlas of Biochemistry, second edition, revised and enlarged, Thieme, Stuttgart-New York, 2005.
- ^ Keith Parker; Laurence Brunton; Goodman, Louis Sanford; Lazo, John S.; Gilman, Alfred (2006). Goodman & Gilman's The Pharmacological Basis of Therapeutics (11. изд.). New York: McGraw-Hill. ISBN 0071422803.
- ^ David Shier, Jackie Butler, Ricki Lewis: Hole's Human Anatomy and Physiology, 8th edition, WCB/McGraw-Hill, 1999.
- ^ Kotoulas OB, Ho J, Adachi F, Weigensberg BI, Phillips MJ (1971). „Fine structural aspects of the mobilization of hepatic glycogen. II. Inhibition of glycogen breakdown” (PDF). Am. J. Pathol. 63 (1): 23—36. PMC 2047463 . PMID 4323475.
- ^ Donald Voet; Judith G. Voet (2005). „Chapter 17 Glycolysis”. Biochemistry (3 изд.). Wiley. ISBN 9780471193500.
Литература
уреди- McArdle, William D.; Katch, Frank I.; Katch, Victor L. (2007). Exercise Physiology: Energy, Nutrition, and Human Performance. Lippincott Williams & Wilkins. ISBN 978-0-7817-4990-9.
Спољашње везе
уреди- Glycogen storage disease – McArdle's Disease Website
- Glycogen на US National Library of Medicine Medical Subject Headings (MeSH)