Целијачна болест
Целијачна болест или целијакија је најчешћа хронична гастроентеролошка аутоимуна болест коју карактерише неподношљивост организма на глутен, бјеланчевину пшенице, јечма, ражи и зоби. Обољели морају да се придржавају стриктне дијете, која је скупа, а подразумијева конзумирање намирница без глутена.[1]
| Целијачна болест | |
|---|---|
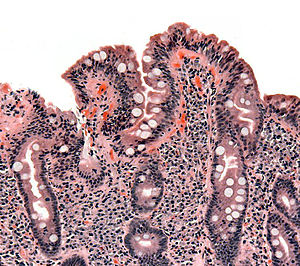 | |
| Класификација и спољашњи ресурси | |
| Специјалност | гастроентерологија |
| Patient UK | [https://patient.info/doctor/coeliac-disease-pro coeliac-disease-pro Целијачна болест] |
Епидемиологија уреди
И поред сазнања да скоро 30% популације носилац гена неопходног за развој целијакије (хаплотип DQ2 i DQ8) само 1% је развило болест и преваленца је у порасту широм света. Разлог ове појаве је непознат. Хипотезе да је појчан садржај глутена у „ модерним житима“ и пораст употребе глутена са временом, су бесмислене, будући да је конзумација жита (свих врста) опала са 99 kg по особи у 1900. години на 60 kg по особи у 2008 години.[2]
Етиопатогенеза уреди
Целијачна болест је аутоимуно обољење узроковано глијадином и сродним проламинима пшенице, ражи и јечма. Ови протеински фрагменти код генетски предиспонираних особа долазе у контакт са интрацелуларним ензимом ткивна трансглутаминаза, која их деаминира (деаминиран глијадин) што доводи до промене стања и облика протеина. Овако измењени пептиди су лако прихватљиви од HLA DQ2 i DQ8 (молекула изложених на површини ламине проприе познате као антиген презентујуће ћелије) ка CD4 Т ћелијама што резултује каскаднном реакцијом која укључује урођени и стечени имунитет и на крају доводи до оштећења цревних ресица.[2]
Фактори средине уреди
У факторе средине доприносе повећаној преваленце целијачне болести спадају:
- Начин порођаја (нарочити ризик представља царски рез),
- Ране инфекције — у зависности од узрочника, могу повећати ризик за развој целијачне болести
- Излагање антибиотицима — мада иако се налази сигнификантна корелација са употребом антибиотика, ипак се не налази сигнификантна корелација са употребом антибиотика
- Исхрана у одојачком узрасту
- Сезона рођења
- Социо-економски статус
- Генска предиспозиција — која према недавним студијама показују да време и количина глутена уведеног у исхрану одојчета и релација са природном исхраном немају значајног удела у испољавању целијакије, већ да важну улогу у настанку целијачне болести има генотип високог ризика HLA DQ2 и DQ8. То потврђују и наредне генерације члана породице који болује од целијакије, које су у повећаном ризику за развој ове болести. Тај ризик је код рођака првог степена (родитељ, брат, сестра, дете): 1 од 22 особе. Код рођака другог степена (тетка, стриц, дед, нећакиња, нећак, рођак или полубрат): 1 у 39.
- Хроничне болести — као што је друга аутоимуна стања и болести, која увећавају ризик од целијакије код следећих болести: тип 1 дијабетеса, болести штитасте жлезде, Сјогренов синдром, јувенилни идиопатски артритис, синдром раздражљивих црева, периферну неуропатију, Даунов синдром, Турнер-ов синдром, Вилијаамсов синдром, недостатак ИгА.
- Улога макробиота — се у последње време јако фаворизује као хипотеза усмерена на улогу микробиота у појави болести. Чињеница је да микробиом утиче на развој имунског система и аутоимуних болести; измењена композиција цревне микробиоте описана у пацијената са целијачном болешћу се нормализује после третмана са дијетом без глутена.
Клиничка слика уреди
Клиничка слика се код неких појединца развија рано у животу, док се други осећају здраво до дубоке старости, јер такве особе са целијачном болести немају никаквих знакова или симптоме.
Због полиморфности манифестних промена клиничка презентација целијакије може бити:
Типична — подразумева присутне гастроинтестиналне симптом. Типична целијакија се караткреише позитивним тестом серологије, са симптомима или без њих и без видљиве интестиналне инфламације на биопсији. Иако су типичне презентације биле много учесталије напочетку и на средини 20. века, после 80-их година 20. века се бележи заокрет од класичних гастроинтестиналних симптома ка више случајева са атипичном и асимптоматском презентацијом, с тим да су најређе оне са слабијим напредовањем у телесној маси.
Атипична — има превасходно екстраинтестиналне манифестације.
Тиха целијакија — описује асимптоматске пацијенте са позитивним тестом серологије и интестиналном инфламацијом на биопсији
Потенцијална форма — укључује пацијенте са позитивним тестом серологије, са симптомима или без њих и без видљиве интестиналне инфламације на биопсији.
Најчешћи клинички знаци и симптоми уреди
На основу бројних истраживања спроведеним у први деценијама 21. века утврђено је да постоји више од 300 симптома целијакије, који се могу разликовати од особе до особе, и зато се због велике бројности могу разврстати на следећи начин:
| Органиски системи | Знаци и симптоми |
|---|---|
| Општи |
|
| Централни нервни систем |
|
| Кожа и слузокожа |
|
| Гастроинтестинални систем |
|
| Репродуктивни систем |
|
| Мускулоскелетни и зубни систем |
|
Дијагноза уреди
Овај одељак би требало проширити. Можете помоћи додавањем садржаја. |
Терапија уреди
Овај одељак би требало проширити. Можете помоћи додавањем садржаја. |
Извори уреди
- ^ Radlović N, Leković Z, Radlović V, et al. Alergija na hranu u dečjoj dobi – klinički aspekt Biomedicinska istraživanja. 2017; 8(2):208-14.
- ^ а б Jericho H, Assiri A, Guandalini S. Celiac disease and wheat intolerance syndrome: A critical update and reappraisal. J Pediatr Gastroenterol Nutr. 2017; 64:15–21.
Спољашње везе уреди
- Званична презентација Удружења Србије за целијакију, Приступљено 18. априла 2011.
- Целијакија – одговори на најчешћа питања, Биошпајз, Приступљено 18. априла 2011.
| Класификација | |
|---|---|
| Спољашњи ресурси |
| Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |