Intrauterina fetalna hipoksija
Intrauterina fetalna hipoksija je patološko stanje a ne bolest, koje se javlja kada fetusa, kada on iz određenih razloga (prolaps ili okluzija pupčane vrpce, placentarni infark, pušenje majke, prenatalna asfiksija itd) u svom organizmu nema dovoljnu količinu kiseonika. Intrauterina hipoksija, ukoliko duže traje, može izazvati reverzibilno oštećenje ćelija unutar centralnog nervnog sistema (mozga i kičmene moždine), ili rezultovati povećanom stopom smrtnosti, uključujući povećani rizik od sindroma iznenadne smrti odojčadi (SIDS). Snižen nivo kiseonika kod fetusa i novorođenčeta je jedan od bitnih činilaca bilo kao primarni ili kao doprinosneći faktor u brojnim neurološkim i neuropsihijatrijskim poremećajima kao što su epilepsija, poremećaj hiperaktivnosti sa nedostatkom pažnje, poremećaji u ishrani i cerebralna paraliza.[1][2][3][4][5]
| Intrauterina fetalna hipoksija | |
|---|---|
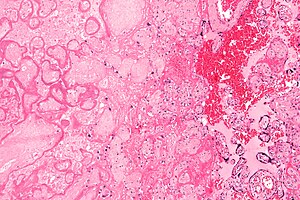 | |
| Patohistološki preparat infarkta placente (na slici levo), kao uzrok intrauterine hipoksije. |
Epidemiologija uredi
Embriogeneza, rast fetusa i njegovo preživljavanje u perinatalnom periodu zavisi od optimalnog zdravlja majke i od normalnog razvoj placente. Izlaganje majke upornom hipoksičnom okruženju može dovesti do kritičnih oštećenja vitalnih organa fetusa. Neuspeh normalne funkcije placente može imati složene akutne i hronični efekte ne samo na razvoj fetusa i intrauterine poremećaja rasta, već i na pojave asfiksije i drugih višestrukih poremećaja poput preranog perioda porođaja i perinatalne smrti.
I pored tog što je savremena medicina dovoljno dobro proučila patologiju fetalne hipoksije, i tako postala sposobna da je pravovremeno identifikuje i eliminiše epidemiološki gledano broj slučajeva iz ove patologije (sa više od 10% svih trudnoća i porođaja), u isto vreme ne opada, već suprotno očekivanjima raste, i postaje jedan je od glavnih uzroka morbiditeta i mortaliteta u nerođenih beba i/ili novorođenčadi u prvoj nedelji života.[6]
Primera radi, u SAD, intrauterini poremećaj rasta i prematurne komplicije javljaju se u oko 12% trudnoća i predstavlja glavni uzrok perinatalni mortalitet i morbiditet koji do današnjih dana čini do 75% perinatalnih smrti.[7]
Dugoročno gledano intrauterina fetalna hipoksija, za sobom ostavlja i brojne organske posledice, kao što su cerebralna paraliza, gubitak sluha, retinopatije i hronična pluća bolest, što je direktno povezano sa značajnim emocionalnim opterećenjem ugroženih porodica sa ovakvom decom i velikim troškove zdravstvene zaštite kako za pojedinca tako i za društvo u celini.[7]
Etiopatogeneza uredi
Na početku embrionalnog razvoja fetusa, hipoksija ne igra glavnu ulogu, jer u ranom razvoju strukturalnih srčanih malformacija verovatno zbog toga što se u ranom razvojnom periodu embriogeneza ovaj proces ionako odvija u anaerobnim uslovima. Tek od drugog i trećeg trimestra, kiseonik postaje važan činilac za normalnu fetalnu organogenezu i dalji rast fetusa. Ako se u toj fazi fetus izloži akutnoj hipoksiji, on u cilju zaštite on još ima brojne zaštitne mehanizme:
- Neposrednu zaštitu od oksidativnog stresa uspostavljenom regulacijom gena.[8]
- Stimulaciju sinteze azot oksida, koja poboljšava ćelijsku signalizaciji za pokretanje mehanizme odbrane, zatim nastaje inhibicija trombocita i regulacija apoptoze.
- β2AR and Gsα regulišu i održaju dovoljan kardiološki učinak.
Međutim kod perzistentne (hronične) hipoksije dolazi do preranog izlaska organizma fetusa iz normalnog ćelijskog ciklusa, što dovodi do pojačane apoptoze (koja je manje izražena), i hipertrofije kardiomiocita. Iako ovaj proces ima za cilj da stvori bolju energetsku efikasnost tokom hipoksičnih uslova on takođe rezultuje manjom veličinom srčanih komora.[9] Izmenjena regulacija izazvana hipoksijom, potom dovodi do pojave ekspresija gena, kao odgovor na intrauterinu hipoksiju, kaja se dalje nastavlja u zrelo doba i oponaša promene kod odraslih sa hroničnom srčanom insuficijencijom.
U daljem toku razvoja trudnoće hipoksija usporava rast fetusa, a restrikcija rasta se sada smatra faktorom rizika od prevremene arterijske hipertenzije i kardiovaskularne bolesti, verovatno sekundarnog porekla u odnosu na endotelne disfunkcije.
Etiološki faktori uredi
Za nastanak intrauterine fetalne hipoksije kao najznačajniji etiološki faktori navode se direktni i indirektni činioci:
Direktni činioci — su neposredno povezani sa trudnoćom, prate nedostatak kiseonika u organizmu fetusa i novorođenčadi, i uzrokuje izuzetno veliki broj komplikacija tokom trudnoće i porođaja
Indirektni činioci — u koje spadaju brojni uzroci koji nisu direktno povezani sa trudnoćom.
Svi uzroci koji mogu dovesti do antenatalne, intranatalne i perinatalne hipoksiju fetusa mogu se podeliti u pet grupa.
| Grupa poremećaja | Patologija | Etiološki činioci |
|---|---|---|
| Prva | Placentalna patologija | Anomalije razvoja, placente previja i placentelna abrupcija, traume, hemoragija, tumori, infekcije placente. |
| Druga | Patologija pupčane vrpce | Razvojne anomalije, torzija pupčane vrpce, pravi čvor pupčane vrpce. |
| Treća | fetalne patologije | Senzitizacija rezus faktora, intrauterina retardacija rasta, intrauterine infekcije, malformacije fetusa, genetske bolesti. |
| Četvrta | Komplikovan tok trudnoće i porođaja | Najveći udeo u ovoj grupi čini gestoza i dugotrajna opasnost od abortusa. Ostali, ne manje važni uzroci obuhvataju: anemiju tokom trudnoće, nefropatiju, antifosfolipidnom sindrom, intrauterine infekcije, polihidramnion i oligohidramnion, višesgtruku trudnoću, prevremeni porođaj, disfunkciju materice, produženu trudnoću. |
| Peta | Hroničnih poremećaja u trudnoći | Najćešča stanja u ovoj grupi su: kardiovaskularne promene (reumatizam, bolesti srca, cardiopsichoneurosis), endokrinih (dijabetesa, bolesti štitaste žlezde, gojaznost), hronične bolesti bubrega, pluća, jetre, krvi, karcinom, narkomanija, alkoholizam. |
Svi navedeni uzroci dovode i do materično — posteljične insuficijencije, glavnog faktora u razvoju hronične hipoksije, koja u nekim slučajevima može biti posledica uticaja npr. egzogenih činilaca koji se javljaju u uslovima niskog parcijalnog pritiska kiseonika u udahnutogm vazduhu (visinska područja, daleko na severu sveta, itd).
Oblici intrauterine hipoksije uredi
Kako je ntrauterina hipoksija povezana sa raznim stanjima majčine placente i stanjem samog fetusa što se može manifestovati drugačije i imati različite ishode. Kingdom i Kaufman su [29]radi lakšeg sagledavanja ovog poremećaja predložili sledeću klasifikuju, ili 3 podtipa hipoksičnih stanja u trudnoći
| Potip hipoksije | Glavne karakteristike |
|---|---|
| Preplacentna hipoksija |
|
| Uteroplacentna hipoksija |
|
| Postplacentna hipoksija |
|
Oblici intrauterine hipoksije prema trajanju uredi
Akutna hipoksija ploda uredi
Uzroci akutne hipoksije ploda koji izazivaju brzi prekid dotoka kiseonika u telo mogu biti:
- prolaps pupčannika,
- čvrsto uplitanje pupčane vrpce oko vrata fetusa,
- čvrsto uvrtanje pupčane vrpce oko svoje ose,
- akutno krvarenje materice,
- placenta praevija i prevremeno odvajanje posteljice tokom porođaja,
- abnormalni položaj ploda,
- prevremeni porođaj, itd .
Hronična hipoksija ploda uredi
Ovaj odeljak bi trebalo proširiti. Možete pomoći dodavanjem sadržaja. |
Izvori uredi
- ^ Maslova, MV; Maklakova, AS; Sokolova, NA; Ashmarin, IP; Goncharenko, EN; Krushinskaya, YV (2003). „The effects of ante- and postnatal hypoxia on the central nervous system and their correction with peptide hormones”. Neuroscience and Behavioral Physiology. 33 (6): 607—11. PMID 14552554. doi:10.1023/A:1023938905744.
- ^ Bulterys, MG; Greenland, S; Kraus, JF (1990). „Chronic fetal hypoxia and sudden infant death syndrome: interaction between maternal smoking and low hematocrit during pregnancy”. Pediatrics. 86 (4): 535—40. PMID 2216618.
- ^ Peleg, D; Kennedy, CM; Hunter, SK (1998). „Intrauterine growth restriction: identification and management”. American Family Physician. 58 (2): 453—60, 466—7. PMID 9713399.
- ^ Rosenberg, A (2008). „The IUGR newborn”. Seminars in Perinatology. 32 (3): 219—24. PMID 18482625. doi:10.1053/j.semperi.2007.11.003.
- ^ Gonzalez, FF; Miller, SP (2006). „Does perinatal asphyxia impair cognitive function without cerebral palsy?”. Archives of Disease in Childhood: Fetal and Neonatal Edition. 91 (6): F454—9. PMC 2672766 . PMID 17056843. doi:10.1136/adc.2005.092445.
- ^ Habek, D; Habek, JC; Jugović, D; Salihagić, A (2002). „Intrauterine hypoxia and sudden infant death syndrome”. Acta Medica Croatica : Casopis Hravatske Akademije Medicinskih Znanosti. 56 (3): 109—18. PMID 12630342.
- ^ a b C. V. Ananth and A. M. Vintzileos, “Epidemiology of preterm birth and its clinical subtypes,” Journal of Maternal-Fetal and Neonatal Medicine, vol. 19, no. 12, pp. 773–782, 2006.
- ^ H. M. Beere and D. R. Green, “Stress management—heat shock protein-70 and the regulation of apoptosis,” Trends in Cell Biology, vol. 11, no. 1, pp. 6–10, 2001.
- ^ J. Jayakumar, K. Suzuki, I. A. Sammut et al., “Heat shock protein 70 gene transfection protects mitochondrial and ventricular function against ischemia-reperfusion injury,” Circulation, vol. 104, no. 12, supplement 1, pp. i303–i307,2001.
- ^ D. J. P. Barker, A. R. Bull, C. Osmond, and S. J. Simmonds, “Fetal and placental size and risk of hypertension in adult life,” British Medical Journal, vol. 301, no. 6746, pp. 259–262, 1990
- ^ J. E. Ramsay, F. Stewart, I. A. Greer, and N. Sattar, “Microvascular dysfunction: a link between pre-eclampsia and maternal coronary heart disease,” BJOG, vol. 110, no. 11, pp. 1029–1031, 2003.
- ^ B. J. Wilson, M. S. Watson, G. J. Prescott et al., “Hypertensive diseases of pregnancy and risk of hypertension and stroke in later life: results from cohort study,” British Medical Journal, vol. 326, no. 7394, pp. 845–849, 2003.
- ^ L. Haukkamaa, M. Salminen, H. Laivuori, H. Leinonen, V. Hiilesmaa, and R. Kaaja, “Risk for subsequent coronary artery disease after preeclampsia,” American Journal of Cardiology, vol. 93, no. 6, pp. 805–808, 2004.
- ^ D. J. P. Barker, “Growth in utero and coronary heart disease,” Nutrition Reviews, vol. 54, no. 2, pp. S1–S7, 1996. D. J. P. Barker, C. Osmond, J. Golding, D. Kuh, and M. E. J. Wadsworth, “Growth in utero, blood pressure in childhood and adult life, and mortality from cardiovascular disease,” British Medical Journal, vol. 298, no. 6673, pp. 564–567, 1989.
- ^ D. J. P. Barker, A. W. Shiell, M. E. Barker, and C. M. Law, “Growth in utero and blood pressure levels in the next generation,” Journal of Hypertension, vol. 18, no. 7, pp. 843–846, 2000.
- ^ E. A. Herrera, V. M. Pulgar, R. A. Riquelme et al., “Highaltitude chronic hypoxia during gestation and after birth modifies cardiovascular responses in newborn sheep,” American Journal of Physiology, vol. 292, no. 6, pp. R2234–R2240, 2007.
- ^ C. N. Martyn, D. J. P. Barker, S. Jespersen, S. Greenwald, C. Osmond, and C. Berry, “Growth in utero, adult blood pressure, and arterial compliance,” British Heart Journal, vol. 73, no. 2, pp. 116–121, 1995.
- ^ C. Sartori, Y. Allemann, L. Trueb, A. Delabays, P. Nicod, and U. Scherrer, “Augmented vasoreactivity in adult life associated with perinatal vascular insult,” The Lancet, vol. 353, no. 9171, pp. 2205–2207, 1999.
- ^ R. B. Ness and B. M. Sibai, “Shared and disparate components of the pathophysiologies of fetal growth restriction and preeclampsia,” American Journal of Obstetrics and Gynecology, vol. 195, no. 1, pp. 40–49, 2006.
- ^ J. G. Ray, M. J. Vermeulen, M. J. Schull, and D. A. Redelmeier, “Cardiovascular health after maternal placental syndromes (CHAMPS): population-based retrospective cohort study,” The Lancet, vol. 366, no. 9499, pp. 1797–1803, 2005
- ^ A. Y. Lausman, J. C. Kingdom, T. J. Bradley, C. Slorach, and J. G. Ray, “Subclinical atherosclerosis in association with elevated placental vascular resistance in early pregnancy,” Atherosclerosis, vol. 206, no. 1, pp. 33–35, 2009.
Spoljašnje veze uredi
| Klasifikacija |
|---|
| Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |