Solvatacija
Solvatacija je proces okruživanja čestice rastvorka česticama rastvarača. Pri tome su čestice rastvarača najčešće molekuli dok čestice rastvorka mogu biti molekuli, atomi ili joni.
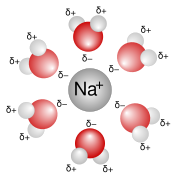
Hidratacija (od grč. hydor - voda) - nagomilavanje molekula vode oko rastvorka. Hidratacija je specijalni slučaj solvatacije.
Solvatacija je univerzalna pojava ali je najizrazitija kod veoma polarnih rastvarača, gde i rastvorak ima izražene polarne osobine ili poseduje jonsku vezu. Molekuli polarnog rastvarača tada grade dosta postojani omot (solvatacionu sferu, a kada je rasrtvarač voda, hidratacionu sferu) debljine do 4-5 molekula rastvarača oko čestice rastvorka. Kod brojnih hemijskih reakcija jona u vodenim rastvorima hidrataciona sfera predstavlja prepreku koja usporava reakciju.
Solvatacija je osnovni uzrok elektrolitičke disocijacije kod rastvora.
Prilikom solvatacije odigravaju se promene u energetskom sadržaju sistema (entalpije) kao i promene uređenosti sistema (entropije). Pre nego što je moguće da dođe do interakcije čestica rastvorka i rastvarača, potrebno je da dođe do raskidanja međumolekulskih veza između njih. Ovaj proces je endoterman ali se uravnotežuje sa stvaranjem novih intermolekulskih veza između rastvorka i rastvarača, što je egzoterman proces. Neto promena energije je u opštem slučaju mala (mada ima ekstremnih izuzetaka) i može da ima kako endo- tako i egzoterman karakter. Endotermne spontane solvatacije objašnjavaju se promanama entropije. Naime, povećanje neuređenosti sistema favorizuje rastvaranje.
Vidi još
urediLiteratura
uredi- Dogonadze, Revaz R.; et al., ur. (1985—88). The Chemical Physics of Solvation (3 vols. izd.). Amsterdam: Elsevier. Proverite vrednost paramet(a)ra za datum:
|date=(pomoć) ISBN 978-0-444-42551-5 (part A), ISBN 978-0-444-42674-1 (part B), ISBN 978-0-444-42984-1 (Chemistry) - Jiang D., Urakawa A., Yulikov M., Mallat T., Jeschke G. & Baiker A., „Size selectivity of a copper metal-organic framework and origin of catalytic activity in epoxide alcoholysis,”. Chemistry. 15 (45): 12255—62. 2009. doi:10.1002/chem.200901510.,. [One example of a solvated MOF, where partial dissolution is described.]
Dodatna literatura
uredi- Holtzer, Alfred; Emerson, Marilyn F. (1969). „Utility of the concept of water structure in the rationalization of the properties of aqueous solutions of proteins and small molecules”. The Journal of Physical Chemistry. 73: 26—33. doi:10.1021/j100721a005.
Spoljašnje veze
uredi- IUPAC Arhivirano na sajtu Wayback Machine (4. mart 2016)
- Transaction Faraday Society