Leukemija vlasastih ćelija
Leukemija vlasastih ćelija (akronim LVĆ) ili triholeukemija (MKB 10 C91.4 Leukaemia "hairy-cell"[1] ) je podtip hronične mijeloidne leukemije ili maligne bolesti krvi i koštane srži, u kojoj koštana srž stvara previše B ćelija (limfocita), vrste belih krvnih zrnaca koja se bore protiv infekcije. Ovaj višak abnormalnih B ćelija pod mikroskopom izgleda "vlasasto". Kako se broj ćelija leukemije povećava, proizvodi se manje zdravih belih i crvenih krvnih zrnaca i trombocita (krvnih pločica).
| Leukemija vlasastih ćelija | |
|---|---|
| Sinonimi | Hairy cell leukemia |
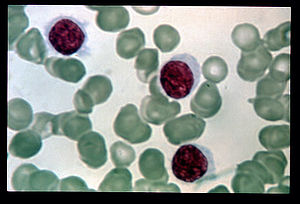 | |
| Razmaz krvi kod leukemija vlasastih ćelija | |
| Specijalnosti | hematologija, onkologija |
Leukemija vlasastih ćelija pogađa više muškarace nego žena, a najčešće se javlja kod odraslih osoba srednjih ili starijih godina.
Etiologija bolesti je nepoznata. Postoje podaci o povezanosti LVĆ sa jonizujućim zračenjem. Dok se porodična predispozicija pretpostavlja na osnovu prikaza u literaturi pojave bolesti u oca i sina, majke i sina, majke i ćerke i tri siblinga sa istim haplotipom Al, B7.
Leukemija vlasastih ćelija smatra se hroničnom bolešću jer možda nikada neće potpuno nestati, iako lečenje može dovesti do remisije bolesti koja može da traje godinama.[2]
Anatomija kostiju
uredi- Kompaktne kosti, koja formira spoljašnji sloj kosti.
- Sunđeraste kosti, koja se nalazi uglavnom na krajevima kostiju i sadrži crvenu koštanu srž.
- Koštane srži, koja se nalazi u centru većine kostiju i ima mnogo krvnih sudova. Postoje dve vrste koštane srži: crvena (koja sadrži krvne matične ćelije koje mogu postati crvena krvna zrnca, bela krvna zrnca ili trombociti) i žuts koja s uglavnom sastoji od masti.
Normalno, koštana srž se sastoji od matičnih krvnih ćelija (nezrele ćelije) koje vremenom postaju zrele krvne ćelije. Matična ćelija krvi mogu postati:
Mijeloidne matične ćelije - stvaraju jednu od tri vrste zrelih krvnih zrnaca:
- Crvena krvna zrnca - koja prenose kiseonik i druge supstance u sva tkiva u telu.
- Trombocite - koji formiraju krvne ugruške da bi zaustavili krvarenje.
- Granulocite (bela krvna zrnca) koji se bore protiv infekcija i bolesti.
Limfoidne matične ćelije - od koje postaje limfoblastna ćelija, a zatim jedna od tri vrste limfocita (belih krvnih zrnaca):
- B limfociti koji proizvode antitela koja pomažu u borbi protiv infekcije.
- T limfociti koji pomažu B limfocitima da proizvode antitela koja pomažu u borbi protiv infekcije.
- Prirodne ćelije ubice koje napadaju ćelije raka i viruse.
Etiopatogeneza
urediLeukemija može uticati na crvena krvna zrnca, bela krvna zrnca i trombocite. Kod leukemije vlasastih ćelija, veliki broj matičnih ćelija postaju limfociti (vrsta belih krvnih ćelija, koje se nazivaju i leukemične ćelije). Ove leukemične ćelije koje se ne mogu se dobro boriti protiv infekcije, zbog velikog broja koji neprestano raste u krvi i koštanoj srži, utiču na sve manji prostor za zdrave bele i crvene krvne ćelije i trombocite. To može rezultovati infekcijom, anemijom i lakšim oblicima krvarenja. Neke stanice leukemije mogu se sakupljati u sleženi i izazvati njeno povećanje.
Klasifikacija
urediKada se posebno ne navodi, „klasični“ oblik leukemije vlasastih ćelija se često podrazumeva kao primarni, ali su pored njega opisane i dve varijante:
- Varijanta leukemije vlasastih ćelija, koju teže lečiti nego bilo koju drugu varijantu.
- Japanska varijanta leukemija vlasastih ćelija
Varijanta leukemije vlasastih ćelija (LVĆ-V)
urediVarijanta leukemije vlasastih ćelija (LVĆ-V) je neuobičajen poremećaj, koji čini približno 0,4% hroničnih limfoidnih maligniteta i 10% svih slučajeva leukemije vlasastih ćelija. Dok klasični leukemije vlasastih ćelija prvenstveno pogađa muškarce, kod LVĆ-V dominacije polova ne postoji.[5][6][7][8]
Varijantna leukemije vlasastih ćelija (LVĆ-V) se obično opisuje i kao prolimfocitna varijanta leukemije vlasastih ćelija.[9] Prvi put je zvanično opisan 1980. godine u laboratoriji Hejho Univerziteta u Kembridžu.[10] Ovaj varijantni oblik leukemije vlasastih ćelija, predstavlja oko 60-75 novih slučajeva HCL-V svake godine u Sjedinjenim Američkim Državama. Iako se bolest može pojaviti u bilo kom uzrastu, srednja starost pri postavljanju dijagnoze je preko 70 godina.[11]
Slično B-ćelijskoj prolimfocitnoj leukemiji (B-PLL) kod hronične limfocitne leukemije, LVĆ-V je agresivnija bolest. Istorijski gledano, smatralo se da je manje verovatno da će se uspešno lečiti nego klasični oblik leukemije vlasastih ćelija, a remisije su bile kraće. Međutim, uvođenje kombinovane terapije sa istovremenom terapijom rituksimabom i kladribinom je pokazalo odlične rezultate u ranom praćenju.[12] Od 2016. godine, ova terapija se smatra tretmanom prve linije izbora za mnoge ljude sa LVĆ-V.
Mnogi stariji pristupi lečenju, kao što su interferon-alfa, kombinovani režim hemoterapije „CHOP“, i uobičajeni agensi za alkilovanje kao što je ciklofosfamid, pokazali su vrlo malu korist.[5] Pentostatin i kladribin koji se primenjuju kao monoterapija (bez istovremenog rituksimaba) pružaju izvesnu korist mnogim ljudima sa LVĆ-V, ali obično izazivaju kraće periode remisije i niže stope odgovora nego kada se koriste u klasičnol leukemiji vlasastih ćelija. Više od polovine ljudi delimično reaguje na splenektomiju.[5]
Što se tiče razvoja B-ćelija, prolimfociti su manje razvijeni od limfocita ili plazma ćelija, ali su i dalje zreliji od svojih limfoblastnih prekursora.
LVĆ-V se razlikuje od klasične leukemije vlasastih ćelija uglavnom u ovim aspektima:
- Veći broj belih krvnih zrnaca, ponekad prelazi 100.000 ćelija po mikrolitru
- Agresivniji tok bolesti koji zahteva češće lečenje
- Vlasaste ćelije sa neobično velikim nukleolom za njihovu veličinu
- Proizvodnja malog viška fibronektina koji proizvode klasične llasaste ćelije da bi ometale biopsiju koštane srži.[13]
- Niska ili nikakva ekspresija CD25 na ćelijskoj površini (alfa lanac interleukina-2 [IL-2] receptora, ili p55).[14]
Nizak nivo CD25, deo receptora za ključni imunoregulacioni hormon, može objasniti zašto su HCL-V slučajevi generalno mnogo otporniji na lečenje hormonima imunog sistema.[9]
LVĆ-V koji obično ima visok udeo vlasastih ćelija bez funkcionalnog gena za supresiju tumora p53, je nešto verovatnije da će se transformisati u malignitet višeg stepena. U Velikoj Britaniji je pretpostavljena tipična stopa transformacije od 5-6%, slična Rihterovoj stopi transformacije za SLVL i CLL.[15] Među pacijentima sa LVĆ-V, najagresivniji slučajevi obično imaju najmanju količinu aktivnosti gena p53.[16] Vlasaste ćelije bez gena p53 imaju tendenciju, tokom vremena, da zamene manje agresivne p53(+) dlakave ćelije.
Neki dokazi sugerišu da preuređenje imunoglobulinskog gena VH4-34, koje se nalazi kod oko 40% pacijenata sa LVĆ-V i 10% pacijenata sa klasičnim oblikom leukemije vlasastih ćelija, može biti važniji kao loš prognostički faktor od varijantnog statusa, sa LVĆ-V pacijenti bez VH4-34 rearanžmana koji reaguju otprilike kao i klasični pacijenti sa leukemijom vlasastih ćelija.[17]
Leukemija vlasastih ćelija-japanska varijanta (LVĆ-J)
urediVarijanta koja se zove leukemija vlasastih ćelija - japanska varijanta, ili LVĆ-J, se lakši oblik bolesti koji se leči, uglavnom kladribinom.[18]
| LDĆ | LVĆ-V | |
|---|---|---|
| KOŠTANA SRŽ | ||
| Celularnost | ||
| Hipercelularni | 54% (44/82) | 43% (6/14) |
| Normocelularni | 18% (15/82) | 28,5% (4/14) |
| Hipocelularni | 28% (23/82) | 28,5% (4/14) |
| Obrazac infiltracije | ||
| međuprostorni | 24% (20/82) | 50% (7/14) |
| intersticijalni sa agregatima | 21% (17/82) | 36% (5/14) |
| Listovi | 55% (45/82) | 14% (2/14) |
| Nivo infiltrata srži | ||
| 75–100% | 73% (60/82) | 21% (3/14) |
| 25–75% | 22% (18/82) | 50% (7/14) |
| Manje od 25% | 5% (4/82) | 29% (4/14) |
| Imunobojenje za TRAP | ||
| Pozitivno na TRAP | 95% (73/77) | 38% (5/13) |
| Negativno za TRAP | 5% (4/77) | 62% (8/13) |
| Rezidualna hematopoeza | ||
| Izrazito potisnuto | 63% (52/82) | 21% (3/14) |
| Prisutan | 37% (30/82) | 79% (11/14) |
| CITOMORFOLOGIJA | ||
| Citoplazmatske projekcije | ||
| Prisutan | 94% (67/71) | 96% (25/26) |
| Odsutan | 6% (4/71) | 4% (1/26) |
| Jedarni iblik | ||
| Serija | 77% (55/71) | 92% (24/26) |
| Atipična (u obliku bučice, nepravilna, žlebovi) | 23% (16/71) | 8% (2/26) |
| Nukleoli | ||
| Odsutan | 79% (56/71) | 0% (0/26) |
| Mala i neupadljiva | 20% (14/71) | 38% (10/26) |
| Istaknuti | 1% (1/71) | 62% (16/26) |
NAPOMENA: LVĆ: leukemija dlakavih ćelija, LVĆ-V: leukemija vlasastih ćelija-varijanta, N/A: nije dostupno.
Klinička slika
urediSimptomi leukemije vlasastih ćelija se razvijaju sporo i slični su onima kod drugih vrsta leukemije, i uključuju:
- nenamerni gubitak težine,
- bledu kožu,
- bol ili otok u trbuhu (abdomenu)
Većina kliničkih znakova bolesti je posledica citopenije i uvećanja slezine ili splenomegalije, koja nastaje kao posledica abnormalne akumulacije belih krvna zrnca u slezini, uzrokujući povećanje njene veličine. Ako je slezina uvećana, verovatno će bolesnik imati bolnu kvržicu na levoj strani trbuha. Uvećana slezina može ukloniti normalne krvne ćelije iz krvi bolesnika, što dovodi do daljeg smanjenja broja normalnih crvenih i belih krvnih zrnaca i trombocita u krvi. i prouzrokovati sledeče kliničke simptome:
- slabost, umor i nedostatak daha
- gubitak telesne težine, groznica i noćno znojenje, slično drugim limfoproliferativnim poremećajima,
- česte infekcije, koje su glavni problem i vodeći uzrok smrti pacijenata sa LVĆ. Ako je prisutna visoka temperatura, treba tražiti znake infekcije, jer se sama bolest ne manifestuje pojavom groznice. Oko 30% pacijenata se prvi put obraća lekaru zbog infekcija, a 70% pacijenata ima infekcije tokom bolesti. Leukemija vlasastih ćelija povezana je sa gram-pozitivnim i gram-negativnim bakterijskim infekcijama, kao i sa atipičnim mikobakterijskim i invazivnim gljivičnim infekcijama. Prijavljene su i druge oportunističke infekcije, kao što su legionela, toksoplazmoza i listerioza.
- hemoragični sindrom (lakše krvarenje ili modrice) izazvan trombocitopenijom, koji se javlja kod više od četvrtine pacijenata.
- multifaktorsku citopeniju koja je u zavisnosti od infiltracije koštane srži vlasastim limfoidnim ćelijama i fibroze srži, karakteriše smanjenom proizvodnjom hematopoetskih ćelija.
Leukemija vlasastih ćelija povezana je i sa drugim sistemskim imunološkim poremećajima uključujući sledeće:[20]
- skleroderma,
- polimiozitis,
- poliarteritis nodosa,
- eritematozne makulopapule,
- pioderma gangrenozum.
Druga neuobičajena stanja koja mogu biti povezana sa leukemijom vlasastih ćelija su:
* stečena antitela na faktor 8,
- paraproteinemija i
- sistemska bolest mastocita.
Dijagnoza
urediAko lekar opšte prakse posumnja na leukemiju, pacijenta šalje lekaru specijalizovanom za poremećaje krvi (hematologu) koji postavlja konačnu dijagnozu LVĆ na osnovu sledećih procedura:[21]
Fizički pregled i istorija bolesti
Fizički pregled proverava opšte znakove zdravlja, uključujući proveru znakova bolesti, kao što je infekcija ili bilo šta drugo što izgleda neobično. Takođe će se ispitati istorijat zdravstvenih navika pacijenata, prošlih bolesti i lečenja.[22]
Kompletna krvna slika (CC) sa diferencijalnom krvnom slikom (DC)
U ovoj proceduri nakon što se uzima uzorak krvi u apruvetu umetanjem igle u venu, u laboratoriji se proverava sledeće:[22]
- broj crvenih krvnih zrnaca
- broj trombocita (krvnih pločica)
- broj i vrsta belih krvnih zrnaca
- količina hemoglobina (proteina koji nosi kiseonik) u crvenim krvnim zrncima
- deo crvenih krvnih zrnaca u ukupnoj zapremini krvi
Biohemijski testovi krvi
Ovim testovima se proverava uzorak krvi kako bi se izmerila količina određenih supstanci koje organi i tkiva u telu oslobađaju u krv. Neuobičajene (više ili manje od normalne) količine ove supstance mogu biti znak bolesti.[22]
Bris periferne krvi
Brisom se proverava uzorak krvi na blastne ćelije, broj i tipove belih krvnih zrnaca, broj trombocita i promene u obliku, veličini i broju krvnih zrnaca.
Aspiracija i biopsija koštane srži
Nakon ubacivanja šuplje igle u karlicu ili grudnu kost, uzima se uzorka koštane srži, krv i maligni komada kosti Ovj uzorak ispituje patolog pod mikroskopom tražeći abnormalne ćelije.
Ostali testovi koji se mogu obaviti na uzorcima krvi ili koštane srži dobijenim biopsijom koštane srži su:
- Citogenetska analiza - laboratorijski test u kome se ćelije u uzorku krvi ili koštane srži posmatraju pod mikroskopom kako bi se utvrdilo da li postoje određene promene u hromozomima limfocita. Na primer, u ALL pozitivnom na hromozom u Filadelfiji, deo jednog hromozoma prelazi na drugi hromozom.[22]
- Imunofenotipizacija - postupak koji se koristi za identifikaciju ćelija, na osnovu tipa antigena ili markera na površini ćelije. Ova procedura se koristi za dijagnozu ALL podtipa, upoređujući ćelije raka sa normalnim ćelijama imunog sistema.[22]
- Protočna citometrija - laboratorijski test koji meri broj ćelija u uzorku, procenat živih ćelija u uzorku i određene karakteristike ćelija, kao što su veličina, oblik i prisustvo tumorskih markera na površini ćelije. Ćelije su obojene bojom osetljivom na svetlost. Osvetljene su laserskom svetlošću, a stepen rasejanja svetlosti iste talasne dužine je pokazatelj fizičkih osobina ćelija – veličina, veličina zrna... Merenja se zasnivaju na tome kako boja osetljiva na svetlost reaguje na svetlost.[22]
- Testiranje genskih mutacija - laboratorijski test koji se izvodi na uzorku koštane srži ili krvi da bi se proverile mutacije u BRAF genu. Mutacija BRAF gena se često nalazi kod pacijenata sa leukemijom vlasastih ćelija.[22]
CT skeniranje-kompjuterska tomografija
CT ili kompjuterizovanom aksijalnom tomografijom (CAT) pravi se serija detaljnih slika područja unutar tela, koja se snima iz različitih uglova. Snimljene slike se potom obrađuju uz pomoć računara povezanog sa rendgenskim aparatom. Pacijentu se takođe može dati kontrastno sredstvo ili „boja“ koja se može ubrizgati u venu ili progutati da bi organi ili tkiva bili jasniji.[23]
- Patohistološki prikaz leukemije vlasastih ćelija
-
Veliko uvećanje koštane srži pokazuje infiltraciju leukemijom vlasastih ćelija.
-
Leukemijom vlasastih ćelija
-
Mikrografija sa velikim uvećanjem leukemije vlasastih ćelija. H&E mrlja.
-
Mikrografija sa velikim uvećanjem leukemije vlasastih ćelija. H&E mrlja.
Dijagnostička razmatranja
urediLeukemija vlasastih ćelija (LVĆ) se mora razlikovati od drugih perifernih malih B-ćelijskih limfoidnih neoplazmi, uključujući:[24]
- varijantu leukemije vlasastih ćelija (LVĆ-V),[25]
- leukemiju vlasastih ćelija koju eksprimira IGHV4-34 i
- limfom difuzne crvene pulpe slezine (SDRPL).
Dok su te neoplazme histološki slične klasičnoj leukemija vlasastih ćelija, one imaju agresivniji klinički tok i manje je verovatno da će reagovati na terapiju analogom purina.[26]
Testiranje za BRAF-V600E omogućava diferencijalnu dijagnozu zasnovanu na genetici između tumora sličnih leukemiji vlasastih ćelija i leukemija vlasastih ćelija, pošto BRAF-V600E nema u drugim neoplazmama B-ćelija.[27][28]
Drugi problemi koje treba uzeti u obzir u diferencijalnoj dijagnozi leukemije vlasastih ćelija uključuju sledeće:[29]
- Primarna mijelofibroza
- Hronična limfocitna leukemija
- Limfom niskog stepena
- mieloskleroza
- Pancitopenija i fibroza srži
- Prolimfocitna leukemija
- Limfom marginalne zone slezine
- Sistemska mastocitoza
Diferencijalne dijagnoze
uredi- Anemija
- aplastična anemija
- hronična limfocitna leukemija
- mijelodisplastični sindrom
- mijeloftična anemija
- mijeloproliferativna bolest
- primarna mijelofibroza
Terapija
urediKako se leukemija vlasastih ćelija razvija sporo, hitno lečenje možda neće biti potrebno, ali će redovni testove krvi biti neophodni kako bi se pratilo stanje bolesti i pacijenta.
Lečenje se može preporučiti ako se poveća broj abnormalnih belih krvnih zrnaca ili ako cu se razvili svi simptomi.
Konzervativna terapija
uredi- Biološka terapija ili imunoterapija
Biološka terapija je tretman koji imuni sistem pacijenta koristi u borbi protiv raka. Supstance proizvedene u telu ili napravljene u laboratoriji koriste se za poboljšanje, usmeravanje ili obnavljanje prirodne odbrane tela protiv raka. Ova vrsta lečenja raka koja se takođe naziva bioterapija ili imunoterapija, koristi interferon alfa koji se obično koristi za lečenje leukemije vlasastih ćelija.[30]
Ovom terapijom splenektomija je zamenjena rekombinantnim interferon (interferon 2a i interferon 2b), koji se primenjuje u dozi od 2 do 4 miliona jedinica/m2. Daje se subkutano, 3 do 7 puta nedeljno, a terapija obično traje oko 12 meseci.[30]
- Hemoterapija
Hemoterapija je glavni tretman leukemije vlasastih ćelija i obično je efikasna u uništavanju ćelija raka.[30]
Dve glavne vrste lekova za hemoterapiju koje se koriste su:[30]
- kladribin – daje se ili kao injekcija neposredno pod kožu, ili putem kapi direktno u venu (infuzija).[31]
- pentostatin – daje se kao injekcija direktno u venu (intravenozno) svake 2 nedelje.[32]
Od ova dva citostatika, 2-hlorodeoksiadenozin se češće koristi u infuziji u dozi od 0,1 mg CdA / m2 / dan tokom 7 dana.
Remisija se postiže kod oko 82% pacijenata.
Kako ovi lekovi mogu izazvati nuspojave, pacijentima se daje dodatna terapija npr. antiemetici.[30]
Hemoterapijski lekovi takođe mogu učiniti pacijenta ranjivijim na infekciju, pa se tokom hemoterapije mogu pojaviti znaci infekcije, praćeni pojavom visoke temperature.
- Ciljana terapija
Ciljana terapija je vrsta lečenja koja koristi lekove ili druge supstance za prepoznavanje i napad specifičnih ćelija raka bez oštećenja normalnih ćelija. Terapija monoklonskim antitelima je vrsta ciljane terapije koja se koristi kod leukemije vlasastih ćelija.[30]
Terapija monoklonskim antitelima je tretman raka koji koristi antitela napravljena u laboratoriji od jedne vrste ćelija imunskog sistema. Ova antitela mogu da identifikuju supstance na ćelijama raka, odnosno antigen kao specifična obeleživačka struktura na površini ćelije. Svako monoklonsko antitelo prepoznaje specifični antigen na ćeliji raka. Antitela se vezuju za antigen i ubijaju ćelije raka, blokirajući njihov rast ili širenje.[30]
Monoklonska antitela se daju infuzijom. Mogu se koristiti sami ili u kombinaciji sa drugim onkološkim lekovima ili zračenjem.
Monoklonsko antitelo pod nazivom rituksimab može se koristiti za određene pacijente sa leukemijom vlasastih ćelija. Rituksimab se ponekad može koristiti u kombinaciji sa hemoterapijom. Deluje tako što se vezuje za protein koji se nalazi na ćelijama leukemije, a imuni sistem zatim cilja i ubija ćelije.[30]
Hirurška terapija
urediSplenektomija je bila standardni tretman leukemije vlasastih ćelija do sredine 1980-ih. Ikako poboljšava pancitopeniju kod većine pacijenata, retko se postiće potpuna remisija LVĆ i to samo kod pacijenata koji imaju čisto slezinski oblik bolesti. Danas je splenektomija retko potrebna, i to samo ako dođe do rupture slezine, teške trombocitopenije kao posledica hipersplenizma i kod pacijenata sa enormno velikom slezinom koja stvara velike mehaničke smetnje pacijentu, kao što su nemogućnost savijanja, gušenja zbog kompresija na dijafragmi itd.[33]
Trenutne indikacije za uklanjanje slezine su:[30]
- jako uvećana i bolna slezina koja izaziva smetnje u svakodnevnom životu.
- uništavanje velikog broj crvenih krvnih zrnaca ili trombocita u slezini
- ako nije došlo da smanjenja veličina slezine nakon hemoterapije.
Neželjeni efekti lečenja LVĆ
urediHemoterapija ubija ćelije koje se brzo množe, kao što su leukemijske ćelije. Takođe uzrokuje oštećenje normalnih ćelija koje brzo rastu, uključujući ćelije kose i ćelije koje čine tkiva u ustima, crevima i koštanoj srži. Neželjeni efekti hemoterapije nastaju kao rezultat ovog oštećenja i uključuju:[34]
Efekte na koštanu srž
urediHemoterapija utiče na sposobnost koštane srži da proizvodi adekvatan broj krvnih zrnaca. Kao rezultat toga, vaša slika (broj belih krvnih zrnaca, trombocita i crvenih krvnih zrnaca koji cirkulišu u bolesnikovoj krvi) će generalno pasti u roku od nedelju dana lečenja. Dužina vremena koje je potrebno da se koštana srž i krvna slika oporave uglavnom zavisi od vrste hemoterapije koja se daje.[34]
Kada je broj trombocita veoma nizak (bolesnik je trombocitopeničan), javljaju se modrice i krvarenje. Za to vreme je korisno dapacijent izbegava oštre predmete u ustima, kao što su seckane kosti ili čips, jer mogu poseći desni. Korišćenje meke četkice za zube takođe pomaže u zaštiti desni. U mnogim slučajevima se daje transfuzija trombocita da bi se smanjio rizik od krvarenja dok se broj trombocita ne oporavi.[34]
Ako broj crvenih krvnih zrnaca i nivo hemoglobina padne, verovatno će bolesnik postati anemični. Kada je anemičnan, osećaće se umornije i letargičnije nego obično. Ako je nivo hemoglobina veoma nizak, lekar može propisati transfuziju krvi.[34]
Rizik od infekcije
urediObično se očekuje da od 10 do 14 dana nakon hemoterapije pacijent biva izloženi većem riziku od razvoja infekcije, jer je pacijent neutropenični, što znači da je njegov broj neutrofila nizak. Infekcije u periodu neutropenije mogu biti prilično ozbiljne i potrebno ih je lečiti antibioticima što je pre moguće.[34]
Mučnina i povraćanje
urediMučnina i povraćanje su često povezani sa hemoterapijom i nekim oblicima radioterapije. Međutim, danas su, zahvaljujući značajnim poboljšanjima lekova protiv bolesti (antiemetika), mučnina i povraćanje su generalno veoma dobro kontrolisani.[34]
Promene u ukusu i mirisu
urediI hemoterapija i terapija zračenjem mogu izazvati promene u čulu ukusa i mirisa. Ovo je obično privremeno, ali u nekim slučajevima traje i do nekoliko meseci.
Upala sluzokože
urediMukozitis ili upala sluznice usta, grla ili creva je uobičajena i neprijatna nuspojava hemoterapije i nekih oblika radioterapije. Obično počinje oko nedelju dana nakon završetka lečenja i nestaje kada se bolesnikova krvna slika oporavi, obično nekoliko nedelja kasnije.[34]
Promene creva
urediHemoterapija može prouzrokovati oštećenje sluznice crevnog zida. To može dovesti do grčeva, meteorizma, otoka stomaka i dijareje.
Gubitak kose
urediGubitak kose je vrlo česta nuspojava hemoterapije i nekih oblika radioterapije. Međutim, to je obično samo privremeno. Kosa počinje da opada u roku od nekoliko nedelja tretmana i ima tendenciju da ponovo raste tri do šest meseci kasnije. Izbegavanje upotrebe toplote ili hemikalija i samo korišćenje meke četke za kosu i blagog šampona za bebe može pomoći u smanjenju svraba i osetljivosti vlasišta koji se mogu javiti dok gubite kosu. Takođe treba izbegavati direktnu sunčevu svetlost na izloženoj glavi (nositi šešir) jer hemoterapija (i radioterapija) čini bolesnikovu kožu još ranjivijom na štetne efekte sunca (kao što su opekotine od sunca i rak kože).[34]
Umor
urediVećina bolesnika doživljava određeni stepen umora u danima i nedeljama nakon hemoterapije i radioterapije. Dosta odmora i malo laganih vežbi svakog dana mogu pomoći da se pacijent oseća bolje tokom ovog perioda. Važno je da sa bolesnik odmara kada ste umorni.
Plodnost
urediNeke vrste hemoterapije i radioterapije mogu izazvati privremeno ili trajno smanjenje plodnosti. Kod žena, neke vrste hemoterapije i radioterapije mogu izazvati različite stepene oštećenja normalnog funkcionisanja jajnika.[34]
Kod muškaraca, proizvodnja sperme može biti poremećena neko vreme, ali proizvodnja nove sperme može ponovo postati normalna u budućnosti. Postoje neke opcije za očuvanje plodnosti, ako je potrebno, dok se bolesnik leči od leukemije.[34]
Rana menopauza
urediNeki tretmani raka mogu uticati na normalno funkcionisanje jajnika. Ovo ponekad može dovesti do neplodnosti i početka menopauze ranije nego što se očekivalo, čak i u mladosti. Početak menopauze u ovim okolnostima može biti iznenadan i, razumljivo, veoma uznemirujući. Hormonske promene mogu dovesti do mnogih klasičnih simptoma menopauze. Neke žene tokom ovog perioda doživljavaju smanjen seksualni nagon, anksioznost, pa čak i simptome depresije.[34]
Prognoza
urediKao i kod većine vrsta raka krvi, izgledi za leukemiju vlasastih ćelija zavisiće od toga koliko je stanje napredovalo u vreme postavljanja dijagnoze i koliko dobro bolesnik reaguje na lečenje.[34]
Kako je leukemija vlasastih ćelija retka vrsta raka, teško je lekarima da tačno predvide kako će bolest dugoročno uticati na pojedince.[34]
Prema raspoloživim podacima bolesnici žive u proseku 4-5 godina. Bolesnici koji su na početku bolesti imali blago uvećanu slezinu žive nešto duže (do 10 godina). Najčešći uzrok smrti je infekcija.[33]
Izvori
uredi- ^ Međunarodna klasifikacija bolesti, revizija iz 1975., Knjiga 1. (Ženeva, Svetska zdravstvena organizacija, 1977, pp. xiii- xxiv.)
- ^ Ravandi F. Hairy cell leukemia. In: Hoffman R, Benz EJ, Silberstein LE, et al, eds. Hematology: Basic Principles and Practice. 7th ed. Philadelphia, PA: Elsevier; 2018:chap 78.
- ^ Hall, Arthur C.; Guyton, John E. (2005). Textbook of medical physiology (11th izd.). . Philadelphia: W.B. Saunders. ISBN 978-0-7216-0240-0.
- ^ „Medical gallery of Blausen Medical 2014”. WikiJournal of Medicine (na jeziku: engleski). 1 (2). 2014. doi:10.15347/wjm/2014.010 .
- ^ a b v Matutes, E.; Wotherspoon, A.; Brito-Babapulle, V.; Catovsky, D. (2001). „The natural history and clinico-pathological features of the variant form of hairy cell leukemia”. Leukemia. 15 (1): 184—186. PMID 11243388. S2CID 6609635. doi:10.1038/sj.leu.2401999.
- ^ Tetreault SA, Robbins BA, Saven A (1999). „Treatment of hairy cell leukemia-variant with cladribine”. Leuk Lymphoma. 35: 347—354..
- ^ Blasinska-Morawiec M, Robak T, Krykowski E,; et al. (1997). „Hairy cell leukemia-variant treated with 2-chlorodeoxyadenosine: a report of three cases”. Leuk Lymphoma. 25: 381—385..
- ^ Catovsky D, Matutes E. Splenic lymphoma with circulating villous lymphocytes/splenic marginal-zone lymphoma. Semin Hematol. 36: 148—154. 1999. Nedostaje ili je prazan parametar
|title=(pomoć) - ^ a b Sainati, L.; Matutes, E.; Mulligan, S.; De Oliveira, MP; Rani, S.; Lampert, IA; Catovsky, D. (1990). „A variant form of hairy cell leukemia resistant to alpha-interferon: Clinical and phenotypic characteristics of 17 patients”. Blood. 76 (1): 157—162. PMID 2364167. doi:10.1182/blood.V76.1.157.157..
- ^ Cawley, J.C.; Burns, G.F.; Hayhoe, F.G.J. (1980). „A chronic lymphoproliferative disorder with distinctive features: A distinct variant of hairy-cell leukaemia”. Leukemia Research. 4 (6): 547—559. PMID 7206776. doi:10.1016/0145-2126(80)90066-1..
- ^ Ya-In, Charin; Brandwein, Joseph; Pantalony, Dominic; Chang, Hong (2005). „Hairy Cell Leukemia Variant with Features of Intrasinusoidal Bone Marrow Involvement”. Archives of Pathology & Laboratory Medicine. 129 (3): 395—398. PMID 15737038. doi:10.5858/2005-129-395-HCLVWF..
- ^ Kreitman, Robert J.; Wilson, Wyndham; Calvo, Katherine R.; Arons, Evgeny; Roth, Laura; Sapolsky, Jeffrey; Zhou, Hong; Raffeld, Mark; Stetler-Stevenson, Maryalice (2013). „Cladribine with Immediate Rituximab for the Treatment of Patients with Variant Hairy Cell Leukemia”. Clinical Cancer Research. 19 (24): 6873—6881. PMC 3867590 . PMID 24277451. doi:10.1158/1078-0432.CCR-13-1752..
- ^ Burthem, J.; Cawley, JC (1994). „The bone marrow fibrosis of hairy-cell leukemia is caused by the synthesis and assembly of a fibronectin matrix by the hairy cells”. Blood. 83 (2): 497—504. PMID 8286747. doi:10.1182/blood.V83.2.497.497..
- ^ De Totero, D.; Tazzari, PL; Lauria, F.; Raspadori, D.; Di Celle, PF; Carbone, A.; Gobbi, M.; Foa, R. (1993). „Phenotypic analysis of hairy cell leukemia: "variant" cases express the interleukin-2 receptor beta chain, but not the alpha chain (CD25)”. Blood. 82 (2): 528—535. PMID 8329708. doi:10.1182/blood.V82.2.528.528..
- ^ Matutes, E.; Wotherspoon, A.; Catovsky, D. (2003). „The variant form of hairy-cell leukaemia”. Best Practice & Research Clinical Haematology. 16 (1): 41—56. PMID 12670464. doi:10.1016/S1521-6926(02)00086-5..
- ^ Vallianatou, Kalliopi; Brito-Babapulle, Vasantha; Matutes, Estela; Atkinson, Shayne; Catovsky, Daniel (1999). „P53 gene deletion and trisomy 12 in hairy cell leukemia and its variant”. Leukemia Research. 23 (11): 1041—1045. PMID 10576509. doi:10.1016/S0145-2126(99)00127-7..
- ^ Arons, Evgeny; Suntum, Tara; Stetler-Stevenson, Maryalice; Kreitman, Robert J. (2009). „VH4-34+ hairy cell leukemia, a new variant with poor prognosis despite standard therapy”. Blood. 114 (21): 4687—4695. PMC 2780305 . PMID 19745070. doi:10.1182/blood-2009-01-201731.
- ^ 宮崎, 睦子; 田口, 昭彦; 櫻木, 志津; 三谷, 紀之; 松田, 万幸; 篠原, 健次 (2004). „Cladribine投与が奏効したhairy cell leukeimia, Japanese variant”. 臨床血液. 45 (5): 405—407. PMID 15199752. doi:10.11406/rinketsu.45.405..
- ^ Shao, Haipeng; Calvo, Katherine R.; Grönborg, Marlene; Tembhare, Prashant R.; Kreitman, Robert J.; Stetler-Stevenson, Maryalice; Yuan, Constance M. (1. 4. 2013). „Distinguishing Hairy Cell Leukemia Variant from Hairy Cell Leukemia: Development and Validation of Diagnostic Criteria”. Leukemia Research. 37 (4): 401—409. ISSN 0145-2126. PMC 5575750 . PMID 23347903. doi:10.1016/j.leukres.2012.11.021.
- ^ „Hairy Cell Leukemia Clinical Presentation: History, Physical Examination”. emedicine.medscape.com. Pristupljeno 2022-02-19.
- ^ Wintrobe, Maxwell Myer (2004). John G. Greer; John Foerster, John N. Lukens, George M Rodgers, Frixos Paraskevas, ur. (11 izd.). Hagerstown, MD: Lippincott Williams & Wilkins. str. 2465—2466. ISBN 978-0-7817-3650-3. Nedostaje ili je prazan parametar
|title=(pomoć) - ^ a b v g d đ e „Diagnosis of Hairy Cell Leukemia In: Understanding Hairy Cell Leukemia”. Hairy Cell Leukemia Foundation (na jeziku: engleski). Pristupljeno 2022-02-24.
- ^ Nelson, Angela. „Diagnosis In: What Is Hairy Cell Leukemia?”. WebMD (na jeziku: engleski). Pristupljeno 2022-02-24.
- ^ „Hairy Cell Leukemia Diagnostic Considerations”. emedicine.medscape.com. Pristupljeno 2022-02-19.
- ^ Cross M, Dearden C (april 2020). „Hairy Cell Leukaemia.”. Curr Oncol Rep. 22 (5): 42..
- ^ Troussard X, Cornet E. Hairy cell leukemia 2018: Update on diagnosis, risk-stratification, and treatment. Am J Hematol. 92 (12): 1382—1390. decembar 2017. Nedostaje ili je prazan parametar
|title=(pomoć) - ^ Tiacci E, Pettirossi V, Schiavoni G, Falini B (mart 2017). „Genomics of Hairy Cell Leukemia”. J Clin Oncol. 35 (9): 1002—1010.
- ^ Swerdlow SH, Campo E, Pileri SA, Harris NL, Stein H, Siebert R; et al. (maj 2016). „The 2016 revision of the World Health Organization classification of lymphoid neoplasms”. Blood. 127 (20): 2375—90.
- ^ „Hairy Cell Leukemia Differential Diagnoses”. emedicine.medscape.com. Pristupljeno 2022-02-19.
- ^ a b v g d đ e ž z „Hairy cell leukemia treatment”. Leukaemia Foundation (na jeziku: engleski). Pristupljeno 2022-02-24.
- ^ a b Sigal DS, Miller HJ, Schram ED, Saven A: Beyond hairy cell: the activity of cladribine in other hematologic malignancies. Blood. 2010 Jul 15. PMID 20634380
- ^ Knox, C.; Law, V.; Jewison, T.; Liu, P.; Ly, S.; Frolkis, A.; Pon, A.; Banco, K.; Mak, C.; Neveu, V.; Djoumbou, Y.; Eisner, R.; Guo, A. C.; Wishart, D. S. (2011). „DrugBank 3.0: A comprehensive resource for 'omics' research on drugs”. Nucleic Acids Research. 39 (Database issue): D1035—41. PMC 3013709 . PMID 21059682. doi:10.1093/nar/gkq1126.
- ^ a b „Leukemija vlasastih ćelija (Hairy cell leukaemia, Tricholeukaemia) • LekarInfo 2021” (na jeziku: srpski). 2013-06-16. Pristupljeno 2022-02-19.
- ^ a b v g d đ e ž z i j k l „Side effects of hairy cell leukaemia treatment”. Leukaemia Foundation (na jeziku: engleski). Pristupljeno 2022-02-24.
Spoljašnje veze
uredi| Klasifikacija | |
|---|---|
| Spoljašnji resursi |
- About HCL at the US National Cancer Institute (jezik: engleski)
- History of HCL and the Godmother of HCL (jezik: engleski)
| Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |