Manganat
Manganat je jon MnO42−, i manganat je svako jedinjenje koje sadrži MnO42− grupu. Soli, kao što je kalijum manganat, su konjugovane baze hipotetične manganske kiseline, H2MnO4. Manganatne soli su intermedijari u industrijskoj sintezi kalijum permanganata. Ponekad se imena soli permanganata i manganata greškom poistovete. Ove dve grupe supstanci imaju različite osobine.
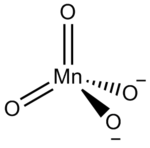
Struktura
уредиMnO42− je tetraedarska struktura koja je srodna sa drugim tetraedarskim oksidima kao što su permanganat i osmijum tetroksid. Sali jona MnO42−, SO42−, i CrO42− su obično izostrukturne ili približno tome, što znači da one mogu da formiraju mešavine, i da imaju sličnu rastvorljivost. Za razliku od sulfata i hromata, međutim, MnO42− je paramagnetičan.
Sinteza
уредиManganatni jon je stabilan u vodi samo u jako baznim uslovima. Konsekventno, soli se formiraju sa elektropozitivnim metalima, kao što su Na+, K+, i Ba2+ koji ne formiraju nerastvorne hidrokside. Manganati se mogu pripremiti oksidacijom MnO2 ili redukcijom permanganata. O2 je nedovoljno oksidirajući da dalje konvertuje Mn(VI) u Mn(VII). Mn(VI)/Mn(VII) oksidacija se izvodi koristeći jake oksidante kao što su O3 ili Cl2.
Reakcije
уредиMnO42− je konjugovana baza hipotetične manganske kiseline, H2MnO4, koja je suviše nestabilna da bi se izolovala. Polu-deprotonizirana kiselina je, međutim, bila ispitana. pKa vrednost jona HMnO4− je bila ustanovljena da je 7.1. MnO42− je oko 100 puta bazniji nego acetatni jon.[1] Na nižim pH vrednostima, manganatni jon se disproporcioniše i permanganati ion i mangan dioksid:
- 3 K2MnO4 → 2 KMnO4 + MnO2 + 4 KOH
Višebojna priroda ove reakcije je uzrokovala da se manganat/permanganat par naziva "hemijski kameleon." Ova disproporciona reakcija, koja postaje brza kad je [OH−
] < 1M, sledi bimolekulsku kinetiku.[2]
Permanganat, manganat, hipomanganit, i manganit
уредиGornja reakcija ilustruje blisku hemijsku srodnost između dva glavna rastvorna oksida mangana, permanganat i manganat. Dva druga, manje rasprostranjena člana serije su takođe poznata, vidi tabelu ispod. Hipomanganat, MnO43−, je plavo-obojeni jon Mn(V) koji se formira kad se MnO42− tretira sa manganitom MnO44− na pH>12. On je bio generisan tretmanom KMnO4 u 10M KOH sa H2O2. pKa HMnO42− je 13.7,[3] što indicira da rastvori hipomanganata sadrže značajne količine protonisane forme čak i u visokim pH uslovima. Oksidacije alkena permanganatom su predložene da se odvijaju putem posredovanja "estara" hipomanganata, drugim rečima putem intermedijara tipa MnO2(OR)2− gde je R alkilna grupa.[4] Smeđe-obojeni manganitni jon, Mn(IV), nastaje rastvaranjem anhidrida njegove kiseline MnO2 u jakim alkalijama. Alternativno, MnO44− može biti generisan MnO43− redukcijom.
| Ime | Formula | Mn oksidaciono stanje | Boja rastvora | Komentar |
|---|---|---|---|---|
| Permanganat | MnO4− | VII | ljubičast | dijamagnetičan, jak oksidant, mnoge soli |
| Manganat | MnO42− | VI | zelen | paramagnetičan, jak oksidant, mnoge soli |
| Hipomanganit | MnO43− | V | plav | paramagnetičan, retko se javlja, bazan |
| Manganit | MnO44− | IV | smeđ | paramagnetičan, retko se javlja, bazan |
Upotreba
уредиBaMnO4 i K2MnO4 se koriste za oksidaciju primarnih i sekundarnih alkohola. Primarni alkoholi se oksidišu u aldehide, a zatim u karboksilne kiseline. Sekundari alkoholi se oksidišu u ketone. Tercijarni alkoholi ne mogu biti oksidisani na ovaj način. Njihova upotreba je slična upotrebi Jonesovog reagensa.
Literatura
уреди- ^ Nyholm R.S.; Woolliams P.R. (1986). „"Manganates(VI)"”. Inorganic Syntheses. XI: 56—61.
- ^ Lee D.G. Chen T. (1993). „Reduction of Manganate(VI) by Mandelic Acid and Its Significance to Development of a General Mechanism for Oxidation of Organic Compounds by High-Valent Transition Metal Oxides”. Journal of the American Chemical Society. 115: 11231—11236. doi:10.1021/ja00077a023.
- ^ Rush J.D. Bielski B.H. (1995). „Studies of Manganate(V), -(VI), and -(VII) Tetraoxyanions by Pulse Radiolysis. Optical Spectra of Protonated Forms”. Inorg. Chem. 34: 5832—8. doi:10.1021/ic00127a022.
Dodatna literatura
уреди- ^ G. Procter, S. V. Ley, G. H. Castle “Barium Manganate” (2004). L. Paquette, ур. Encyclopedia of Reagents for Organic Synthesis. New York: J. Wiley & Sons. doi:10.1002/047084289.
- ^ Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 978-0-12-352651-9.