Estar
Estri (nem. Essig-Äther, što je stari naziv za etil-etanoat) organska su jedinjenja koja u svojim molekulima sadrže ostatak molekula kiseline i ostatak molekula alkohola.[1] Estri daju miris voću, povrću i četinarima. Njihova opšta formula je: CnH2n+1-COO-CnH2n+1. U hemiji, estar je funkcionalna grupa izvedena iz kiseline (organske ili neorganske) u kojoj je atom vodonika (H) najmanje jedne kisele hidroksilne grupe (−OH) te kiseline zamenjen organskom grupom (R′) . Analogi dobijeni od kiseonika zamenjenog drugim halkogenima takođe pripadaju kategoriji estara.[2] Prema nekim autorima, organski derivati kiselog vodonika drugih kiselina su takođe estri (npr. amidi), ali ne prema IUPAC.[2]

Estri dobijaju nazive u zavisnosti od toga koji je alkohol i koja kiselina izreagovala. Ako je recimo, reagovao etanol i etanska kiselina, dobija se estar koji se naziva etil-etanoat ili etil-acetat. Taj naziv je izveden od etil-grupe alkohola i naziva soli etanske kiseline. Soli etanske kiseline se nazivaju etanoati ili acetati.
- CH3-COOH + CH3-CH2-OH → CH3-COO-CH2-CH3 + H2O
Estri se dobijaju u reakciji esterifikacije. Ta se reakcija odvija u kiseloj sredini. Suprotna reakcija esterifikaciji je hidroliza. U toj reakciji se dobijena voda iz esterifikacije jedini sa estrom koji je dobijen i daje polazne supstance: alkohol i kiselinu.
- CH3-COO-CH2-CH3 + H2O → CH3-COOH + CH3-CH2-OH
Estri se koriste u prehrambenoj industriji za proizvodnju veštačkih mirisa, kao rastvarači boja, lakova i kao sirovina za dobijanje veštačkih vlakana. Jedan od najpoznatijih estara je nitroglicerin, koji se dobija reakcijom trovalentnog alkohola glicerola i azotne kiseline, uz prisustvo sumporne kiseline.[3][4][5]
Gliceridi su estri masnih kiselina i glicerola; oni su važni u biologiji, jer su jedna od glavnih klasa lipida i čine većinu životinjskih masti i biljnih ulja. Laktoni su ciklični karboksilni estri; Prirodni laktoni su uglavnom 5- i 6-člani laktoni u prstenu. Laktoni doprinose aromi voća, putera, sira, povrća poput celera i druge hrane.
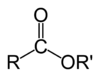
Estri se mogu formirati od oksokiselina (npr. estri sirćetne kiseline, ugljene kiseline, sumporne kiseline, fosforne kiseline, azotne kiseline, ksantične kiseline), ali i od kiselina koje ne sadrže kiseonik (npr. estri tiocijanske kiseline i tritiokarbonske kiseline). Primer formiranja estra je reakcija supstitucije između karboksilne kiseline (R−C(=O)−OH) i alkohola (R'−OH), formirajući estar (R−C(=O)−O−R'), gde R predstavlja bilo koju grupu (obično vodonik ili organil), a R′ označava organil grupu.
Organil estri karboksilnih kiselina obično imaju prijatan miris; oni male molekularne težine se obično koriste kao mirisi i nalaze se u eteričnim uljima i feromonima. Oni deluju kao rastvarači visokog kvaliteta za široku lepezu plastike, plastifikatora, smola i lakova,[6] i predstavljaju jednu od najvećih klasa sintetičkih maziva na komercijalnom tržištu.[7] Poliesteri su važne plastike, sa monomerima povezanim estarskim delovima. Estri fosforne kiseline čine kičmu molekula DNK. Estri azotne kiseline, kao što je nitroglicerin, poznati su po svojim eksplozivnim svojstvima.
Postoje jedinjenja u kojima kiseli vodonik kiselina navedenih u ovom članku nije zamenjen organilom, već nekom drugom grupom. Prema nekim autorima, ta jedinjenja su estri, posebno kada je prvi atom ugljenika organske grupe koja zamenjuje kiseli vodonik, zamenjen drugim atomom iz grupe 14 elemenata (Si, Ge, Sn, Pb); na primer, prema njima, trimetilstanil acetat (ili trimetilkalaj acetat) CH
3COOSn(CH
3)
3 je trimetilstanil estar sirćetne kiseline i dibutilkalaj dilaurat (CH
3(CH
2)
10COO)
2Sn((CH
2)
3CH
3)
2 je dibutilstanilenski estar laurinske kiseline, a Filipsov katalizator CrO
2(OSi(OCH
3)
3)
2 je trimetoksisilil estar hromne kiseline (H
2CrO
4).[8][9]
Imenovanje
уредиImenovanje estera se bazira na nazivu alkohola koji je stupio u reakciju tj. prvo ide naziv alkilne skupine alkohola (npr. naziv alkilne skupine propanola je propil). Drugim riječima, umjesto uobičajenog završetka -anol na osnovu imena alkohola doda se nastavak -il. Druga riječ u nazivu estera potiče od kiseline, a tvori se tako da se imenu kiseline oduzme nastavak -ska i doda nastavak -oat (npr., druga riječ u imenu estera butanske kiseline bila bi butanoat). Kod estera sa etanskom kiselinom, često se umjesto etanoata upotrebljava: acetat, kod onih sa metanskom kiselinom: formijat, kod estera sa butanskom kiselinom: butirat, a kod propanske kiseline: propionat. Kod alkohola također postoje drugi nazivi pa se tako umjesto pentil, često nađe i amil: alkohol (-ol → -il) + karboksilne kiseline (-ska → -oat)
Etimologija
уредиReč estar je 1848. skovao nemački hemičar Leopold Gmelin,[10] verovatno kao kontrakciju nemačkog Essigäther, „sirćetni etar“.
IUPAC-ova nomenklatura
уредиEsterska imena izvedena su iz naziva matičnog alkohola i roditeljske kiseline, gde ova može biti organska ili neorganska. Estri izvedeni iz najjednostavnijih karboksilnih kiselina se obično zove prema tradicijskim, takozvanim trivijalnim nazivima, npr. kao format, acetat, propionat, i butirat, za razliku od IUPAC-ove nomenklature: metanoat, etanoat, propanoat i butanoat. Estri izvedeni iz kompleksnijih karboksilnih kiselina su, s druge strane, češće pod nazivom koji koristi sistematski naziv po IUPAC-u, na osnovu imena za kiselinu zatim dolazi sufiks –oat. Na primer, ester-heksiloktanoat, poznat i pod trivijalnim imenom heksil-kaprilat, ima formulu CH3(CH2)6CO2(CH2)5CH3.
Hemijske formule organskih estera obično imaju oblik RCO2R', gde su R i R' delovi ugljikovodika iz karboksilne kiseline i alkohola. Na primer, butil acetat (sistematski butil-etanoat), izveden iz butanola i acetatne kiseline (sistematski etanska kiselina) se piše kao CH3CO2C4H9. Alternativno prikazivanje obično uključuje BuOAc i CH3COOC4H9. Ciklični estri se zovu laktoni, bez obzira na to da li su izvedeni iz organske ili neorganske kiseline. Jedan primer (organskog) laktona je γ-valerolakton.
Ortoestri
уредиNeuobičajena klasa organskih estera su ortoesteri, koji imaju formulu RC(OR′)3. Trietilortoformat (HC(OC2H5)3) je izvedenica, u smislu imena (ali ne i sinteze) iz ortomravlje kiseline (HC(OH)3) i etanola.
Neorganski estri
уредиEsteri mogu takođe da budu izvedeni iz neorganskih kiselina i alkohola. Dakle, nomenklatura se proteže na neorganske oksokiseline i njihove odgovarajuće estre: fosforna kiselina i fosfatni ester/organofosfati, sumporna kiselina i sulfatni ester/organosulfati, azotna kiselina i nitrat, borna kiselina i borati. Na primer, trifenil fosfat je ester izveden iz fosforne kiseline i fenola. Organski karbonati su izvedeni iz ugljene kiseline; na primer, etilen karbonat je izveden iz ugljene kiseline i etilen glikola.
Alkohol i neorganska kiselina povezivani su preko atoma kiseonika. Definicija estera neorganske kiseline koji imaju vezu neorganskih hemijskih elemenata između alkohola i neorganske kiseline – vezanje atoma fosfor i tri alkoksi funkcionalne grupe u organofosfatima – može se proširiti na iste elemente u raznim kombinacijama kovalentne veze između ugljenikovih i centralnog neorganskog atoma i vezi ugljenik-kiseonik, sa centralnim neorganski atomima. Na primer, fosforna svojstva tri veze ugljenik-kiseonik-fosfor i jednu dvostruku vezu fosfor-kiseonik u organofosfatima, tri veze ugljenik–kiseonik–fosfor i nijednu dvostruku vezu fosfor–kiseonik u fosfitni esterima ili organofosfitima, dve veze ugljenik–kiseonik–fosfor, nijedna fosfor–kiseonik dvostruka veza, ali jedna veza fosfor–ugljenik u fosfonitima, jedna veza ugljenik–kiseonik–fosfor, nijedna dvostruka veza fosfor–kiseonik, ali dve veze fosfor–ugljenik u fosfonitima.
Kao posledica, funkcije bora je stvaranje bornih estara (n = 2), boronskih estara (n = 1) i borata (n = 0). Kiseonik je hemijski element grupe 16, a atomi sumpora mogu zameniti neke atome kiseonika u ugljenik–kiseonik centralnom neorganskom atomu kovalentnih veza estera. Kao rezultat, stvaraju se tiosulfinati i tiosulfonati, sa centralnin neorganskim atomom sumpora, jasno pokazujući asortiman sumpornih estera, koji uključuju i sulfatne, sulfitne, sulfonatne, sulfinatne i sulfenatne estere.
Estri se takođe mogu dobiti iz neorganskih kiselina.
- Perhlorna kiselina formira perhloratne estre, na primer, metil perhlorat (CH
3−O−Cl(=O)
3) - Sumporna kiselina formira sulfatne estre, na primer, dimetil sulfat ((CH
3−O−)
2S(=O)
2) i metil bisulfat (CH
3−O−S(=O)
2−OH) - Azotna kiselina formira nitratne estre, npr. metil nitrat (CH
3−O−NO
2) i nitroglicerin (CH(−O−NO
2)(−CH
2−O−NO
2)
2) - Fosforna kiselina formira fosfatne estre, npr. trifenil fosfat (O=P(−O−C
6H
5)
3) i [[[methyl dihydrogen phosphate|metil dihidrogen fosfat]] (O=P(−O−CH
3)(−OH)
2)- Pirofosforna (difosforna) kiselina formira pirofosfatne estre, npr. tetraetil pirofosfat, ADP, dADP, ADPR, cADPR, CDP, dCDP, GDP, dGDP, UDP, dTDP, MEcPP, HMBPP, DMAPP, IPP, GPP, FPP, GGPP, ThDP, FAD, NAD, NADP.
- Trifosforna kiselina formira trifosfatne estre, npr. ATP, dATP, CTP, dCTP, GTP, dGTP, UTP, dTTP, ITP, XTP, ThTP, AThTP.
- Ugljena kiselina formira karbonatne estre, npr. dimetil karbonat ((CH
3−O−)
2C=O) i petočlani ciklični etilen karbonat ((−CH
2−O−)
2C=O) (ako se ugljena kiselina klasifikuje kao neorgansko jedinjenje) - Tritiokarbonska kiselina formira tritiokarbonatne estre, npr. dimetil tritiokarbonat ((CH
3−S−)
2C=S) (ako se tritiokarbonska kiselina klasifikuje kao neorgansko jedinjenje) - Hloromravlja kiselina formira hloroformatne estre, npr. metil hloroformijat (Cl−C(=O)−O−CH
3) (ako se hloromravlja kiselina klasifikuje kao neorgansko jedinjenje) - Borna kiselina formira boratne estre, npr. trimetil borat (B(−O−CH
3)
3) - Hromna kiselina formira di-terc-butil hromat (((CH
3)
3C−O−)
2Cr(=O)
2)
Neorganske kiseline koje postoje kao tautomeri formiraju dve ili više vrsta estara.
- Tiosumporna kiselina formira dve vrste tiosulfatnih estara, npr. O,O-dimetil tiosulfat ((CH
3−O−)
2S(=O)(=S)) i O,S-dimetil tiosulfat ((CH
3−O−)(CH
3−S−)S(=O)
2) - Tiocijanska kiselina formira tiocijanatne estre, npr. metil tiocijanat (CH
3−S−C≡N) (ako se tiocijanska kiselina klasifikuje kao neorgansko jedinjenje), ali formira i izotiocijanatne „estre“, npr. metil izotiocijanat (CH
3−N=C=S), iako IUPAC ne klasifikuje organil izotiocijanate kao estre - Fosforna kiselina formira dve vrste estara: fosfitne estre, npr. trietil fosfit (P(−O−CH
2CH
3)
3), i fosfonatne estre, npr. dietil fosfonat (H−P(=O)(−O−CH
2CH
3)
2)
Neke neorganske kiseline koje su nestabilne ili neuhvatljive formiraju stabilne estre.
- Sumporna kiselina, koja je nestabilna, formira stabilan dimetil sulfit ((CH
3−O−)
2S=O) - Dikarbonska kiselina, koja je nestabilna, formira stabilan dimetil dikarbonat (CH
3−O−C(=O)−O−C(=O)−O−CH
3)
U principu, deo metalnih i metaloidnih alkoksida, kojih je poznato na stotine, mogao bi se klasifikovati kao estri odgovarajućih kiselina (npr. aluminijum trietoksid (Al(OCH
2CH
3)
3 može se klasifikovati kao estar aluminijumske kiseline koji je aluminijum hidroksid, tetraetil ortosilikat (Si(OCH
2CH
3)
4) može se klasifikovati kao estar ortosilicijumske kiseline i titanijum etoksid (Ti(OCH
2CH
3)
4) može se klasifikovati kao estar ortotitanske kiseline).
Struktura i vezivanje
уредиEstri sadrže karbonilni centar, koji ima strukturne motive C-C-O i O-C-O sa uglovima između veza od 120°. Za razliku od amida, estri su strukturno fleksibilne funkcionalne grupe jer rotacija oko C-O-C veza ima nisku barijeru. Njihova fleksibilnost i niska polarnost se manifestuje u njihovim fizičkim osobinama. Oni su manje rigidni (imaju nižu tačku topljenja) i isparljiviji su (niža tačka ključanja) od odgovarajućih amida.[12] pKa vrednosti alfa-vodonika estera je oko 25.[13]
Mnogi estri karboksilne kiseline imaju potencijal za konformacioni izomerizam, ali imaju tendenciju da poprime S-cis (ili Z) konformaciju pre nego S-trans (ili E) alternativu, zbog kombinacije efekata hiperkonjugacije i minimizacije dipola. Na preferenciju Z konformacije utiče priroda supstituenata i rastvarača, ako je prisutan.[14][15] Laktoni sa malim prstenovima su ograničeni na s-trans (tj. E) konformaciju zbog svoje ciklične strukture.
Fizička svojstva i karakterizacija
уредиEstri dobijeni od karboksilnih kiselina i alkohola su polarniji od etara, ali manje polarni od alkohola. Oni učestvuju u vodoničnim vezama kao akceptori vodonične veze, ali ne mogu delovati kao donori vodonične veze, za razliku od svojih matičnih alkohola. Ova sposobnost da učestvuju u vezivanju vodonika daje izvesnu rastvorljivost u vodi. Zbog nedostatka sposobnosti doniranja vodonične veze, estri se ne povezuju sami. Shodno tome, estri su isparljiviji od karboksilnih kiselina slične molekulske težine.[12]
Karakterizacija i analiza
уредиEstri se generalno identifikuju gasnom hromatografijom, koristeći prednost njihove isparljivosti. IR spektri za estre karakterišu intenzivnu oštru traku u opsegu 1730–1750 cm−1 koja je dodeljena νC=O. Ovaj pik se menja u zavisnosti od funkcionalnih grupa vezanih za karbonil. Na primer, benzenski prsten ili dvostruka veza u sprezi sa karbonilom će smanjiti talasni broj za oko 30 cm−1.
Triacilglicerol
уредиTriacilgliceroli (masti i ulja) su estri koji sadrže tri hidroksilne grupe. Imenuju se slično kao i soli. Nerastvorni su ili slabo rastvorni u vodi (lipidi).
Estri se mogu dobiti reakcijom, obično organskih, kiselina i alkohola, uz katalitsko prisustvo sumporne kiseline, iako ima i drugih načina dobijanja estera. Esterifikacija je reverzibilna reakcija u kojoj se istovremeno događa i hidroliza, pa je potrebno higroskopno sredstvo koje reakciji oduzima vodu.
- Alkoholi + karboksilne kiseline ↔ ester + voda (esterifikacija)
- Ester + voda ↔ alkoholi + karboksilne kiseline (hidroliza)
Mnogi estri imaju specifičan miris, zbog čega se često koriste kao veštačke arome i u proizvodnji mirisa. Na primer:
Metil formijat
уредиMetil metanoat je bezbojna tečnost karakterističnog eterskog mirisa, lako ispariva, sa malim površinskim naponom.
- C2H4O2O=COC
Etil acetat / etil etanoat
уредиOvo je bezbojna, lako zapaljiva tečnost karakterističnog mirisa, poput lepka ili sredstava za skidanje laka za nokte (C4H8O2, CC(=O)OCC ili CH3COOCH2CH3). Etil acetat je zapaljiv i kožni iritant.
Upotreba
уредиEstri se između ostalog koriste:
- kao otrov za ubijanje insekata (za prepariranje u entomologiji: insekt se ubije, ali se ne uništi)
- u lepkovima i odstranjivačima laka za nokte
- kao reagens za određivanje angiotenzin konvertirajućeg enzima (ACE)
Estri se obično upotrebljavaju u prehrambenoj i konditorskoj industriji, proizvodnji rastvarača i plastičnih masa, i proizvodnju parfema. Upotrebljava se i kao insekticid i u proizvodnji nekih lekova.
Estri su rasprostranjeni u prirodi i široko se koriste u industriji. U prirodi, masti su, generalno, triestri dobijeni od glicerola i masnih kiselina.[16] Estri su odgovorni za aromu mnogih voća, uključujući jabuke, durijane, kruške, banane, ananas i jagode.[17] Godišnje se industrijski proizvodi nekoliko milijardi kilograma poliestera, a važni proizvodi su polietilen tereftalat,[18] akrilatni estri[19] i acetat celuloze.[20]
Dobijanje estera
уредиEsteri se dobijaju pri sintezi sirćetne kiseline i etanola, uz prisustvo jakih kiselina kao što je sumporna kiselina.
- CH3CH2OH + CH3COOH → CH3COOCH2CH3 + H2O
Dobijaju se:
- esterifikacijom metanola i etanoata: HCOOH + CH3OH → HCOOCH3 + H2O
- industrijski kombinacijom metanola i ugljen monoksida: CH3OH + CO → HCOOCH3.
Esterifikacija je opšti naziv za hemijsku reakciju u kojoj dva reaktanta (obično alkohol i kiselina) formiraju estar kao proizvod reakcije. Estri su uobičajeni u organskoj hemiji i biološkim materijalima i često imaju prijatan karakterističan, voćni miris. To dovodi do njihove široke upotrebe u industriji mirisa i ukusa. Estarske veze se takođe nalaze u mnogim polimerima.
Esterifikacija karboksilnih kiselina alkoholima
уредиKlasična sinteza je Fišerova esterifikacija, koja uključuje tretiranje karboksilne kiseline alkoholom u prisustvu agensa za dehidrataciju:
- RCO
2H + R'OH ⇌ RCO
2R' + H
2O
Konstanta ravnoteže za takve reakcije je oko 5 za tipične estre, na primer, etil acetat.[21] Reakcija je spora u odsustvu katalizatora. Sumporna kiselina je tipičan katalizator ove reakcije. Koriste se i mnoge druge kiseline kao što su polimerne sulfonske kiseline. Pošto je esterifikacija veoma reverzibilna, prinos estra se može poboljšati korišćenjem Le Šateljeovog principa:[22][23][24][25][26]
- Korišćenje alkohola u velikom višku (tj. kao rastvarača).
- Korišćenje sredstva za dehidrataciju: sumporna kiselina ne samo da katalizuje reakciju, već sekvestrira vodu (proizvod reakcije). Druga sredstva za sušenje kao što su molekularna sita[27][28][29] su takođe efikasna.
- Uklanjanje vode fizičkim sredstvima kao što je destilacija kao azeotrop niske tačke ključanja sa toluenom, u kombinaciji sa Dean-Starkovim aparatom.[30][31][32][33]
Poznati su reagensi koji pokreću dehidrataciju smeša alkohola i karboksilnih kiselina. Jedan primer je Steglihova esterifikacija, koja je metoda formiranja estara pod blagim uslovima.[34][35][36] Metoda je popularna u sintezi peptida, gde su supstrati osetljivi na oštre uslove poput visoke toplote. DCC (dicikloheksilkarbodiimid) se koristi za aktiviranje karboksilne kiseline za dalju reakciju. 4-Dimetilaminopiridin (DMAP) se koristi kao katalizator acil-transfera.[37]
Druga metoda za dehidrataciju smeša alkohola i karboksilnih kiselina je Micunobuova reakcija:[38][39][40][41][42][43][44]
- RCO
2H + R'OH + P(C
6H
5)
3 + R
2N
2 → RCO
2R' + OP(C
6H
5)
3 + R
2N
2H
2
Karboksilne kiseline mogu biti esterifikovane pomoću diazometana:
- RCO
2H + CH
2N
2 → RCO
2CH
3 + N
2
Korišćenjem diazometana, smeše karboksilnih kiselina mogu se konvertovati u njihove metil estre u skoro kvantitativnim prinosima, na primer, za analizu gasnom hromatografijom. Metoda je korisna u specijalizovanim organsko sintetičkim operacijama, ali se smatra previše opasnom i skupom za primene u velikim razmerama.
Esterifikacija karboksilnih kiselina epoksidima
уредиKarboksilne kiseline se esterifikuju tretmanom sa epoksidima, dajući β-hidroksiestre:
- RCO
2H + RCHCH
2O → RCO
2CH
2CH(OH)R
Ova reakcija se koristi u proizvodnji vinil estarske smole od akrilne kiseline.
Alkoholiza acilhlorida i anhidrida kiselina
уредиAlkoholi reaguju sa acil hloridima i anhidridima kiselina dajući estre:
- RCOCl + R'OH → RCO
2R' + HCl - (RCO)
2O + R'OH → RCO
2R' + RCO
2H
Reakcije su nepovratne i pojednostavljuju obradu. Pošto acil hloridi i anhidridi kiselina takođe reaguju sa vodom, poželjni su anhidrovani uslovi. Analogne acilacije amina koje daju amide su manje osetljive jer su amini jači nukleofili i reaguju brže od vode. Ova metoda se koristi samo za laboratorijske procedure, jer je skupa.
Alkilacija karboksilnih kiselina i njihovih soli
уредиTrimetiloksonijum tetrafluoroborat se može koristiti za esterifikaciju karboksilnih kiselina pod uslovima gde su reakcije katalizovane kiselinom neizvodljive:[45]
- RCO
2H + (CH
3)
3OBF
4 → RCO
2CH
3 + (CH
3)
2O + HBF
4
Iako se retko koriste za esterifikacije, karboksilatne soli (često stvorene in situ) reaguju sa elektrofilnim alkilacionim agensima, kao što su alkil halogenidi, dajući estre.[20][46] Dostupnost anjona može inhibirati ovu reakciju, što shodno tome pospešeno katalizatorima faznog transfera[47][48][49] ili takvih visoko polarnih aprotičnih rastvarača kao što je DMF. Dodatna jodidna so može, preko Finkelštajnove reakcije,[50][51][52][53][54] da katalizuje reakciju neposlušnog alkil halida. Alternativno, soli koordinacionog metala, kao što je srebro, mogu poboljšati brzinu reakcije olakšavanjem eliminacije halogenida.
Transesterifikacija
уредиTransesterifikacija,[55][56] koja uključuje promenu jednog estra u drugi, široko se praktikuje:
- RCO
2R' + CH
3OH → RCO
2CH
3 + R'OH
Kao i hidroliza, transesterifikacija je katalizovana kiselinama i bazama. Reakcija se široko koristi za razgradnju triglicerida, npr. u proizvodnji estara masnih kiselina i alkohola. Poli(etilen tereftalat) se proizvodi transeterifikacijom dimetil tereftalata i etilen glikola:[20]
- n (C
6H
4)(CO
2CH
3)
2 + 2n C
2H
4(OH)
2 → [(C
6H
4)(CO
2)
2(C
2H
4)]
n + 2n CH
3OH
Podskup transesterifikacije je alkoholiza diketena. Ova reakcija daje 2-ketoestre.[20]
- (CH
2CO)
2 + ROH → CH
3C(O)CH
2CO
2R
Karbonilacija
уредиAlkeni se podvrgavaju karboalkoksilaciji[57][58][59] u prisustvu metalnih karbonilnih katalizatora. Estri propionske kiseline se komercijalno proizvode ovom metodom:
- H
2C=CH
2 + ROH + CO → CH
3CH
2CO
2R
Priprema metil propionata je jedan ilustrativan primer.
- H
2C=CH
2 + CO + CH
3OH → CH
3CH
2CO
2CH
3
Karbonilacija metanola daje metil format, koji je glavni komercijalni izvor mravlje kiseline. Reakcija je katalizovana natrijum metoksidom:
- CH
3OH + CO → HCO
2CH
3
Dodavanje karboksilnih kiselina alkenima i alkinima
уредиU hidroesterifikaciji, alkeni i alkini se umeću u O−H vezu karboksilnih kiselina. Vinil acetat se industrijski proizvodi dodavanjem sirćetne kiseline acetilenu u prisustvu katalizatora cink acetata:[60]
- HC≡CH + CH
3CO
2H → CH
3CO
2CH=CH
2
Vinil acetat se takođe može proizvesti reakcijom etilena, sirćetne kiseline i kiseonika katalizovanom paladijumom:
- 2 H
2C=CH
2 + 2 CH
3CO
2H + O
2 → 2 CH
3CO
2CH=CH
2 + 2 H
2O
Silikovolframska kiselina se koristi za proizvodnju etil acetata alkilacijom sirćetne kiseline etilenom:
- H
2C=CH
2 + CH
3CO
2H → CH
3CO
2CH
2CH
3
Iz aldehida
уредиTiščenkova reakcija[61][62][63][64] uključuje disproporcionisanje aldehida u prisustvu anhidrovane baze da bi se dobio estar. Katalizatori su aluminijum alkoksidi ili natrijum alkoksidi. Benzaldehid reaguje sa natrijum benziloksidom (generisanim od natrijuma i benzil alkohola) da bi se dobio benzil benzoat.[64] Metoda se koristi u proizvodnji etil acetata iz acetaldehida.[20]
Druge metode
уреди- Favorskijevo preuređenje α-haloketona u prisustvu baze[65][66][67][68][69]
- Bejer-Viligerova oksidacija ketona sa peroksidima[70][71][72]
- Pinerova reakcija[73][74][75][76][77][78][79] nitrila sa alkoholom
- Nukleofilna apstrakcija metal–acil kompleksa[80][81]
- Hidroliza ortoestara u vodenoj kiselini
- Celuloliza putem esterifikacije[82]
- Ozonoliza[83][84][85] alkena korišćenjem obrade u prisustvu hlorovodonične kiseline i raznih alkohola.[86]
- Anodna oksidacija[87][88][89][90] metil ketona dovodi do metil estara.[91]
- Interesterifikacija razmenjuje grupe masnih kiselina različitih estara.[92][93][94][95][96][97]
Reakcije
уредиEstri su manje reaktivni od kiselih halogenida i anhidrida. Kao i kod reaktivnijih acil derivata, oni mogu da reaguju sa amonijakom i primarnim i sekundarnim aminima dajući amide, iako se ova vrsta reakcije ne koristi često, pošto kiseli halogenidi daju bolje prinose.
Transesterifikacija
уредиEstri se mogu konvertovati u druge estre u procesu poznatom kao transesterifikacija. Transesterifikacija može biti katalizovana kiselinom ili bazom i obuhvata reakciju estra sa alkoholom. Pošto je odlazeća grupa takođe alkohol, reakcija unapred i unazad će se često odvijati sličnom brzinom. Korišćenje velikog viška reaktantnog alkohola ili uklanjanje alkohola odlazeće grupe (npr. destilacijom) potisnuće reakciju napred ka završetku, u skladu sa Le Šateljeovim principom.[98]
Hidroliza i saponifikacija
уредиHidroliza estara katalizovana kiselinom je takođe ravnotežni proces – u suštini reverzan reakciji Fišerove esterifikacije.[99][100][101][102][103] Pošto alkohol (koji deluje kao odlazeća grupa) i voda (koja deluje kao nukleofil) imaju slične pKa vrednosti, direktna i reverzna reakcija se takmiče jedna sa drugom. Kao i kod transesterifikacije, korišćenje velikog viška reaktanta (vode) ili uklanjanje jednog od proizvoda (alkohola) može podstaći reakciju unapred.
Bazna hidroliza estara, poznata kao saponifikacija, nije ravnotežni proces; pun ekvivalent baze se troši u reakciji, pri čemu se proizvodi jedan ekvivalent alkohola i jedan ekvivalent karboksilatne soli. Saponifikacija estara masnih kiselina je industrijski važan proces, koji se koristi u proizvodnji sapuna.[98]
Esterifikacija je reverzibilna reakcija. Estri se podvrgavaju hidrolizi u kiselim i baznim uslovima. U kiselim uslovima, reakcija je reverzna reakcija Fišerove esterifikacije. U baznim uslovima, hidroksid deluje kao nukleofil, dok je alkoksid odlazeća grupa. Ova reakcija, saponifikacija, je osnova za pravljenje sapuna.
Alkoksidna grupa takođe može biti zamenjena jačim nukleofilima kao što su amonijak ili primarni ili sekundarni amini da bi se dobili amidi (reakcija amonolize):
- RCO
2R' + NH
2R″ → RCONHR″ + R'OH
Ova reakcija obično nije reverzibilna. Umesto amina mogu se koristiti hidrazini i hidroksilamin. Estri se mogu konvertovati u izocijanate preko intermedijarnih hidroksaminskih kiselina[104][105] u Losenovom preuređenju.[106][107][108][109][110]
Izvori ugljenikovih nukleofila, na primer, Grignardovi reagensi[111][112][113] i organolitijumova jedinjenja, lako se dodaju karbonilu.
Redukcija
уредиU poređenju sa ketonima i aldehidima, estri su relativno otporni na redukciju. Uvođenje katalitičke hidrogenacije u ranom delu 20. veka predstavljao je proboj; estri masnih kiselina se hidrogenišu u masne alkohole.
- RCO
2R' + 2 H
2 → RCH
2OH + R'OH
Tipičan katalizator je bakar hromit. Pre razvoja katalitičke hidrogenacije, estri su redukovani u velikoj meri korišćenjem Buvo-Blankove redukcije.[114][115][116][117][118][119][120][121] Ovaj metod, koji je u velikoj meri zastareo, koristi natrijum u prisustvu izvora protona.
Posebno za fine hemijske sinteze, litijum aluminijum hidrid se koristi za redukciju estara na dva primarna alkohola. Povezani reagens natrijum borohidrid je spor u ovoj reakciji. DIBAH redukuje estre u aldehide.[122]
Direktna redukcija da bi se dobio odgovarajući etar je teška jer središnji hemiacetal ima tendenciju da se razgradi dajući alkohol i aldehid (koji brzo redukuje da bi se dobio drugi alkohol). Reakcija se može postići korišćenjem trietilsilana sa raznim Luisovim kiselinama.[123][124]
Klajzenova kondenzacija i srodne reakcije
уредиEstri mogu biti podvrgnuti raznim reakcijama sa nukleofilima ugljenika. Reaguju sa viškom Grignardovog reagensa dajući tercijarne alkohole. Estri takođe lako reaguju sa enolatima. U Klajzenovoj kondenzaciji,[125][126][127][128][129] enolat jednog estra (1) će napasti karbonilnu grupu drugog estra (2) da bi dao tetraedarski intermedijer 3. Intermedijer se kolapsira, istiskujući alkoksid (R'O−) i stvarajući β-keto estar 4.
Moguće su i ukrštene Klajzenovove kondenzacije, u kojima su enolat i nukleofil različiti estri. Intramolekularna Klajzenovova kondenzacija se zove Dikmanova kondenzacija[130][131][132] ili Dikmanova ciklizacija, jer se može koristiti za formiranje prstenova. Estri se takođe mogu podvrgnuti kondenzaciji sa ketonskim i aldehid enolatima da bi se dobila β-dikarbonilna jedinjenja.[133] Specifičan primer ovoga je Bejker-Venkataramanovo preuređenje,[134][135][136][137][138][139][140][141][142][143][144] u kome aromatični orto-aciloksi keton prolazi kroz intramolekularnu nukleofilnu acil supstituciju i naknadno preuređenje da bi se formirao aromatični β-diketon.[145] Čanovo preuređenje[146][147] je još jedan primer preuređenja koji je rezultat reakcije intramolekularne nukleofilne acil supstitucije.
Druge estarske reaktivnosti
уредиEstri reaguju sa nukleofilima na karbonilnom ugljeniku. Karbonil je slabo elektrofilan, ali ga napadaju jaki nukleofili (amini, alkoksidi, izvori hidrida, organolitijumova jedinjenja, itd.). C–H veze susedne karbonilu su slabo kisele, ali podležu deprotonaciji jakim bazama. Ovaj proces je onaj koji obično pokreće reakcije kondenzacije. Karbonil kiseonik u estrima je slabo bazičan, manje od karbonilnog kiseonika u amidima zbog rezonantne donacije elektronskog para iz azota u amidima, ali formira adukte.
Što se tiče aldehida, atomi vodonika na susednom ugljeniku (u „α poziciji“) karboksilnoj grupi u estrima su dovoljno kiseli da podležu deprotonaciji, što zauzvrat dovodi do raznih korisnih reakcija. Deprotonacija zahteva relativno jake baze, kao što su alkoksidi. Deprotonacija daje nukleofilni enolat, koji može dalje da reaguje, na primer, Klajazenovom kondenzacijom i njenim intramolekularnim ekvivalentom, Dikmanovom kondenzacijom. Ova konverzija se koristi u sintezi estra malonske kiseline,[148][149] pri čemu diestar malonske kiseline reaguje sa elektrofilom (npr. alkil halidom), a zatim se dekarboksilira. Druga varijacija je Frater-Sebahova alkilacija.[150][151][152][153][154]
Druge reakcije
уреди- Estri se mogu direktno pretvoriti u nitrile.[155]
- Metil estri su često podložni dekarboksilaciji u Krapčovoj dekarboksilaciji.[156][157] [158][159][160]
- Fenil estri reaguju na hidroksiarilketone u Frajesovom rearanžmanu.[161][162][163][164]
- Specifični estri su funkcionalizovani sa α-hidroksilnom grupom u Čanovom rearanžmanu.
- Estri sa β-atomima vodonika mogu se konvertovati u alkene u estarskoj pirolizi.[165][166][167]
- Parovi estara su spojeni da daju α-hidroksiketone u aciloinskoj kondenzaciji.[168][169][170]
Zaštitne grupe
уредиKao klasa, estri služe kao zaštitne grupe[171][172] za karboksilne kiseline. Zaštita karboksilne kiseline je korisna u sintezi peptida, da bi se sprečile samostalne reakcije bifunkcionalnih aminokiselina. Metil i etil estri su obično dostupni za mnoge aminokiseline; t-butil estar ima tendenciju da bude skuplji. Međutim, t-butil estri su posebno korisni jer, pod jako kiselim uslovima, t-butil estri se podvrgavaju eliminaciji dajući karboksilnu kiselinu i izobutilen, što pojednostavljuje obradu.
Esterski mirisi
уредиReference
уреди- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ а б IUPAC. „esters”. Kompendijum hemijske terminologije (Internet izdanje).
- ^ Hunter G. K. (2000): Vital Forces. The discovery of the molecular basis of life. . London: Academic Press. 2000. ISBN 978-0-12-361811-5.
- ^ Nelson D. L., Cox M. M. (2013): Lehninger Principles of Biochemistry. . W. H. Freeman and Co. ISBN 978-1-4641-0962-1.
- ^ Hall J. E., Guyton A. C. (2006): Textbook of medical physiology, 11th edition. Elsevier Saunders, St. Louis, Mo. ISBN 978-0-7216-0240-0.
- ^ Cameron Wright (1986). A worker's guide to solvent hazards. The Group. стр. 48. ISBN 9780969054542.
- ^ E. Richard Booser (21. 12. 1993). CRC Handbook of Lubrication and Tribology, Volume III: Monitoring, Materials, Synthetic Lubricants, and Applications. CRC. стр. 237. ISBN 978-1-4200-5045-5.
- ^ „Acetoxytrimethyltin”.
- ^ „Trimethyltin acetate | C5H12O2Sn | ChemSpider”.
- ^ Leopold Gmelin, Handbuch der Chemie, vol. 4: Handbuch der organischen Chemie (vol. 1) (Heidelberg, Baden (Germany): Karl Winter, 1848), page 182.
Original text:
Translation:b. Ester oder sauerstoffsäure Aetherarten.
Ethers du troisième genre.
Viele mineralische und organische Sauerstoffsäuren treten mit einer Alkohol-Art unter Ausscheidung von Wasser zu neutralen flüchtigen ätherischen Verbindungen zusammen, welche man als gepaarte Verbindungen von Alkohol und Säuren-Wasser oder, nach der Radicaltheorie, als Salze betrachten kann, in welchen eine Säure mit einem Aether verbunden ist.b. Ester or oxy-acid ethers.
Ethers of the third type.
Many mineral and organic acids containing oxygen combine with an alcohol upon elimination of water to [form] neutral, volatile ether compounds, which one can view as coupled compounds of alcohol and acid-water, or, according to the theory of radicals, as salts in which an acid is bonded with an ether. - ^ A. A. Yakovenko; J. H. Gallegos; M. Yu. Antipin; A. Masunov; T. V. Timofeeva (2011). „Crystal Morphology as an Evidence of Supramolecular Organization in Adducts of 1,2-Bis(chloromercurio)tetrafluorobenzene with Organic Esters”. Crystal Growth & Design. 11 (9): 3964—3978. doi:10.1021/cg200547k.
- ^ а б Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th изд.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
- ^ „Chemistry of Enols and Enolates - Acidity of alpha-hydrogens”. Архивирано из оригинала 07. 01. 2018. г. Приступљено 25. 11. 2011.
- ^ Diwakar M. Pawar; Abdelnaser A. Khalil; Denise R. Hooks; Kenneth Collins; Tijuana Elliott; Jefforey Stafford; Lucille Smith; Eric A. Noe (1998). „E and Z Conformations of Esters, Thiol Esters, and Amides”. Journal of the American Chemical Society. 120 (9): 2108—2112. doi:10.1021/ja9723848.
- ^ Christophe Dugave; Luc Demange (2003). „Cis−Trans Isomerization of Organic Molecules and Biomolecules: Implications and Applications”. Chemical Reviews. 103 (7): 2475—2932. PMID 12848578. doi:10.1021/cr0104375.
- ^ Isolation of triglyceride from nutmeg: G. D. Beal "Trimyristen" Organic Syntheses, Coll. Vol. 1, p.538 (1941). Link
- ^ McGee, Harold. On Food and Cooking. 2003, Scribner, New York.
- ^ De Vos, Lobke; Van de Voorde, Babs; Van Daele, Lenny; Dubruel, Peter; Van Vlierberghe, Sandra (децембар 2021). „Poly(alkylene terephthalate)s: From current developments in synthetic strategies towards applications”. European Polymer Journal. 161: 110840. Bibcode:2021EurPJ.16110840D. doi:10.1016/j.eurpolymj.2021.110840. hdl:1854/LU-8730084 .
- ^ Takashi Ohara; Takahisa Sato; Noboru Shimizu; Günter Prescher; Helmut Schwind; Otto Weiberg; Klaus Marten; Helmut Greim (2003). „Acrylic Acid and Derivatives”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. ISBN 3527306730. doi:10.1002/14356007.a01_161.pub2.
- ^ а б в г д „Esters, Organic”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. 2005. doi:10.1002/14356007.a09_565.pub2.
- ^ Williams, Roger J.; Gabriel, Alton; Andrews, Roy C. (1928). „The Relation Between the Hydrolysis Equilibrium Constant of Esters and the Strengths of the Corresponding Acids”. Journal of the American Chemical Society. 50 (5): 1267—1271. doi:10.1021/ja01392a005.
- ^ Helmenstine, Anne Marie (2020). „Le Chatelier's Principle Definition”. ThoughtCo. Архивирано из оригинала 2021-04-20. г. Приступљено 2022-03-09.
- ^ Ball, David W.; Key, Jessie A. (2014-09-16). „Shifting Equilibria: Le Chatelier’s Principle”. Introductory Chemistry – 1st Canadian edition (на језику: енглески). Victoria, B.C: BCcampus: OpenEd. ISBN 978-1-77420-003-2 — преко opentextbc.ca.
- ^ Mander, Peter (2016-09-01). „Le Châtelier’s principle”. carnotcycle (на језику: енглески). Приступљено 2024-09-29.
- ^ fr:s:Page:Comptes rendus hebdomadaires des séances de l’Académie des sciences, tome 099, 1884.djvu/786
- ^ Kheilová, M.; Štrunc, M. (1995-01-01). „Is the Le Chatelier-Braun Principle Valid in General in Linear Nonequilibrium Thermodynamics?” (на језику: енглески). 20 (1): 19—38. ISSN 1437-4358. doi:10.1515/jnet.1995.20.1.19.
- ^ Kresge, Charles T.; Dhingra, Sandeep S. (2004). „Molecular Sieves”. Kirk-Othmer Encyclopedia of Chemical Technology. ISBN 978-0-471-48494-3. doi:10.1002/0471238961.1315120511210812.a01.pub2.
- ^ Mazur, Michal; Přech, Jan; Čejka, Jiří (2019). „Zeolites and Other Micro- and Mesoporous Molecular Sieves”. Kirk-Othmer Encyclopedia of Chemical Technology. стр. 1—36. ISBN 978-0-471-48494-3. doi:10.1002/0471238961.zeolcejk.a01.pub2.
- ^ Cohen, Alan P. (2003). „Desiccants”. Kirk-Othmer Encyclopedia of Chemical Technology. ISBN 978-0-471-48494-3. doi:10.1002/0471238961.0405190903150805.a01.pub2.
- ^ „Dean–Stark Apparatus”. University of Southampton, University of Birmingham, University of Nottingham and University of Sheffield. Архивирано из оригинала 8. 9. 2011. г. Приступљено 17. 11. 2011.
- ^ Wiberg, Kenneth B. (1960). Laboratory Technique in Organic Chemistry. McGraw-Hill series in advanced chemistry. New York: McGraw Hill. ASIN B0007ENAMY.
- ^ E. W. Dean and D. D. Stark (1920). „A convenient method for the determination of water in petroleum and other organic emulsions”. The Journal of Industrial & Engineering Chemistry. 12 (5): 486—490. doi:10.1021/ie50125a025.
- ^ Andrea Sella (јун 2010). „Classic kit: Dean–Stark apparatus”. Chemistry World. Royal Society of Chemistry.
- ^ B. Neises, W. Steglich (1978). „Simple Method for the Esterification of Carboxylic Acids”. Angew. Chem. Int. Ed. 17 (7): 522—524. doi:10.1002/anie.197805221.
- ^ J. C. Sheehan, G. P. Hess (1955). „A New Method of Forming Peptide Bonds”. J. Am. Chem. Soc. 77 (4): 1067—1068. doi:10.1021/ja01609a099.
- ^ W. König, R. Geiger (1970). „Eine neue Methode zur Synthese von Peptiden: Aktivierung der Carboxylgruppe mit Dicyclohexylcarbodiimid unter Zusatz von 1-Hydroxy-benzotriazolen”. Chem. Ber. 103 (3): 788—798. PMID 5436656. doi:10.1002/cber.19701030319.
- ^ B. Neises; W. Steglich. „Esterification of Carboxylic Acids with Dicyclohexylcarbodiimide/4-Dimethylaminopyridine: tert-Butyl ethyl fumarate”. Org. Synth.; Coll. Vol., 7, стр. 93
- ^ Mitsunobu, O.; Yamada, Y. (1967). „Preparation of Esters of Carboxylic and Phosphoric Acid via Quaternary Phosphonium Salts”. Bulletin of the Chemical Society of Japan. 40 (10): 2380—2382. doi:10.1246/bcsj.40.2380.
- ^ „Organic Syntheses Procedure”. orgsyn.org (на језику: енглески). Приступљено 2023-02-13.
- ^ Mitsunobu, O. (1981). „The Use of Diethyl Azodicarboxylate and Triphenylphosphine in Synthesis and Transformation of Natural Products”. Synthesis. 1981 (1): 1—28. doi:10.1055/s-1981-29317.
- ^ Castro, B. R. (1983). „Replacement of Alcoholic Hydroxyl Groups by Halogens and Other Nucleophiles via Oxyphosphonium Intermediates”. Replacement of Alcoholic Hydroxy Groups by Halogens and Other Nucleophiles via Oxyphosphonium Intermediates. Organic Reactions. 29. стр. 1—162. ISBN 9780471264187. doi:10.1002/0471264180.or029.01.
- ^ Hughes, D. L. (1992). „The Mitsunobu Reaction”. Organic Reactions. 42. стр. 335—656. ISBN 9780471264187. doi:10.1002/0471264180.or042.02.
- ^ Hughes, D. L. (1996). „Progress in the Mitsunobu Reaction. A Review”. Organic Preparations and Procedures International. 28 (2): 127—164. doi:10.1080/00304949609356516.
- ^ Swamy, K. C. K.; Kumar, N. N. B.; Balaraman, E.; Kumar, K. V. P. P. (2009). „Mitsunobu and Related Reactions: Advances and Applications”. Chemical Reviews. 109 (6): 2551—2651. PMID 19382806. doi:10.1021/cr800278z.
- ^ Raber, Douglas J.; Gariano, Jr, Patrick; Brod, Albert O.; Gariano, Anne L.; Guida, Wayne C. (1977). „Esterification of Carboxylic Acids with Trialkyloxonium Salts: Ethyl and Methyl 4-Acetoxybenzoates”. Organic Syntheses. 56: 59. doi:10.15227/orgsyn.056.0059.
- ^ Matsumoto, Kouichi; Shimazaki, Hayato; Miyamoto, Yu; Shimada, Kazuaki; Haga, Fumi; Yamada, Yuki; Miyazawa, Hirotsugu; Nishiwaki, Keiji; Kashimura, Shigenori (2014). „Simple and Convenient Synthesis of Esters from Carboxylic Acids and Alkyl Halides Using Tetrabutylammonium Fluoride”. Journal of Oleo Science (на језику: енглески). 63 (5): 539—544. ISSN 1345-8957. PMID 24770480. doi:10.5650/jos.ess13199 .
- ^ Katole DO, Yadav GD. Process intensification and waste minimization using liquid-liquid-liquid triphase transfer catalysis for the synthesis of 2-((benzyloxy)methyl)furan. Molecular Catalysis 2019;466:112–21. https://doi.org/10.1016/j.mcat.2019.01.004
- ^ J. O. Metzger (1998). „Solvent-Free Organic Syntheses”. Angewandte Chemie International Edition. 37 (21): 2975—2978. PMID 29711128. doi:10.1002/(SICI)1521-3773(19981116)37:21<2975::AID-ANIE2975>3.0.CO;2-A.
- ^ Mieczyslaw Makosza (2000). „Phase-transfer catalysis. A general green methodology in organic synthesis”. Pure Appl. Chem. 72 (7): 1399—1403. doi:10.1351/pac200072071399 .
- ^ Finkelstein, Hans (1910). „Darstellung organischer Jodide aus den entsprechenden Bromiden und Chloriden”. Ber. Dtsch. Chem. Ges. (на језику: German). 43 (2): 1528—1532. doi:10.1002/cber.19100430257.
- ^ Ervithayasuporn, V. (2013). „One-pot synthesis of halogen exchanged silsesquioxanes: octakis(3-bromopropyl)octasilsesquioxane and octakis(3-iodopropyl)octasilsesquioxane”. Dalton Trans. 42 (37): 13747—13753. PMID 23907310. doi:10.1039/C3DT51373D.
- ^ B. H. Lipshutz; M. R. Wood; R. Tirado (1999). „Copper-catalyzed Conjugate Addition of Functionalized Organozinc Reagents to α,β-Unsaturated Ketones: Ethyl 5-(3-oxocyclohexyl)pentanoate”. Org. Synth. 76: 252. doi:10.15227/orgsyn.076.0252.
- ^ Streitwieser, A. (1956). „Solvolytic Displacement Reactions at Saturated Carbon Atoms”. Chem. Rev. 56 (4): 571—752. doi:10.1021/cr50010a001.
- ^ Bordwell, F. G.; Brannen, W. T. (1964). „The Effect of the Carbonyl and Related Groups on the Reactivity of Halides in SN2 Reactions”. J. Am. Chem. Soc. 86 (21): 4645—4650. doi:10.1021/ja01075a025.
- ^ Otera, Junzo. (јун 1993). „Transesterification”. Chemical Reviews. 93 (4): 1449—1470. doi:10.1021/cr00020a004.
- ^ „ENZYME – 3.1.1.3 Triacylglycerol lipase”. enzyme.expasy.org. SIB Swiss Institute of Bioinformatics. Приступљено 2021-02-17.
- ^ Ahmad, Shahbaz; Bühl, Michael (2021-08-04). „Computational modelling of Pd-catalysed alkoxycarbonylation of alkenes and alkynes”. Physical Chemistry Chemical Physics (на језику: енглески). 23 (30): 15869—15880. Bibcode:2021PCCP...2315869A. ISSN 1463-9084. PMID 34318843. S2CID 236472958. doi:10.1039/D1CP02426D . hdl:10023/23678 .
- ^ Scott D. Barnicki (2012). „Synthetic Organic Chemicals”. Ур.: James A. Kent. Handbook of Industrial Chemistry and Biotechnology (12th изд.). New York: Springer. ISBN 978-1-4614-4259-2.
- ^ Kiss, Gabor (2001). „Palladium-Catalyzed Reppe Carbonylation”. Chemical Reviews. 101 (11): 3435—3456. PMID 11840990. doi:10.1021/cr010328q.
- ^ „Vinyl Esters”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. 2005. стр. 1—16. doi:10.1002/14356007.a27_419.pub2.
- ^ Seki, Tsunetake; Nakajo, Tetsuo; Onaka, Makoto (2006). „The Tishchenko Reaction: A Classic and Practical Tool for Ester Synthesis”. Chemistry Letters. 35 (8): 824—829. doi:10.1246/cl.2006.824.
- ^ Mlynarski, Jacek (2006). „Direct Asymmetric Aldol-Tishchenko Reaction”. European Journal of Organic Chemistry. 2006 (21): 4779—4786. doi:10.1002/ejoc.200600258.
- ^ Hattori, Hideshi (2001). „Solid base catalysts: Generation of basic sites and application to organic synthesis”. Applied Catalysis A: General. 222 (1–2): 247—259. doi:10.1016/S0926-860X(01)00839-0.
- ^ а б Kamm, O.; Kamm, W. F. (1922). „Benzyl benzoate”. Organic Syntheses. 2: 5. doi:10.15227/orgsyn.002.0005.
- ^ Cope, Arthur (1960). Organic Reaction Volume XI (1 изд.). New York: Wiley-Interscience. ISBN 9780471171270. doi:10.1002/jps.2600500225.
- ^ Wohllebe, J.; Garbisch, E. W. (1977). „Ring Contraction via a Favorskii-Type Rearrangement: Cycloundecanone”. Org. Synth. 56: 107. doi:10.15227/orgsyn.056.0107.; Coll. Vol., 6, стр. 368
- ^ Shioiri, Takayuki; Kawai, Nobutaka (1978). „New methods and reagents in organic synthesis. 2. A facile conversion of alkyl aryl ketones to α-arylalkanoic acids using diphenyl phosphorazidate. Its application to a new synthesis of ibuprofen and naproxen, nonsteroidal antiinflammatory agents”. J. Org. Chem. 43 (14): 2936—2938. doi:10.1021/jo00408a049.
- ^ Hamada, Yasumasa; Shioiri, Takayuki (1982). „Cycloundecanecarboxylic Acid”. Org. Synth. 62: 191. doi:10.15227/orgsyn.062.0191.; Coll. Vol., 7, стр. 135
- ^ Goheen, D. W.; Vaughan, W. R. (1963). „Cyclopentanecarboxylic acid, methyl ester”. Org. Synth. 39: 37. doi:10.15227/orgsyn.039.0037.; Coll. Vol., 4, стр. 594
- ^ Kürti, László; Czakó, Barbara (2005). Strategic Applications of Named Reactions in Organic Synthesis . Burlington; San Diego; London: Elsevier Academic Press. стр. 28. ISBN 978-0-12-369483-6.
- ^ Krow, Grant R. (1993). „The Baeyer-Villiger Oxidation of Ketones and Aldehydes”. Organic Reactions. 43 (3): 251—798. ISBN 0471264180. doi:10.1002/0471264180.or043.03.
- ^ Carey, Francis A.; Sundberg, Richard J. (2007). Advanced Organic Chemistry: Part B: Reactions and Synthesis (5th изд.). New York: Springer. стр. 1135. ISBN 978-0387683546.
- ^ „Pinner Reaction”. Comprehensive Organic Name Reactions and Reagents (504): 2237—2240. 2010. ISBN 9780470638859. doi:10.1002/9780470638859.conrr504.
- ^ A. Pinner, F. Klein; Klein (1877). „Umwandlung der Nitrile in Imide”. Berichte der deutschen chemischen Gesellschaft. 10 (2): 1889—1897. doi:10.1002/cber.187701002154.
- ^ A. Pinner, Fr. Klein; Klein (1878). „Umwandlung der Nitrile in Imide”. Berichte der deutschen chemischen Gesellschaft. 11 (2): 1475—1487. doi:10.1002/cber.18780110258.
- ^ A. Pinner (1883). „Ueber die Umwandlung der Nitrile in Imide”. Berichte der deutschen chemischen Gesellschaft. 16 (2): 1643—1655. doi:10.1002/cber.18830160235.
- ^ Roger, R.; Neilson, D. G. (1961). „The Chemistry of Imidates”. Chem. Rev. 61 (2): 179—211. doi:10.1021/cr60210a003.
- ^ Adams, Roger; Thal, A. F. (1922). „Ethyl Phenylacetate”. Organic Syntheses. 2: 27. doi:10.15227/orgsyn.002.0027.
- ^ Elvidge, J. A.; Linstead, R. P. (1954). „Heterocyclic imines and amines. Part III. Succinimidine”. Journal of the Chemical Society (Resumed): 442. doi:10.1039/JR9540000442.
- ^ Spessard, Gary; Miessler, Gary (2010).Organometallic Chemistry: Second Edition. pp. 285-289 ISBN 978-0-19-533099-1
- ^ Xu, Ruren; Pang, Wenqin; Huo, Qisheng (2011).Modern Inorganic Synthetic Chemistry. pp. 275-278 ISBN 978-0-444-53599-3
- ^ Ignatyev, Igor; Charlie Van Doorslaer; Pascal G.N. Mertens; Koen Binnemans; Dirk. E. de Vos (2011). „Synthesis of glucose esters from cellulose in ionic liquids” . Holzforschung. 66 (4): 417—425. S2CID 101737591. doi:10.1515/hf.2011.161.
- ^ Bailey, P. S.; Erickson, R. E. (1973). „Diphenaldehyde”. Org. Synth.; Coll. Vol., 5, стр. 489
- ^ Tietze, L. F.; Bratz, M. (1998). „Dialkyl Mesoxalates by Ozonolysis of Dialkyl Benzalmalonates”. Org. Synth.; Coll. Vol., 9, стр. 314
- ^ Harwood, Laurence M.; Moody, Christopher J. (1989). Experimental Organic Chemistry: Principles and Practice (Illustrated изд.). Wiley-Blackwell. стр. 55–57. ISBN 978-0632020171.
- ^ Neumeister, Joachim; Keul, Helmut; Pratap Saxena, Mahendra; Griesbaum, Karl (1978). „Ozone Cleavage of Olefins with Formation of Ester Fragments”. Angewandte Chemie International Edition in English. 17 (12): 939—940. doi:10.1002/anie.197809392.
- ^ Sperry, Jeffrey B.; Wright, Dennis L. (2006). „The application of cathodic reductions and anodic oxidations in the synthesis of complex molecules”. Chem. Soc. Rev. 35 (7): 605—621. PMID 16791332. doi:10.1039/b512308a.
- ^ Topics in current chemistry. Electrochemistry, Vol. 3 (Topics in Current Chemistry, Vol. 148) E. Steckhan (Ed), Springer, NY 1988.
- ^ Yan, M.; Kawamata, Y.; Baran, P. S. (2017). „Synthetic Organic Electrochemistry: Calling All Engineers.”. Angewandte Chemie International Edition. 57 (16): 4149—4155. PMC 5823775 . PMID 28834012. doi:10.1002/anie.201707584.
- ^ Utley, James (1997). „Trends in Organic Electrosynthesis”. Chemical Society Reviews. 26 (3): 157. doi:10.1039/cs9972600157.
- ^ Makhova, Irina V.; Elinson, Michail N.; Nikishin, Gennady I. (1991). „Electrochemical oxidation of ketones in methanol in the presence of alkali metal bromides”. Tetrahedron. 47 (4–5): 895—905. doi:10.1016/S0040-4020(01)87078-2.
- ^ Hui, Y.H. (2006), Handbook of Food Science, Technology, and Engineering, Vol.1, Boca Raton: Taylor & Francis, ISBN 1-57444-551-0
- ^ T. L. Husum, L. S. Pedersen, P. M. Nielsen, M. W. Christensen, D. Kristensen, and H. C. Holm (2003): "Enzymatic interesterification: Process advantages and product benefits." Архивирано 2006-01-04 на сајту Wayback Machine . Palm Oil Information Online Service. Retrieved 2010-10-20.
- ^ W. Hamm and R. Hamilton, editors (2000): Edible Oil Processing. ISBN 1-84127-038-5
- ^ Rousseau, D. (2002): "The Effects of Interesterification on the Physical Properties of Fats". Chapter 13 of Physical Properties of Lipids. CRC Press.
- ^ Institute of Shortenings and Edible oils (2006). „Food Fats and oils” (PDF). Архивирано из оригинала (PDF) 2007-03-26. г. Приступљено 2009-02-19.
- ^ Costales-Rodriquez, R.; Gibon, V.; Verhe, R.; De Greyt, W. (2009), „Chemical and Enzymatic Interesterification of a Blend of Palm Stearin: Soybean Oil for Low Trans-Margarine Formulation.”, J Am Oil Chem Soc, 86 (7): 681—697, doi:10.1007/s11746-009-1395-2
- ^ а б Wade 2010, pp. 1005–1009.
- ^ Emil Fischer, Arthur Speier (1895). „Darstellung der Ester”. Chemische Berichte. 28 (3): 3252—3258. doi:10.1002/cber.189502803176.
- ^ Offenhauer, Robert D. (1964). „The direct esterification of phenols”. Journal of Chemical Education. 41 (1): 39. Bibcode:1964JChEd..41...39O. doi:10.1021/ed041p39.
- ^ Hocking, M.B. (1980). „Phenyl acetate preparation from phenol and acetic acid: Reassessment of a common textbook misconception”. Journal of Chemical Education. 57 (7): 527. Bibcode:1980JChEd..57..527H. doi:10.1021/ed057p527.
- ^ Furniss, Brian; Hannaford, Antony; Smith, Peter; Tatchell, Austin (1996). Vogel's Textbook of Practical Organic Chemistry 5th Ed. London: Longman Science & Technical. стр. 695–697 & 699–704. ISBN 9780582462366.
- ^ Tingle, J. Bishop (1906). „Reports: Esterification”. American Chemical Journal. 35: 368—369. Приступљено 19. 1. 2016.
- ^ Munson, James W. (1992). „Hydroxamic acids”. Ур.: S. Patai. Acid Derivatives (1992), Volume 2. PATAI'S Chemistry of Functional Groups. стр. 849—873. ISBN 9780470772508. doi:10.1002/9780470772508.ch15.
- ^ C. R. Hauser; W. B. Renfrow Jr (1939). „Benzohydroxamic Acid”. Org. Synth. 19: 15. doi:10.15227/orgsyn.019.0015.
- ^ Wang, Zerong (2010). Comprehensive organic name reactions and reagents. John Wiley & Sons, Inc. стр. 1772—1776. ISBN 9780471704508.
- ^ Yale, H. L. (1943). „The Hydroxamic Acids”. Chem. Rev. 33 (3): 209—256. doi:10.1021/cr60106a002.
- ^ Bauer, L.; Exner, O. (1974). „The Chemistry of Hydroxamic Acids and N-Hydroxyimides”. Angew. Chem. Int. Ed. Engl. 13 (6): 376. doi:10.1002/anie.197403761.
- ^ Shioiri, Takayuki (1991). „Degradation Reactions”. Comprehensive Organic Synthesis. 6: 795—828. ISBN 9780080359298. doi:10.1016/B978-0-08-052349-1.00172-4.
- ^ Hauser, C. R.; Renfrow, Jr.., W. B. (1939). „Benzohydroxamic Acid”. Organic Syntheses. 19: 15. doi:10.15227/orgsyn.019.0015.
- ^ Goebel, M. T.; Marvel, C. S. (1933). „The Oxidation of Grignard Reagents”. Journal of the American Chemical Society. 55 (4): 1693—1696. doi:10.1021/ja01331a065.
- ^ Smith, David H. (1999). „Grignard Reactions in "Wet" Ether”. Journal of Chemical Education. 76 (10): 1427. Bibcode:1999JChEd..76.1427S. doi:10.1021/ed076p1427.
- ^ Philip E. Rakita (1996). „5. Safe Handling Practices of Industrial Scale Grignard Ragents” (Google Books excerpt). Ур.: Gary S. Silverman; Philip E. Rakita. Handbook of Grignard reagents. CRC Press. стр. 79—88. ISBN 0-8247-9545-8.
- ^ Wang, Zerong, ур. (2009). „109. Bouveault–Blanc Reduction”. Comprehensive Organic Name Reactions and Reagents. стр. 493—496. ISBN 978-0-471-70450-8. doi:10.1002/9780470638859.conrr109.
- ^ Bouveault, L.; Blanc, G. (1903). „Préparation des alcools primaires au moyen des acides correspondants” [Preparation of primary alcohols by means of the corresponding acids]. Compt. Rend. (на језику: French). 136: 1676—1678.
- ^ Bouveault, L.; Blanc, G. (1903). „Préparation des alcools primaires au moyen des acides correspondants” [Preparation of primary alcohols by means of the corresponding acids]. Compt. Rend. (на језику: French). 137: 60—62.
- ^ Bouveault, L.; Blanc, G. (1904). „Transformation des acides monobasiques saturés dans les alcools primaires correspondants” [Transforming saturated monobasic acids into the corresponding primary alcohols]. Bull. Soc. Chim. Fr. (на језику: French). 31: 666—672.
- ^ Bouveault, L.; Blanc, G. (1904). „Hydrogénation des éthers des acides possédant en outre les fonctions éther-oxyde ou acétal” [Hydrogenation of the ether of the acids furthermore possessing the ether-oxide or acetal functions]. Bull. Soc. Chim. Fr. (на језику: French). 31 (3): 1210—1213.
- ^ Reid, E. E.; Cockerille, F. O.; Meyer, J. D.; Cox, W. M.; Ruhoff, J. R. (1935). „Oleyl Alcohol”. Organic Syntheses. 15: 51. doi:10.15227/orgsyn.015.0051.
- ^ Adkins, Homer; Gillespie, R. H. (1949). „Oleyl alcohol”. Organic Syntheses. 29: 80. doi:10.15227/orgsyn.029.0080.
- ^ Ford, S. G.; Marvel, C. S. (1930). „Lauryl Alcohol”. Organic Syntheses. 10: 62. doi:10.15227/orgsyn.010.0062.
- ^ W. Reusch. „Carboxyl Derivative Reactivity”. Virtual Textbook of Organic Chemistry. Архивирано из оригинала 2016-05-16. г.
- ^ Yato, Michihisa; Homma, Koichi; Ishida, Akihiko (јун 2001). „Reduction of carboxylic esters to ethers with triethyl silane in the combined use of titanium tetrachloride and trimethylsilyl trifluoromethanesulfonate”. Tetrahedron. 57 (25): 5353—5359. doi:10.1016/S0040-4020(01)00420-3.
- ^ Sakai, Norio; Moriya, Toshimitsu; Konakahara, Takeo (јул 2007). „An Efficient One-Pot Synthesis of Unsymmetrical Ethers: A Directly Reductive Deoxygenation of Esters Using an InBr3/Et3SiH Catalytic System”. The Journal of Organic Chemistry. 72 (15): 5920—5922. PMID 17602594. doi:10.1021/jo070814z.
- ^ Carey, F. A. (2006). Organic Chemistry (6th изд.). New York, NY: McGraw-Hill. ISBN 0-07-111562-5.
- ^ Claisen, L.; Claparede, A. (1881). „Condensationen von Ketonen mit Aldehyden”. Berichte der Deutschen Chemischen Gesellschaft. 14 (2): 2460—2468. doi:10.1002/cber.188101402192.
- ^ Claisen, L. (1887). „Ueber die Einführung von Säureradicalen in Ketone”. Berichte der Deutschen Chemischen Gesellschaft. 20 (1): 655—657. doi:10.1002/cber.188702001150.
- ^ Hauser, C. R.; Hudson, B. E. Jr. (1942). „The Acetoacetic Ester Condensation and Certain Related Reactions”. Organic Reactions. 1: 266—302. ISBN 0471264180. doi:10.1002/0471264180.or001.09.
- ^ Riemenschneider, Wilhelm; Bolt, Hermann M. (2005). „Esters, Organic”. Ullmann's Encyclopedia of Industrial Chemistry. ISBN 3527306730. doi:10.1002/14356007.a09_565.pub2.
- ^ Kwart, Harold; King, Kenneth (1969). „Rearrangement and cyclization reactions of carboxylic acids and esters”. Ур.: S. Patai. PATAI'S Chemistry of Functional Groups: Carboxylic Acids and Esters (1969). стр. 341—373. ISBN 9780470771099. doi:10.1002/9780470771099.ch8.
- ^ Schaefer, J. P.; Bloomfield, J. J. (1967). „The Dieckmann Condensation (Including the Thorpe-Ziegler Condensation)”. Organic Reactions. 15: 1—203. ISBN 0471264180. doi:10.1002/0471264180.or015.01.
- ^ Janice Gorzynski Smith (2007). Organic Chemistry (2nd изд.). стр. 932–933. ISBN 978-0073327495.
- ^ Carey 2006, pp. 919–924.
- ^ Baker, W. (1933). „Molecular rearrangement of some o-acyloxyacetophenones and the mechanism of the production of 3-acylchromones”. J. Chem. Soc.: 1381—1389. doi:10.1039/JR9330001381.
- ^ Mahal, H. S.; Venkataraman, K. (1934). „Synthetical experiments in the chromone. group. XIV. Action of sodamide on 1-acyloxy-2-acetonaphthones”. J. Chem. Soc.: 1767—1769. doi:10.1039/JR9340001767.
- ^ Wheeler, T. S. (1952). „Flavone”. Organic Syntheses. 32: 72. doi:10.15227/orgsyn.032.0072. (also in the Collective Volume (1963) 4: 478 (PDF)).
- ^ Jain, P. K.; Makrandi, J. K. (1982). „A Facile Baker-Venkataraman Synthesis of Flavones using Phase Transfer Catalysis”. Synthesis. 1982 (3): 221—222. doi:10.1055/s-1982-29755.
- ^ Kalinin, A. V.; Da Silva, A. J. M.; Lopes, C. C.; Lopes, R. S. C.; Snieckus, V. (1998). „Directed ortho metalation – cross coupling links. Carbamoyl rendition of the Baker-Venkataraman rearrangement. Regiospecific route to substituted 4-hydroxycoumarins”. Tetrahedron Letters. 39 (28): 4995—4998. doi:10.1016/S0040-4039(98)00977-0.
- ^ Kraus, G. A.; Fulton, B. S.; Wood, S.H. (1984). „Aliphatic acyl transfer in the Baker-Venkataraman reaction”. J. Org. Chem. 49 (17): 3212—3214. doi:10.1021/jo00191a033.
- ^ Reddy, B.P.; Krupadanam, G.L.D. (1996). „The synthesis of 8-allyl-2-styrylchromones by the modified baker-venkataraman transformation”. J. Heterocycl. Chem. 33 (6): 1561. doi:10.1002/jhet.5570330602.
- ^ Kalinin, A.V.; Sneckus, V. (1998). „4,6-Dimethoxy-3,7-dimethylcoumarin from Colchicum decaisnei. Total synthesis by carbamoyl Baker-Venkataraman rearrangement and structural revision to isoeugenetin methyl ether”. Tetrahedron Lett. 39 (28): 4999. doi:10.1016/S0040-4039(98)00978-2.
- ^ Thasana, N.; Ruchirawat, S. (2002). „The application of the Baker–Venkataraman rearrangement to the synthesis of benz[b]indeno[2,1-e]pyran-10,11-dione”. Tetrahedron Lett. 43 (25): 4515. doi:10.1016/S0040-4039(02)00818-3.
- ^ Santos, C.M.M.; Silva, A.M.S.; Cavaleiro, J.A.S. (2003). „Synthesis of New Hydroxy-2-styrylchromones”. Eur. J. Org. Chem. 2003 (23): 4575. doi:10.1002/ejoc.200300468. hdl:10198/3932 .
- ^ Santos, Clementina M.; Silva, Artur M. S. (2017). „An Overview of 2-Styrylchromones: Natural Occurrence,Synthesis, Reactivity and Biological Properties”. Eur. J. Org. Chem. 2017 (22): 3115—3133. doi:10.1002/ejoc.201700003. hdl:10198/14517 — преко Reaxys.
- ^ Kürti and Czakó 2005, p. 30.
- ^ Rearrangement of α-acyloxyacetates into 2-hydroxy-3-ketoesters S. D. Lee, T. H. Chan, and K. S. Kwon Tetrahedron Lett. 1984, 25, 3399-3402. (doi:10.1016/S0040-4039(01)91030-5)
- ^ First total synthesis of taxol 1. Functionalization of the B ring Robert A. Holton, Carmen Somoza, Hyeong Baik Kim, Feng Liang, Ronald J. Biediger, P. Douglas Boatman, Mitsuru Shindo, Chase C. Smith, Soekchan Kim, et al.; J. Am. Chem. Soc. 1994, 116(4), 1597-1598. (doi:10.1021/ja00083a066)
- ^ House, Herbert O. (1972). Modern Synthetic Reactions . Menlo Park, CA.: W. A. Benjamin. ISBN 0-8053-4501-9.
- ^ „Malonic Ester Synthesis”. Organic Chemistry Portal. Приступљено 2007-10-26.
- ^ Fráter, G.; Müller, U.; Günther, W. (1984). „The stereoselective α-alkylation of chiral β-hydroxy esters and some applications thereof”. Tetrahedron. 40 (8): 1269—1277. doi:10.1016/S0040-4020(01)82413-3.
- ^ Seebach, Dieter; Wasmuth, Daniel (1980). „Herstellung von erythro-2-Hydroxybernsteinsäure-Derivaten aus Äpfelsäureester. Vorläufige Mitteilung”. Helvetica Chimica Acta (на језику: German). 63 (1): 197—200. doi:10.1002/hlca.19800630118.
- ^ Mundy, Bradford; Ellerd, Michael; Favaloro, Frank (2005). Name Reactions and Reagents in Organic Synthesis. John Wiley & Sons. стр. 252—253. ISBN 9780471228547.
- ^ Crimmins, Michael; Vanier, Grace (2006). „Enantioselective Total Synthesis of (+)-SCH 351448”. Organic Letters. 8 (13): 2887—2890. PMID 16774282. doi:10.1021/ol061073b.
- ^ Raghavan, Sadagopan; Rathore, Kailash (2009). „Asymmetric synthesis of (−)-tetrahydrolipstatin”. Tetrahedron. 65 (48): 10083—10092. doi:10.1016/j.tet.2009.09.062.
- ^ Wood, J. L.; Khatri, N. A.; Weinreb, S. M. (1979). „A direct conversion of esters to nitriles”. Tetrahedron Letters. 20 (51): 4907. doi:10.1016/S0040-4039(01)86746-0.
- ^ Poon, Po. S.; Banerjee, Ajoy K.; Laya, Manuel S. (2011). „Advances in the Krapcho Decarboxylation”. Journal of Chemical Research (на језику: енглески). 35 (2): 67—73. ISSN 1747-5198. doi:10.3184/174751911X12964930076403.
- ^ Hansen, Thomas; Roozee, Jasper C.; Bickelhaupt, F. Matthias; Hamlin, Trevor A. (2022-02-04). „How Solvation Influences the S N 2 versus E2 Competition”. The Journal of Organic Chemistry (на језику: енглески). 87 (3): 1805—1813. ISSN 0022-3263. PMC 8822482 . PMID 34932346. doi:10.1021/acs.joc.1c02354.
- ^ Olejar, Kenneth J.; Kinney, Chad A. (2021). „Evaluation of thermo-chemical conversion temperatures of cannabinoid acids in hemp (Cannabis sativa L.) biomass by pressurized liquid extraction”. Journal of Cannabis Research (на језику: енглески). 3 (1): 40. ISSN 2522-5782. PMC 8408919 . PMID 34465400. doi:10.1186/s42238-021-00098-6 .
- ^ Dunn, Gerald E.; Thimm, Harald F. (1977-04-15). „Kinetics and mechanism of decarboxylation of some pyridinecarboxylic acids in aqueous solution. II”. Canadian Journal of Chemistry (на језику: енглески). 55 (8): 1342—1347. ISSN 0008-4042. doi:10.1139/v77-185.
- ^ Krapcho, A. Paul; Weimaster, J. F.; Eldridge, J. M.; Jahngen, E. G. E.; Lovey, A. J.; Stephens, W. P. (1978-01-01). „Synthetic applications and mechanism studies of the decarbalkoxylations of geminal diesters and related systems effected in dimethyl sulfoxide by water and/or by water with added salts”. The Journal of Organic Chemistry. 43 (1): 138—147. ISSN 0022-3263. doi:10.1021/jo00395a032.
- ^ Fries, K.; Finck, G. (1908). „Über Homologe des Cumaranons und ihre Abkömmlinge”. Chemische Berichte. 41 (3): 4271—4284. doi:10.1002/cber.190804103146.
- ^ Fries, K.; Pfaffendorf, W. (1910). „Über ein Kondensationsprodukt des Cumaranons und seine Umwandlung in Oxindirubin”. Chemische Berichte. 43 (1): 212—219. doi:10.1002/cber.19100430131.
- ^ March, J. Advanced Organic Chemistry, 3rd Ed.; John Wiley & Sons: Chichester, 1985; S. 499ff.
- ^ Blatt, A. H. Org. React. 1942, 1.
- ^ Organic Syntheses, Coll. Vol. 3, p.30 (1955); Vol. 29, p.2 (1949). Link
- ^ Organic Syntheses, Coll. Vol. 4, p.746 (1963); Vol. 38, p.78 (1958). Link
- ^ Organic Syntheses, Coll. Vol. 5, p.235 (1973); Vol. 43, p.17 (1963). Link
- ^ Bouveault, L.; Locquin, R. (1905). „Action du sodium sur les éthers des acides monobasiques à fonction simple de la série grasse” [Effect of sodium on the ethers of single-function monobasic acids of the fatty series]. Compt. Rend. (на језику: француски). 140: 1593—1595.
- ^ Finley, K. T. (1964). „The Acyloin Condensation as a Cyclization Method”. Chem. Rev. 64 (5): 573—589. doi:10.1021/cr60231a004.
- ^ Bloomfield, J. J.; Owsley, D. C.; Nelke, J. M. Org. React. 1976, 23.
- ^ Theodora W. Greene; Peter G. M. Wuts (1999). Protecting Groups in Organic Synthesis (3 изд.). J. Wiley. ISBN 978-0-471-16019-9.
- ^ Chan, Weng C.; White, Peter D. (2004). Fmoc Solid Phase Peptide Synthesis. Oxford University Press. ISBN 978-0-19-963724-9.