Pitka voda
Pitka voda, poznata i kao pijaća voda ili voda za piće, voda je koja je dovoljno sigurna za piće ili za pripremu hrane. Globalno, 2012. godine, 89% ljudi je imalo pristup vodi za piće.[1] Oko 4 milijarde ima pristup vodi iz česme, dok ostale 2,3 milijarde ima pristup izvorima ili javnim česmama.[1] Oko 1,8 milijardi ljudi još uvijek koristi nesigurnu vodu koja može biti kontaminirana izmetom.[1] Ovo može rezultirati upalnim oboljenjima digestivnog trakta kao što je kolera ili tifus.[1] Voda je neophodna za život. Količina vode potrebne za piće je promjenljiva.[2] Zavisi od fizičke aktivnosti, starosti, zdravstvenih problemima, kao i uslova sredine.[3][4] Voda čini oko 60% ukupne težine muškarca i oko 50% težine žene.[5] Novorođenčad imaju 70—80% vode, dok ona starija imaju oko 45%.[6]

Voda je u prirodi jako rasprostranjena, pokriva oko tri četvrtine Zemljine površine. Ukupna zapremina vode na Zemljinoj površini iznosi 1 360 000 000 km³, i to 98 procenata u okeanima i morima, 1.96 procenata u lednicima i snegu i 0.04 procenata u rekama, jezerima, podzemnoj i atmosferskoj vodi. Prema tome, za čoveka je ova poslednja stavka (0.04 procenata) najvažnija, a njoj odgovara ukupna količina slatke vode na Zemlji 544 000 km³. Potpuno čista voda ne nalazi se u prirodi; najčistija je atmosferska voda (prirodno destilovana voda), mada i ona sadrži, pored čestica prašine i sledeće sastojke: ugljen-dioksid, amonijum-nitrat, vodonik-peroksid, mikroorganizme itd. pH vrednost kišnice je oko 5,7 (zbog ugljene kiseline), ali može biti i manja (3,5-5), u zavisnosti od oksida u vazduhu koji su rastvorni u vodi (na primer SO2).
Prolazeći kroz razne slojeve Zemljine kore, voda rastvara mnoge supstance; zato se u rečnoj, bunarskoj i izvorskoj vodi nalazi oko 0.01 – 0.2 čvrstih supstanci, najvećim delom kalcijumovih i magnezijumovih jedinjenja. Morska voda sadrži oko 3.6 procenata rastvorenih supstanci, od čega na kuhinjsku so otpada najveći deo. Prirodne vode koje sadrže veću količinu kalcijumovih i magnezijumovih jedinjenja, zovu se tvrde vode, za razliku od mekih voda, koje sadrže malu količinu pomenutih jedinjenja. Tvrde vode su nezgodne za upotrebu, u njima se teško pere, nisu pogodne za kuvanje namirnica, ne smejuu da se upotrebe za parne kotlove, jer se na njihovim zidovima stvara kamenac, itd. One izvorske vode koje sadrže u sebi veću količinu rastvorenih nekih čvrstih i gasovitih supstanci, koje ne sadrži obična voda, mogu da se upotrebe za lečenje raznih oboljenja. Takve vode zovu se mineralne vode Prema supstancama koje se u njima nalaze rastvorene, dele se na slane (od NaCl), gorke (od magnezijumovih soli), kisele (od ugljen-oksida), gvožđevite (od rastvorenih soli gvožđa) itd.
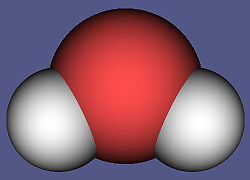
Voda za piće mora da bude čista, bez bakterija, da ima temperaturu od 12 – 15 °C i da je svežeg ukusa, koji jednim delom dolazi od rastvorenog ugljen-dioksida i kiseonika, a delom od rastvorenih čvrstih supstanci. Pošto veća naselja i gradovi ne mogu da se obezbede izvorskom vodom, ljudi su primorani da upotrebljavaju rečnu ili jezersku vodu. Da bi ova voda bila upotrebljiva za piće, mora da se očisti mehanički i hemijski. Nesumnjivo najvažniji od svih oksida, a možda i najvažnija od svih jedinjenja uopšte jeste voda.[7] Molekul vode je uglovni molekul sa uglom 104.5 stepeni između dve OH veze. Zbog velike razlike u elektronegativnosti između vodonika i kiseonika, molekul vode je izrazito dipolnog karaktera što je prikazano na slici 1. Time pozitivan kraj jednog molekula privlači negativan kraj drugog, što posredstvom vodoničnih veza dovodi do asocijacije molekula i u tečnom i u čvrstom agregatnom stanju. Fizičke osobine vode.
Oko 1 do 2 milijarde ljudi nema bezbednu vodu za piće.[8] Voda može prenositi vektore bolesti. Više ljudi umire od nebezbedne vode nego od rata, izjavio je svojevremeni U.N. generalni sekretar Ban Ki-mun 2010. godine.[9] Zemlje trećeg sveta su najviše pogođene nedostatkom vode, poplavama i kvalitetom vode. Do 80 procenata bolesti u zemljama u razvoju je direktna posledica neadekvatne vode i sanitarnih uslova.[10] Prema izveštaju UNICEF-a i Uneska, Finska ima najbolji kvalitet vode za piće na svetu.[11][12][13][14]
Čista voda
urediČista voda je na običnoj temperaturi providna tečnost, bez mirisa i ukusa, u tankim slojevima bezbojna, a u debljim slojevim je plave boje. Voda se pod normalnim pritiskom mrzne na 0 , a ključa na 100 °C, pretvarajući se u paru. Retko koja druga supstanca postoji u sva tri agregatna stanja, kao voda, na temperaturi uobičajenoj za normalni eksperimentalni rad. Potpuno čista voda gotovo da ne provodi električnu struju, ali prisustvo male količine ugljene kiseline ili neke soli, omogućava da se poveća njena provodljivost. Voda se, po svojim fizičkim osobinama, znatno razlikuje od osobina drugih supstanci.
Hemijske osobine vode
urediVoda spada u vrlo reaktivne supstance, reaguje sa najreaktivnijim metalima (kalijum, natrijum) na sobnoj temperaturi i gradi odgovarajuće baze. Sa manje aktivnim metalima, na višoj temperaturi, izdvaja se vodonik iz vodonik iz vodene pare. Sa nemetalima fluorom, hlorom i bromom reaguje na običnoj temperaturi, a na visokoj temperaturi reaguje sa ugljenikom. Sa metalnim oksidima voda gradi baze, a sa nemetalnim oksidima kiseline.
Zagađivanje vode
urediVoda je vrlo zagađena raznim materijalima koje potiču iz mnogobrojnih izvora. Otpadne vode gradova, kanalizacije gradova, izlivaju se u vode reka, jezera i mora. Veštačka đubriva i razni pesticidi, koje kiša spira sa oranica, takođe zagađuju vode; često se voda zagađuje naftom i njenim derivatima. U novije vreme, sve se više radi na sprečavanju izlivanja otpadnih voda u reke, jezera i mora, pre nego što se izvrši njihovo prečišćavanje pomoću specijalnih uređaja.
Hemijski sastav prirodnih voda
urediMikroorganizmi troše kiseonik, koji je rastvoren u vodi, razlažu organske supstance u prosta jedinjenja i elemente: CO2, H2O2, N2, N2O, SO2, C, H, O, S, P, Cl, Cu, Mg, K, Na. Osim njih ima i elemenata koji su prisutni u tragovima. To su tzv. Mikroelementi, koji su veoma važni, jer njihov suficit i deficit može imati za posledicu pojjavu mnogih oboljenja. Svi mikroelementi se mogu svrstati u tri grupe: Bitni mikroelementi, važni za ljudski organizam: Fe, Mn, Zn, Cu, I Netoksični elementi, ali nevažni za ljudski organizam: Al, Si, Sr, Ni Toksični mikroelementi, čiji tragovi su prisutni u vodi nemaju biološki značaj, ali njihovo unošenje u većim količinama, nema samo štetno, već i toksično dejstvo: Pb, F, Se, Br, Ag
Maksimalno dozvoljene koncentracije
urediU našoj zemlji zakonski su regulisane norme za maksimalno dozvoljene koncentracije zagađivača u vazduhu. Međutim, još uvek ne postoje takvi standardi za kontrolu vodene sredine, ali kao kriterijumi služe standardi koji se primenjuju u većini zemalja.[15]
Vidi još
urediReference
uredi- ^ a b v g „Water Fact sheet N°391”. jul 2014. Arhivirano iz originala 5. 6. 2015. g. Pristupljeno 24. 5. 2015.
- ^ Yamada, Yosuke; Zhang, Xueying; Henderson, Mary E. T.; Sagayama, Hiroyuki; Pontzer, Herman; Speakman, John R. (2022). „Variation in human water turnover associated with environmental and lifestyle factors”. Science (na jeziku: engleski). 378 (6622): 909—915. Bibcode:2022Sci...378..909I. PMC 9764345 . PMID 36423296. doi:10.1126/science.abm8668.
- ^ Grandjean, Ann C. (2004). „3”. Water Requirements, Impinging Factors, and Recommended Intakes (PDF). World Health Organization. str. 25—34.
- ^ Exposure Factors Handbook: 2011 Edition (PDF). National Center for Environmental Assessment. septembar 2011. Arhivirano iz originala (PDF) 24. 9. 2015. g. Pristupljeno 24. 5. 2015.
- ^ Miller, Thomas A. (2006). Modern surgical care physiologic foundations and clinical applications (3rd izd.). New York: Informa Healthcare. str. 34. ISBN 9781420016581.
- ^ Nancy caroline's emergency care in the streets. (07 izd.). [S.l.]: Jones And Bartlett Learning. 2012. str. 340. ISBN 9781449645861.
- ^ „Arhivirana kopija”. svet medicine. Arhivirano iz originala 01. 04. 2018. g. Pristupljeno 31. 3. 2018.
- ^ „Drinking-water”. World Health Organization. mart 2018. Pristupljeno 23. 3. 2018.
- ^ „Unsafe water kills more people than war, Ban says on World Day”. UN News. 22. 3. 2010. Pristupljeno 10. 5. 2018.
- ^ „Water in developing countries”. GAC. 12. 6. 2017. Pristupljeno 4. 10. 2021.
- ^ „WWDR1: Water for People – water for life” (PDF). UNESCO and Berghahn Books. 2003. Pristupljeno 21. 9. 2022.
- ^ „Water Is Enough Reason to Visit Finland, Here's Why”. Culture Trip. 4. 6. 2018. Pristupljeno 21. 9. 2022.
- ^ „Water in Finland purest in the world”. MEDI Connection. 22. 3. 2019. Pristupljeno 21. 9. 2022.
- ^ „The quality of water produced by Turku Region Water is rated the best in the world by Unesco”. City of Turku. 1. 12. 2021. Pristupljeno 21. 9. 2022.
- ^ „voda za piće-uticaj na zdravlje”. Arhivirano iz originala 26. 01. 2021. g. Pristupljeno 31. 03. 2018.
Literatura
uredi- Dr.Ivan Filipović,dr.Stjepan Lipanović,Opća i anorganska kemija,
- Opća i anorganska kemija - I. i II. dio Ivan Filipović, Stjepan Lipanović
- Stanja i procesi u životnoj sredini,grupa autora, fakultet za fizičku hemiju Beogradd 1955. godine
- Enciklopedija zaštite na radu, medicine i higijene rada,Institut zaštite na radu "edvard Kardelj" Niš
- Dr.Momčilo St.Mokrnjac, Toksikološka hemija, Univerzitet u Beogradu, 1972 godine
- Sadoff, Claudia; Grey, David; Borgomeo, Edoardo (2020). „Water Security”. Oxford Research Encyclopedia of Environmental Science. ISBN 978-0-19-938941-4. doi:10.1093/acrefore/9780199389414.013.609.
- Grey, David; Sadoff, Claudia W. (2007-12-01). „Sink or Swim? Water security for growth and development”. Water Policy (na jeziku: engleski). 9 (6): 545—571. ISSN 1366-7017. doi:10.2166/wp.2007.021. hdl:11059/14247.
- Global water security : lessons learnt and long-term implications. Singapore: World Water Council. 2018. ISBN 978-981-10-7913-9. OCLC 1021856401.
- Varady, Robert G.; Albrecht, Tamee R.; Staddon, Chad; Gerlak, Andrea K.; Zuniga-Teran, Adriana A. (2021). „The Water Security Discourse and Its Main Actors”. Handbook of Water Resources Management: Discourses, Concepts and Examples. str. 215—252. ISBN 978-3-030-60145-4. S2CID 236726731. doi:10.1007/978-3-030-60147-8_8.
- Bonnafous, Luc; Lall, Upmanu; Siegel, Jason (2017-04-19). „A water risk index for portfolio exposure to climatic extremes: conceptualization and an application to the mining industry”. Hydrology and Earth System Sciences (na jeziku: engleski). 21 (4): 2075—2106. Bibcode:2017HESS...21.2075B. doi:10.5194/hess-21-2075-2017 .
- „The Water Crisis and Industries at Risk”. Morgan Stanley (na jeziku: engleski). Pristupljeno 2020-04-06.
- Hoekstra, Arjen Y; Buurman, Joost; van Ginkel, Kees C H (2018). „Urban water security: A review”. Environmental Research Letters. 13 (5): 053002. doi:10.1088/1748-9326/aaba52 .
- Carr, Acacia (3. 12. 2018). „Water Risk: Single Largest Risk Threatening People, Planet and Profit | GreenMoney Journal” (na jeziku: engleski). Pristupljeno 2020-04-06.
- „Climate change is devastating the world's water supplies. Why aren't we talking about it?”. Climate & Capital Media (na jeziku: engleski). 2021-01-14. Pristupljeno 2021-01-15.
- „New Water Risk Filter Scenarios will help companies and investors turn risk into resilience”.
- Grasham, Catherine Fallon; Charles, Katrina Jane; Abdi, Tilahun Geneti (2022). „(Re-)orienting the Concept of Water Risk to Better Understand Inequities in Water Security”. Frontiers in Water. 3: 799515. doi:10.3389/frwa.2021.799515 .
- Vörösmarty, C. J.; McIntyre, P. B.; Gessner, M. O.; Dudgeon, D.; Prusevich, A.; Green, P.; Glidden, S.; Bunn, S. E.; Sullivan, C. A.; Liermann, C. Reidy; Davies, P. M. (septembar 2010). „Global threats to human water security and river biodiversity”. Nature (na jeziku: engleski). 467 (7315): 555—561. Bibcode:2010Natur.467..555V. PMID 20882010. S2CID 4422681. doi:10.1038/nature09440. hdl:10983/13924.
- Foster, S.; Villholth, Karen; Scanlon, B.; Xu, Y. (2021-07-01). „Water security and groundwater”. International Association of Hydrogeologists. hdl:10568/116815.
- Staddon, Chad; Scott, Christopher (2021). Putting water security to work : addressing global sustainable development challenges (1st izd.). London. ISBN 9780367650193.
- Caretta, M.A., A. Mukherji, M. Arfanuzzaman, R.A. Betts, A. Gelfan, Y. Hirabayashi, T.K. Lissner, J. Liu, E. Lopez Gunn, R. Morgan, S. Mwanga, and S. Supratid, 2022: Chapter 4: Water. In: Climate Change 2022: Impacts, Adaptation and Vulnerability. Contribution of Working Group II to the Sixth Assessment Report of the Intergovernmental Panel on Climate Change [H.-O. Pörtner, D.C. Roberts, M. Tignor, E.S. Poloczanska, K. Mintenbeck, A. Alegría, M. Craig, S. Langsdorf, S. Löschke, V. Möller, A. Okem, B. Rama (eds.)]. Cambridge University Press, Cambridge, UK and New York, NY, USA, pp. 551–712,„Water”. Climate Change 2022 – Impacts, Adaptation and Vulnerability. 2023. str. 551—712. ISBN 9781009325844. doi:10.1017/9781009325844.006..
Spoljašnje veze
uredi- U.S. Centers for Disease Control and Prevention (CDC) Healthy Water – Drinking Water One-stop resource for drinking water
- US Environmental Protection Agency – National drinking water program – General info, regulations & technical publications
- WHO – Water Sanitation and Health: drinking water quality