Алуминијум хлорид
Алуминијум хлорид AlCl3 је једна од најважнијих соли алуминијума, која налази примену у органским синтезама.[3][4] Алуминијум хлорид је веома добро растворљив. Ово једињење показује веома јаке киселе особине. Релативна атомска маса овог једињења износи приближно 133,34

| |
| |
| Називи | |
|---|---|
| IUPAC назив
Алуминијум(III)-хлорид
| |
| Други називи
Алуминијум-трихлорид
| |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.028.371 |
| MeSH | Aluminium+chloride |
| UNII | |
| |
| |
| Својства | |
| AlCl3 | |
| Моларна маса | 133,34 g mol−1 (анхидрован) 241.432 g mol−1 (хексахидрат) |
| Агрегатно стање | бледожута чврста супстанца, хигроскопна супстанца. |
| Густина | 2,48 g cm−3 |
| Тачка топљења | 190°C 463 K) испод 2.5 atm притиска |
| Тачка кључања | 178°C (451 K) (сублимира) |
| 43.9 g/100 ml (0°C) 44.9 g/100 ml (10°C) 45.8 g/100 ml (20°C) 46.6 g/100 ml (30°C) 47.3 g/100 ml (40°C) 48.1 g/100 ml (60°C) 48.6 g/100 ml (80°C) 49 g/100 ml (100°C) | |
| Структура | |
| Кристална решетка/структура | 6-координатна положена решетка |
| Геометрија молекула | октаедар (основно стање) тетраедар (течност) |
| Облик молекула (орбитале и хибридизација) | тригонална планарна (мономер у стању паре) |
| Опасности | |
ЕУ класификација (DSD)
|
Корозиван (C) |
| R-ознаке | R34 |
| S-ознаке | (S1/2), S7/8, S28, S45 |
| Сродна једињења | |
Други анјони
|
Алуминијум-флуорид Алуминијум-бромид Алуминијум-јодид |
Други катјони
|
Бор-трихлорид Галијум(III)-хлорид Индијум(III)-хлорид Талијум(III)-хлорид Магнезијум-хлорид |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |

Структура
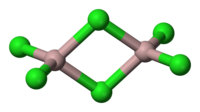
уредиАлуминијум хлорид се састоји од једног атома алуминијума са оксидационим бројем +3 и од три атома хлора са оксидационим бројем -1.
Налази се у чврстом агрегатном стању
Извори
уреди- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Lide David R., ур. (2006). CRC Handbook of Chemistry and Physics (87th изд.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ Susan Budavari, ур. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th изд.). Merck Publishing. ISBN 0911910131.
Литература
уреди- Holleman A. F.; Wiberg E. (2001). Inorganic Chemistry (1st изд.). San Diego: Academic Press. ISBN 0-12-352651-5.
- Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. изд.). Prentice Hall. ISBN 978-0-13-175553-6.