Сублимација (физика)
Сублимација је директни прелазак супстанце из чврстог у гасовито агрегатно стање без течног међустања.[1] Сублимација је (у физици) један од фазних прелаза. Сублимација је ендотермни процес који се одвија на температурама и притисцима испод тројне тачке супстанце у њеном фазном дијаграму, што одговара најнижем притиску при коме супстанца може постојати као течност. Обрнути процес од сублимације је десублимација, при чему супстанца прелази директно из гаса у чврсту фазу.[2] Сублимација се такође користи као генерички израз за опис преласка из чврстог стања на гас (сублимација), након чега следи прелаз гас-чврсто стање (десублимација).[3] Док се прелазак из течности у гас описује као испаравање ако се одвија испод тачке кључања течности, и као кључање ако се одвија на тачки кључања, не постоји таква разлика у прелазу из чврстог стања до гасовито, већ се оно увек назива сублимацијом.

При нормалним притисцима, већина хемијских једињења и елемената имају три различита стања на различитим температурама. У тим случајевима, за прелазак из чврстог у гасовито стање потребно је средње течно стање. Наведени притисак је парцијални притисак супстанце, а не укупни (нпр. атмосферски) притисак целог система. Стога, све чврсте материје које имају значајан напон паре на одређеној температури обично могу да сублимирају у ваздуху (нпр. водени лед мало испод 0 °C). За неке супстанце, као што су угљеник и арсен, сублимација је много лакша од испаравања из отопине, јер је притисак њихове тројне тачке веома висок, па их је тешко добити као течност.
Израз сублимација односи се на физичку промену стања и не користи се за описивање претварања чврсте супстанце у гас у хемијској реакцији. На пример, дисоцијација при загревању чврстог амонијум хлорида у хлороводоник и амонијак није сублимација, већ хемијска реакција. Слично томе сагоревање свећа, које садрже парафински восак, до угљен диоксида и водене паре, није сублимација, већ хемијска реакција са кисеоником.
Сублимација настаје апсорпцијом топлоте која пружа довољно енергије неким молекулама да превазиђу привлачне силе својих суседа и побегну у фазу паре. С обзиром да процес захтева додатну енергију, то је ендотермна промена. Енталпија сублимације (која се такође назива топлота сублимације) може се израчунати сабирањем енталпије топљења и енталпије испаравања.
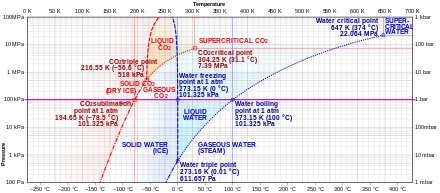
Услови
уредиОд четири агрегатна стања, при нормалном притиску, супстанце се, на различитим температурама, налазе у једном од три стања. Притом, прелазак из чврстог у гасовито стање захтева течно међустање. Код сублимације се оно не јавља. Супстанце које лако сублимују по правилу имају висок напон паре и при нормалним условима.
Значај
уредиОва особина се примењује у хемији за пречишћавање супстанци, нарочито када је кристализацијом то знатно отежано.
Методе
уреди1 довод хладне воде 2 одвођење хладне воде 3 вакуум 4 посуда за сублимацију 5 супстанца која се кристализује 6 супстанца која сублимише 7 спољно загревање
У најпростијем случају сублимација може да се изведе са два сахатна стакла исте величине. Између њих стави се хартија за цеђење нешто већег пречника и по средини избушена. Жељена супстанца се стави на доње стакло и оба стакла се причврсте штипаљком. Доње се стакло полако загрева на пешчаном или воденом купатилу при чему се пара супстанце у додиру са хладном површином сахатног стакла претвара у ситне кристале. Већи ефекат се постиже када се горње стакло хлади влажном хартијом или крпом. Постављена хартија спречава да кристали падну на доње врело стакло.
Веће количине супстанце се пречишћавају тако што се уместо сахатних стакала користе порцеланске шоље, епрувете, лончићи, реторте и друго посуђе.
Примери
уредиУ лабораторији се често врши сублимација сумпора, јода, амонијум-хлорида и других супстанци. Неке супстанце сублимују при нормалним условима. Примери за то су јод и угљеник-диоксид (суви лед - CO2 у чврстом стању - прелази у гас без топљења). То се дешава и са обичним ледом, (односно залеђеном водом).
Угљен диоксид
уредиЧврсти угљен диоксид (суви лед) сублимира на температурама испод тројне тачке (нпр., на температури од −78,5 °C (194,65 K, −109,30 °F) на атмосферском притиску, док се његово топљење у течни CO2 може јавити само при притиску и температурама изнад тројне тачке (тј. 5,2 atm, −56,4 °C).
Вода
уредиСнег и лед сублимирају, мада спорије, на температурама испод температуре замрзавања/топљења од 0 °C на већини притисака; погледајте линију испд тројне тачке.[4] При сушењу замрзавањем, материјал који се дехидрира се замрзава, и води се дозвољава да сублимира под сниженим притиском или вакуумом. Губитак снега са снежног поља током хладног периода често је узрокован сунчевим сјајем које делује директно на горње слојеве снега. Аблација је процес који обухвата сублимацију и ерозивно трошење ледењачког леда.
Нафтален
уредиНафтален, органско једињење које се често присутно у пестицидима као што су куглице против мољаца, лако сублимира јер је направљено од неполарних молекула који се држе заједно само ван дер Валсовим интермолекуларним силама. Нафтален је чврста супстанца која се сублимира на стандардној атмосферској температури[5] са тачком сублимације на око 80 °C.[6] При ниској температури његов напон паре је довољно висок, 1 mmHg на 53 °C,[7] да чврсти облик нафталена испарава у гас. На хладним површинама, испарења нафталена ће се очврснути да би формирала кристале налик на игле.
Друге супстанце
уредиЈод ствара димове при лаганом загревању. Течни јод је могуће добити под атмосферским притиском, контролисањем температуре мало изнад тачке топљења јода. У судској медицини, јодна пара може открити латентне отиске прстију на папиру.[8] Арсен такође може да сублимира при високим температурама.
Кадмијум и цинк нису подесни материјали за употребу у вакууму јер они сублимирају знатно више од других често кориштених материјала.
Пречишћавање сублимацијом
уредиСублимација је техника коју хемичари користе за прочишћавање једињења. Чврста супстанца се обично ставља у апарат за сублимацију и греје под вакуумом. Под овим смањеним притиском, чврста супстанца се испарава и кондензује као пречишћено једињење на охлађеној површини (хладни прст), остављајући неиспарљиви остатак од нечистоћа иза себе. Једном када грејање престане и вакуум се уклони, пречишћено једињење се може прикупити са хлађене површине.[9][10] Ради још веће ефикасности пречишћавања примењује се градијент температуре, који такође омогућава одвајање различитих фракција. Уобичајена поставка користи евакуисану стаклену цев која се постепено загрева на контролисан начин. Проток материјала је од врућег краја, где се поставља почетни материјал, до хладног краја који је повезан са постољем пумпе. Путем контролисања температура дуж цеви, оператер може да контролише зоне поновне кондензације, при чему се врло испарљива једињења потпуно избацују из система (или их хвата посебна хладна замка), умерено испарљива једињења се поново кондензују дуж цеви сходно њиховим различитим испарљивостима, а неиспарљива једињења остају на врућем крају. Вакуумска сублимација овог типа такође је метода избора за прочишћавање органских једињења за употребу у индустрији органске електронике, где су потребне веома високе чистоће (често > 99,99%) да би се задовољили стандарди за потрошачку електронику и друге примене.
Историјска употреба
уредиУ древној алхемији, протонауци која је допринела развоју савремене хемије и медицине, алхемичари су развили структуру основних лабораторијских техника, теорије, терминологије и експерименталних метода. Сублимација је коришћена за означавање процеса у коме се супстанца загрева до испарења, затим се одмах сакупља као седимент на горњем делу и врату грејног медијума (обично реторта или алембик), али се такође може користити за описивање других сличних нелабораторијских прелаза. Спомињу је алхемијски аутори као што су Базил Валентин и Џорџ Рипли, а поменута је и у Филозофској бројаници, као процес неопходан за довршавање магнум опуса. Овде се реч сублимација користи за опис размене „тела” и „духова” слично лабораторијском фазном прелазу између чврстих материја и гасова. Валентин је у свом раду Triumphal Chariot of Antimony (објављеном 1678. године) упоређује са радњом у којој се сублимација поврћа може користити за раздвајање алкохола у вину и пиву.[11] Рипли користи језик који више указује на мистичне импликације сублимације, што указује на то да процес има двоструки аспект у подуховљавању тела и корпорализацији духа.[12][13]
Предвиђање сублимације
уредиЕнталпија сублимације се обично предвиђа коришћењем еквипартиционе теореме. Ако се претпостави да је енергија решетке приближно једнака половини енергије паковања, тада се могу применити следеће термодинамичке корекције за предвиђање енталпије сублимације. Узимајући да 1 моларни идеални гас пружа корекцију термодинамичког окружења (притиска и запремине) у којем је pV = RT, добија се корекција 1RT. Затим је потребно применити додатне корекције за вибрацију, ротацију и транслацију. Из еквипартиционе теореме следи да гасна ротација и транслација доприносе по 1,5 RT финалном стању, те се добија корекција од +3RT. Кристалне вибрације и ротације доприносе 3RT свака иницијалном стању, дакле –6RT. Сумирањем RT корекција добија се −6RT + 3RT + RT = −2RT.[14] То доводи до следеће приближне енталпије сублимације. Слична апроксимација се може наћи за ентропијски члан, ако се претпоставе крута тела.[15][16]
Види још
уредиРеференце
уреди- ^ „Sublimate”. Merriam-Webster Dictionary.
- ^ Boreyko, Jonathan B.; Hansen, Ryan R.; Murphy, Kevin R.; Nath, Saurabh; Retterer, Scott T.; Collier, C. Patrick (2016). „Controlling condensation and frost growth with chemical micropatterns”. Scientific Reports. 6: 19131. Bibcode:2016NatSR...619131B. PMC 4726256 . PMID 26796663. doi:10.1038/srep19131.
- ^ „Sublime”. Dictionary.com Unabridged. Random House.
- ^ Fassnacht, S. R. (2004). „Estimating Alter-shielded gauge snowfall undercatch, snowpack sublimation, and blowing snow transport at six sites in the coterminous USA”. Hydrol. Process. 18 (18): 3481—3492. Bibcode:2004HyPr...18.3481F. doi:10.1002/hyp.5806.
- ^ Caroll, J. (2014). Natural Gas Hydrates. стр. 16. ISBN 9780128005750.
- ^ Staff writer(s) (2015). „what solid go through sublimation?”. National Science Foundation and UCSB School-University partnership. Приступљено 13. 11. 2015.
- ^ Pavia, D. (2005). Introduction to organic laboratory technique. стр. 781–782. ISBN 978-0534408336.
- ^ Girard, James (2011). Criminalistics: Forensic Science, Crime and Terrorism. Jones & Bartlett Learning. стр. 143–144. ISBN 978-0-7637-7731-9.
- ^ R. B. King Organometallic Syntheses. Volume 1 Transition-Metal Compounds; Academic Press: New York, (1965). ISBN 0-444-42607-8.
- ^ Harwood, Laurence M.; Moody, Christopher J. (1989). Experimental organic chemistry: Principles and Practice (Illustrated изд.). WileyBlackwell. стр. 154–155. ISBN 978-0-632-02017-1.
- ^ Barrett, Francis (1815). The lives of alchemystical philosophers: with a critical catalogue of books in occult chemistry, and a selection of the most celebrated treatises on the theory and practice of the hermetic art. Macdonald and Son for Lackington, Allen, & Co. стр. 233.
- ^ DiBernard, Barbara (1980). Alchemy and Finnegans wake. SUNY Press. стр. 57. ISBN 978-0873953887.
- ^ Ripley, George (1591). Compound of Alchemy Архивирано на сајту Wayback Machine (11. мај 2023).
- ^ Gavezzotti, A. (1997). Theoretical Aspects and Computer Modeling of the Molecular Solid State. Chichester: Wiley and Sons.
- ^ McDonagh, J. L.; Nath; De Ferrari, Luna; Van Mourik, Tanja; Mitchell, John B. O. (2014). „Uniting Cheminformatics and Chemical Theory To Predict the Intrinsic Aqueous Solubility of Crystalline Druglike Molecules”. Journal of Chemical Information and Modeling. 54 (3): 844—56. PMC 3965570 . PMID 24564264. doi:10.1021/ci4005805.
- ^ McDonagh, James; Palmer, David S.; Van Mourik, Tanja; Mitchell, John B. O. (17. 10. 2016). „Are The Sublimation Thermodynamics of organic molecules predictable?” (PDF). Journal of Chemical Information and Modeling. 56 (11): 2162—2179. ISSN 1549-9596. PMID 27749062. doi:10.1021/acs.jcim.6b00033. hdl:10023/11874.
Литература
уреди- Нешић, С. & Вучетић, Ј. 1988. Неорганска препаративна хемија. Грађевинска књига: Београд.
- Челонер, Џ. 2001. Визуелни речник физике. „NNK International“: Београд.