Т-ћелија
Т ћелије или Т лимфоцити су тип лимфоцита (подтипа белих крвних зрнаца) који имају централну улогу у ћелијском имунитету. Од других лимфоцита, као што су Б ћелије и природних ћелија убица, разликују се по присуству рецептора Т ћелија на површини ћелије. Оне се називају Т ћелијама, јер сазревају у тимусним тимоцитима[1][2] (неке такође сазревају у крајницима.[3]). Од неколико подскупова Т ћелија, сваки има различите функције. Већина људских Т ћелија које преуређују своје алфа и бета ланце на ћелијском рецептору, називају се алфа и бета Т ћелије (αβ Т ћелије) и део су у адаптивног имунитета. Специјализиране гама делта ћелије, (мали број Т ћелија у људском телу, много чешће код преживара), имају неварирајуће рецепторе Т лимфоцита, с ограниченом разноликости, који се могу ефективно представљати путем антигена другим Т ћелијама,[4] и сматрају се делом урођеног имунског система.
| Т-ћелија (Лyмпхоцyтус Т) | |
|---|---|
 Т-ћелија под скенирајућим електронским микроскопом | |
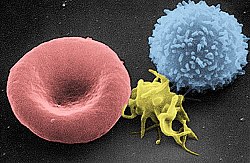 Т-лимфоцит (десно), тромбоцит (центар) и црвена крвна зрнца (лево) | |
| Детаљи | |
| Систем | Имунски систем |
| Показатељи | |
| Код | ТХ Х2.00.04.1.02007 |
| ТХ | Х2.00.04.1.02007 |
| ФМА | 62870 |
| Анатомска терминологија | |

Типови
уредиПомоћне ћелије
уредиТ помоћне ћелије (ТХћелије) помажу осталим белим крвним ћелијама у имунским процесима, укључујући сазревање Б ћелија у плазмоците и меморијске Б ћелије, те активацији цитотоксичних Т ћелија и макрофага. Ове ћелије су такође познате као ЦД4+ Т ћелије, због испољавања ЦД4 гликопротеина на површини. Хелпер Т ћелије постају активне када се презентирају пептидним антигенима молекула МХЦ II класе, које се испољавају на површини антиген-презентирајућих ћелија (АПЦ).[1] Једном активиране, брзо се деле и луче мале протеине зване цитокини, који регулишу или помажу активни имунски одговор. Ове ћелије се могу диференцирати у један од неколико подтипова, укључујући ТХ1, ТХ2, ТХ3, ТХ17, ТХ9, или ТФХ, које луче различите цитокине имунског одговора. Сигнализација из АПЦ усмерава Т ћелије у посебне подстипове.
Цитотоксичне Т ћелије
уредиЦитотоксичне Т ћелије (ТC ћелије или ЦТЛ) уништавају ћелије које су инфициране вирусима и туморске ћелије, а такође учествују и у реакцијама на трансплантацији органа. Ове ћелије су такође познате и као ЦД8+ Т ћелије, јер на површини испољавају ЦД8 гликопротеин. Ове ћелије препознају своје циљеве путем везања за антиген који је асоциран са молекулама МХЦ класе I, које се испољавају на површини нуклеираних ћелија. Током секреције ИЛ-10, аденозина и осталих молекула које се луче путем регулацијских Т ћелија, ЦД8+ ћелије могу прећи у неактивно стање које превенира аутоимунске болести.[1]
Меморијске Т ћелије
уредиМеморијске Т ћелије су подскуп антиген – специфичних Т ћелија које трају дугорочно након савладавања инфекције.[1] Оне се брзо проширују на велики број ефекторских Т ћелија на поновно испољавање свог сродног антигена, омогућавајући да се имунски "меморише" активност против прошлих инфекција.[5] Меморијске Т ћелије обухватају три подтипа:
- централне меморијске Т ћелије(ТCM ћелије),
- ефекторске меморијске Т ћелије (ТЕМ ћелије) и ТЕМРА ћелије,[6] те
- резидентне меморијске Т ћелије (ТРМ).[7]
Супресорске ћелије
уредиСупресорске Т ћелије су кључне за одржавање имунске толеранције. Њихова главна улога је да угасе имуност која је посредована Т ћелијама, крајем имунске реакције и да сузбију аутореактивне Т ћелије које су избегле процес негативне селекције у тимусу.[1] Супресорске Т ћелије, уз помоћне ћелије, могу се заједнички назвати регулаторским Т ћелијама.
Описане су две главне класе ЦД4+ Трегћелија — ФОXП3+ Трег и ФОXП3− Трег ћелије.
Регулаторне Т ћелије могу настати у било током нормалног развоја у тимусу, када су познате као тимусне Трег ћелије, или могу бити периферно индуковане и називају се периферно изведене Трег ћелије. Ова два подскупа су раније била називана "природни" и "адаптивни" или "индуковани".[8] За оба подскупа је неопходно изражавање транскрипционог фактора ФОXП3, који се може употребити за идентификацију ћелија. Мутације ФОXП3 гена могу да спрече развиће регулаторних Т ћелија, узрокујући фаталне аутоимунске болести ИПЕX.
Неколико других врста Т ћелија имају супресивну активност, али не изражавају ФОXП3. Ова група обухвата Тр1 и Тх3 ћелије, за које се сматра да настају током имунског одговора и актом производње супресивних молекула. Тр1 ћелије су повезане са ИЛ-10, Тх3 ћелије су повезани са ТГФ-бета. Недавно су на ову листу додате и Трег17 ћелије.[9]
Природне ћелије убице
уредиПриродне Т ћелијске убице (НКТ ћелије - не треба мешати са природним ћелијама убицама урођеног имунског система) премошћавају адаптивни и урођени имунски систем. За разлику од конвенцијских Т ћелија, које препознају пептидне антигене презентиране молекулама главног комплекса хистокомпатибилности (МХЦ), НКТ ћелије препознају гликолипидне антигене представљене молекулама под називом ЦД1д. Када се активирају, ове ћелије могу обављати функције које се приписују и Тх и ТC ћелијама (тј. производњу цитокина и ослобађање цитолитичких/ћелијских смртоносних молекула). Такође имају способност да препознају и уклоне неке туморске ћелије и ћелије заражене херпес вирусима.
Неваријантне слузокожне ћелије
уредиСлузокожно повезани инваријантни Т лимфоцити (МАИТ) су посебна врста Т ћелија, чије постојање је објављено 2009.[10][11][12][13]
Гама делта Т ћелије
уредиГама Делта Т ћелије (γδ Т-лимфоцити) представљају мали подскуп Т ћелија које на површини имају посебан рецептор Т ћелије (ТЦР). Већина Т ћелија има рецептор Т ћелија који се састоји од два гликопротеинска ланца, који се зову α- и β-ТЦР ланци. Међутим, код γδ Т-лимфоцитима, ТЦР се састоји од по једног γ-ланца и δ-ланца. Ова група Т ћелија је мање уобичајена код људи и мишева (око 2% од укупног броја Т лимфоцита). Налазе се углавном у слузокожи црева, унутар популације лимфоцита познате као интраепителни лимфоцити. Код кунића, оваца и кокошки, број γδ Т ћелија може бити висок и око 60% од укупног броја Т лимфоцита. Антигени молекули који активирају γδ Т ћелије су још увек углавном непознати.
Међутим, γδ Т ћелије нису МХЦ ограничене и сматра се да су у стању да препознају целе протеине уместо регулаторних пептида представљених МХЦ молекулима на АПЦ. Неке γδ Т ћелије глодара препознају МХЦ класу ИБ молекула, док људске Вγ9/Вδ2 Т ћелије, које чине највећи број γδ Т лимфоцита у периферној крви, су јединствене по томе што специфично и брзо одговарају на низ непептидних фосфорилисиних изопреноидних прекурсора, заједничког назива фосфоантигени, који се производе у готово свим живим ћелијама. Најчешћи фосфоантигени животињских и људских ћелија (укључујући и ћелије рака) су изопентенил пирофосфати (ИПП) и његов изомер диметилалил пирофосфат (ДСПП). Многи микроби производе веома активно једињеје хидрокси-ДМАПП (ХМБ-ПП) и одговарајуће мононуклеотидне коњугате, поред ИПП и ДМАПП. Биљне ћелије производе оба типа фосфоантигена. Људске Вγ9/Вδ2 Т ћелије које се активирају лековима, садрже синтетске фосфоантигене и аминобисфосфонате, који регулишу ендогени ИПП/ДМАПП.
Генетичко инжењерство
уреди2015. године, тим истраживача предвођен Александером Марсоном[14] на Универзитету Калифорније у Сан Франциску, успешно је едитовао геном људских Т ћелија применом Цас9 рибонуклеопротеинског метода испоруке.[15] Овај напредак има потенцијал за примену у лечењу „имунотерапије рака и терапије на бази ћелија за ХИВ, примарног недостатка имуности и аутоимуних болести“.[15]
Поремећаји
уредиНедостаци
уредиУзроци недостатака Т ћелија укључују лимфоцитопенију Т ћелија и/или недостатке функције појединих Т ћелија. Комплетна инсуфицијенција функције Т лимфоцита може резултирати због наследних стања, као што су тешка комбинована имунодефицијенција (СЦИД), Оменов синдром и хипоплазија хрскавице и косе. Узроци парцијалних недостатака функције Т лимфоцита укључују синдром стечене имунодефицијенције (АИДС), и наследне промене, као што су синдром Ди Џорџа (ДГС), синдром хромозомске нестабилности (ХБСД), и Б-ћелијски и Т-ћелијски комбиновани поремећаји, као што су атаксија-телеангиектатика (АТ) и Вискот-Алдричов синдром (WАС).
Главни забрињавајући патогени Т лимфоцита укључују интрацелуларне патогене, као што су Херпес симплеx вирус, Мyцобацтериум и Листериа.[16][17] При недостатку Т ћелија, такође су уобичајене и гљивичне инфекције.
Канцер
уредиКанцер Т ћелија се назива лимфомом Т-ћелија, и узрок је једне десетине случајева Нехоџкинсовог лимфома.[18]
Главни облици лимфома Т ћелије су:
Види још
уредиРеференце
уреди- ^ а б в г д Хаџиселимовић Р, Појскић Н (2005). Увод у хуману имуногенетику. Сарајево: Институт за генетичко инжењерство и биотехнологију (ИНГЕБ). ИСБН 9958-9344-3-4.
- ^ Албертс Б, Јохнсон А, Леwис Ј, Рафф M, Робертс к, Wалтер П (2002) Молецулар Биологy оф тхе Целл. Гарланд Сциенце: Неw Yорк, НY пг 1367. "Т целлс анд Б целлс дериве тхеир намес фром тхе органс ин wхицх тхеy девелоп. Т целлс девелоп ин тхе тхyмус, анд Б целлс, ин маммалс, девелоп ин тхе боне марроw ин адултс ор тхе ливер ин фетусес."
- ^ МцЦлорy, Сусан; Хугхес, Тиффанy; Фреуд, Ахарон Г.; Бриерцхецк, Едwард L.; Мартин, Цхелсеа; Тримболи, Антхонy Ј.; Yу, Јианхуа; Зханг, Xиаоли; Леоне, Густаво (2012). „Евиденце фор а степwисе програм оф еxтратхyмиц Т целл девелопмент wитхин тхе хуман тонсил”. Тхе Јоурнал оф Цлиницал Инвестигатион. 122 (4): 1403—1415. ИССН 1558-8238. ПМЦ 3314444 . ПМИД 22378041. дои:10.1172/ЈЦИ46125.
- ^ Вантоуроут, Пиерре; Хаyдаy, Адриан (2013). „Сиx-оф-тхе-бест: униqуе цонтрибутионс оф γδ Т целлс то иммунологy”. Натуре Ревиеwс. Иммунологy. 13 (2): 88—100. ИССН 1474-1741. ПМЦ 3951794 . ПМИД 23348415. дои:10.1038/нри3384.
- ^ Акбар АН, Террy L, Тиммс А, Беверлеy ПЦ, Јаноссy Г (1988). „Лосс оф ЦД45Р анд гаин оф УЦХЛ1 реацтивитy ис а феатуре оф примед Т целлс”. Ј. Иммунол. 140 (7): 2171—8. ПМИД 2965180.
- ^ Wиллингер Т, Фрееман Т, Хасегаwа Х, МцМицхаел АЈ, Цаллан МФ (2005). „Молецулар сигнатурес дистингуисх хуман централ меморy фром еффецтор меморy ЦД8 Т целл субсетс.”. Јоурнал оф Иммунологy. 175 (9): 5895—903. ПМИД 16237082. дои:10.4049/јиммунол.175.9.5895.
- ^ Схин, Хаина; Иwасаки, Акико (2013-09-01). „Тиссуе-ресидент меморy Т целлс”. Иммунологицал Ревиеwс. 255 (1): 165—181. ИССН 1600-065X. ПМЦ 3748618 . ПМИД 23947354. дои:10.1111/имр.12087.
- ^ Аббас АК, Беноист C, Блуестоне ЈА, Цампбелл ДЈ, Гхосх С, Хори С, Јианг С, Куцхроо ВК, Матхис D, Ронцароло МГ, Руденскy А, Сакагуцхи С, Схевацх ЕМ, Вигнали ДА, Зиеглер СФ (2013). „Регулаторy Т целлс: рецоммендатионс то симплифy тхе номенцлатуре”. Нат. Иммунол. 14 (4): 307—8. ПМИД 23507634. дои:10.1038/ни.2554.
- ^ Сингх Б, Сцхwартз ЈА, Сандроцк C, Беллеморе СМ, Никоопоур Е (2013). „Модулатион оф аутоиммуне дисеасес бy интерлеукин (ИЛ)-17 продуцинг регулаторy Т хелпер (Тх17) целлс”. Индиан Ј. Мед. Рес. 138 (5): 591—4. ПМЦ 3928692 . ПМИД 24434314.
- ^ Серриари НЕ, Еоцхе M, Ламотте L, Лион Ј, Фумерy M, Марцело П, Цхателаин D, Барре А, Нгуyен-Кхац Е, Лантз О, Дупас ЈЛ, Треинер Е (2014). „Иннате муцосал-ассоциатед инвариант Т (МАИТ) целлс аре ацтиватед ин инфламматорy боwел дисеасес”. Цлин. Еxп. Иммунол. 176: 266—74. ПМЦ 3992039 . ПМИД 24450998. дои:10.1111/цеи.12277.
- ^ МР1 антиген пресентатион то муцосал-ассоциатед инвариант Т целлс wас хигхлy цонсервед ин еволутион. 2009
- ^ Иннате Т целлс детецт бацтериа. Бацтериа, муцосал-ассоциатед инвариант Т целлс анд МР1. 2010
- ^ Кјер-Ниелсен L, Пател О, Цорбетт АЈ, Ле Ноурс Ј, Меехан Б, Лиу L, Бхати M, Цхен З, Костенко L, Реантрагоон Р, Wиллиамсон НА, Пурцелл АW, Дудек НЛ, МцЦонвилле МЈ, О'Хаир РА, Кхаираллах ГН, Годфреy DI, Фаирлие ДП, Россјохн Ј, МцЦлускеy Ј (2012). „МР1 пресентс мицробиал витамин Б метаболитес то МАИТ целлс”. Натуре. 491: 717—23. ПМИД 23051753. дои:10.1038/натуре11605.
- ^ http://www.independent.co.uk/news/science/crispr-breakthrough-announced-in-technique-of-editing-dna-to-fight-off-deadly-illnesses-10420050.html. Недостаје или је празан параметар
|title=(помоћ) - ^ а б Schumann, Kathrin; Lin, Steven; Boyer, Eric; Simeonov, Dimitre R.; Subramaniam, Meena; Gate, Rachel E.; Haliburton, Genevieve E.; Ye, Chun J.; Bluestone, Jeffrey A. (2015). „Generation of knock-in primary human T cells using Cas9 ribonucleoproteins”. Proceedings of the National Academy of Sciences of the United States of America. 112 (33): 10437—10442. ISSN 1091-6490. PMC 4547290 . PMID 26216948. doi:10.1073/pnas.1512503112.
- ^ Medscape > T-cell Disorders. Author: Robert A Schwartz, MD, MPH; Chief Editor: Harumi Jyonouchi, MD. Updated: May 16, 2011
- ^ Jones J, Bannister BA, Gillespie SH, ур. (2006). Infection: Microbiology and Management. Wiley-Blackwell. стр. 435. ISBN 1-4051-2665-5.
- ^ „The Lymphomas” (PDF). The Leukemia & Lymphoma Society. 2006. стр. 2. Архивирано из оригинала (PDF) 06. 07. 2008. г. Приступљено 07. 04. 2008.
Dodatna literatura
уреди- Davies AJ (1993). „The tale of T cells”. Immunology Today. 14 (3): 137—139. PMID 8466629. doi:10.1016/0167-5699(93)90216-8.
Spoljašnje veze
уреди- Immunobiology, 5th Edition
- „niaid.nih.gov” (PDF). Архивирано из оригинала (PDF) 25. 06. 2009. г. – The Immune System
- „T-cell Group – Cardiff University”. Архивирано из оригинала 11. 12. 2018. г.
- „(Successful!) Treatment of Metastatic Melanoma with Autologous CD4+ T Cells against NY-ESO-1”. Архивирано из оригинала 05. 01. 2010. г..