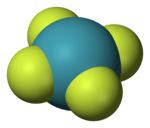
Ksenon-tetrafluorid
Ksenon-tetrafluorid je hemijsko neorgansko jedinjenje hemijske formule XeF4.

| |||
| |||
| Nazivi | |||
|---|---|---|---|
| IUPAC naziv
Ksenon-tetrafluorid
| |||
| Drugi nazivi
Ksenon(IV)-fluorid
| |||
| Identifikacija | |||
| ECHA InfoCard | 100.033.858 | ||
| MeSH | Xenon+tetrafluoride | ||
| Svojstva | |||
| XeF4 | |||
| Molarna masa | 207,2836 g mol−1 | ||
| Agregatno stanje | bela čvrsta supstanca | ||
| Gustina | 4,040 g cm−3, основно | ||
| Tačka ključanja | 117 °C (390 K) | ||
| Struktura | |||
| Geometrija molekula | D4h | ||
| Oblik molekula (orbitale i hibridizacija) | pravougla planarna geometrija molekula | ||
| Dipolni moment | 0 D | ||
| Opasnosti | |||
| Tačka paljenja | ? °C | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |||
| Reference infokutije | |||
Dobijanje
urediMože se dobiti prevođenjem smeše ksenona i fluora u odnosu 1:5 kroz cev od nikla zagrejanu na temperaturi od 400 °C i naglim hlađenjem dobijenog produkta.[1]
Svojstva
urediOvo je bezbojna do bela čvrsta supstanca. Rastvara se u fluorovodoničnoj kiselini. U vodi disproporcioniše na elementarni ksenon i jedinjenja ksenona koja zaostaju u rastvoru, gde mu je oksidacioni broj +6. Kada se taj rastvor ispari, dobija se ksenon-trioksid.[1]
Reference
uredi- ^ a b Filipović I. & Lipanović, S. (1982.) Opća i anorganska kemija. Školska knjiga: Zagreb.
Vidi još
urediSpoljašnje veze
uredi