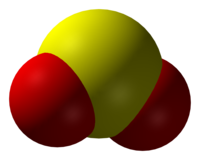
Sumpor-dioksid
Sumpor-dioksid (molekulska formula SO2) je bezbojni gas zagušljivog mirisa koji nastaje spaljivanjem sumpora na vazduhu. Teži je od vazduha. Rastvara se u vodi. Rastvor koji nastaje je kiseo jer gas reaguje sa vodom gradeći sumporastu kiselinu (H2SO3) čime se dokazuje da je sumpor-dioksid kiseli oksid. Sumporasta kiselina je nestabilna i lako se ponovo razlaže na sumpor-dioksid i na vodu.[2]

| |
| |
| Nazivi | |
|---|---|
| Drugi nazivi
sumpor(IV)-oksid; anhidrid sumporaste kiseline
| |
| Identifikacija | |
| ECHA InfoCard | 100.028.359 |
| Е-бројеви | E220 (конзерванси) |
| MeSH | Sulfur+dioxide |
| RTECS | WS4550000 |
| Svojstva | |
| S O2 | |
| Molarna masa | 64,054 g mol−1 |
| Agregatno stanje | bezbojan gas |
| Gustina | 2,551 g/L, гас |
| Tačka topljenja | −72.4 °C (200.75 K) |
| Tačka ključanja | −10 °C (263 K) |
| 9.4 g/100 mL (25 °C)[1] | |
| Kiselost (pKa) | 1.81 |
| Struktura | |
| Oblik molekula (orbitale i hibridizacija) | Iskrivljen pod uglom od 120° |
| Dipolni moment | 1.63 D |
| Opasnosti | |
EU klasifikacija (DSD)
|
Otrovan |
| R-oznake | R23 R34 |
| S-oznake | (S1/2) S9 S26 S36/37/39 S45 |
| NFPA 704 | |
| Tačka paljenja | nije zapaljiv |
| Srodna jedinjenja | |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |
| Reference infokutije | |
Rastvor sumpor-dioksida u vlažnoj okolini deluje kao izbeljivač tako što redukuje sastojke u materiji koja se izbeljuje.
Sumpor-dioksid je nusprodukt rada automobilskih motora i fabričkih postrojenja i zagađuje životnu sredinu. Napada sistem za disanje ljudi i životinja. Rastvarajući se u vazduhu uzrokuje kisele kiše koje uništavaju biljke, metalne konstrukcije i građevine.
Reference
uredi- ^ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ Holleman A. F.; Wiberg E. (2001). Inorganic Chemistry (1st izd.). San Diego: Academic Press. ISBN 0-12-352651-5.
Spoljašnje veze
uredi
