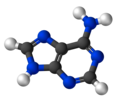
Аденин
Аденин је једна од две пуринске нуклеобазе, које се користе у формирању нуклеотида нуклеинских киселина ДНК и РНК. У ДНК, аденин (A) се везује за тимин (T) помоћу две водоничне везе, како би помогао у стабилизацији структуре нуклеинске киселине. У РНК се аденин везује за урацил (U).

| |||
| |||
| Називи | |||
|---|---|---|---|
| IUPAC назив
9H-пурин-6-амин
| |||
| Други називи
6-аминопурин
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.724 | ||
| EC број | 200-796-1 | ||
| KEGG[1] | |||
| RTECS | AU6125000 | ||
| UNII | |||
| |||
| |||
| Својства | |||
| C5H5N5 | |||
| Моларна маса | 135,13 g/mol | ||
| Агрегатно стање | бели или бледожути кристали | ||
| Густина | 1,6 g/cm³ (израчуната) | ||
| Тачка топљења | 360–365 °C (разлаже се) | ||
| 0,103 g/100 mL | |||
| Растворљивост | занемарљива у етанолу | ||
| Киселост (pKa) | 4,15 (секондарна), 9,80 (примарна)[4] | ||
| Термохемија | |||
| Специфични топлотни капацитет, C | 147,0 J/K·mol | ||
Стандардна енталпија
стварања (ΔfH |
96,9 kJ/mol | ||
| Опасности | |||
| Смртоносна доза или концентрација (LD, LC): | |||
LD50 (средња доза)
|
227 mg/kg (пацов, орално) | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |||
| Референце инфокутије | |||
Аденин формира аденозин, нуклеозид, када се причврсти за рибозу, и дезоксиаденозин када се причврсти за дезоксирибозу, и гради аденозин трифосфат (АТП), нуклеотид, када му се додају три фосфатне групе. Аденозин трифосфат је изузетно значајан јер се у ћелијском метаболизму користи као једна од основних метода за трансфер хемијске енергије између реакција.
У старијој литератури, аденин се некад назива именом Витамин Б4. Међутим, више се не сматра правим витамином (види Витамин Б).
Комплементарност уреди
У молекулима нуклеинских киселина аденин се везује двоструком водоничном везом за пиримидинске базе:
Та особина назива се комплементарност и на њој се заснива секундарна структура нуклеинских мкиселина.
Пар аденин-тимин кога одржавају две водоничне везе има облик који је исти као пар гуанин-цитозин кога одржавају најмање две водоничне везе. Од свих азотних база се могу направити парови (два аденина, аденин и гуанин, гуанин и цитозин, два цитозина, тимин и гуанин) али само за парове А-Т и Г-Ц кажемо да су комплементарни зато што само та два пара база имају потпуно истоветан просторни облик, и само они могу да се сложе у двоструку спиралу тако да дају савршено стабилну структуру.
Референце уреди
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.