p-Toluensulfonska kiselina
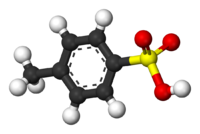
п-Толуенсулфонска киселина (ПТСА, тосилна киселина, ТсОХ) је органско једињење са формулом CH3C6H4SO3H. Она је бели прах који је растворан у води, алкохолима, и другим поларним органским растварачима. 4-CH3C6H4SO2- група је позната као тозил група и често се означава као Ts или Tos. Најчешће се TsOH односи на монохидрат, TsOH.H2O.

| |
| |
| Називи | |
|---|---|
| IUPAC назив
4-methylbenzenesulfonic acid
| |
| Други називи
Тосилна киселина
ПТСА | |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.002.891 |
| КЕГГ[2] | |
| |
| Својства | |
| CH3C6H4SO3H | |
| Моларна маса | 172,20 g/mol (anhidrat) 190,22 g/mol (monohidrat) |
| Агрегатно стање | безбојни (бели) прах |
| Густина | 1,24 g/cm3 |
| Тачка топљења | 38 °C, 311 K (anhidrat) [5] 103-106 °C, 376-379 K (monohidrat) |
| Тачка кључања | 140 °C (284 °F; 413 K) |
| 67 g/100 mL | |
| Киселост (пКа) | -2.8 (вода),[6] 8.5 (ацетонитрил)[7] |
| Структура | |
| Облик молекула (орбитале и хибридизација) | тетраедарна на S |
| Опасности | |
| Опасност у току рада | иритант коже |
| Безбедност приликом руковања | External MSDS |
| R-oznake | R36/37/38 |
| S-oznake | S26 |
| Srodna jedinjenja | |
Srodne sulfonske kiseline
|
Benzensulfonska kiselina Sulfanilska kiselina |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Референце инфокутије | |
TsOH је јака органска киселина. Она је око милион пута јача од бензојеве киселине. Она је једна од малобројних чврстих киселина, те је стога подесна за мерење. За разлику од јаких минералних киселина (посебно азотне, сумпорне, и перхлорне киселине), TsOH није оксидујућа.
Референце
уреди- ^ Мерцк11тх 9459.
- ^ Јоанне Wиxон; Доуглас Келл (2000). „Wебсите Ревиеw: Тхе Кyото Енцyцлопедиа оф Генес анд Геномес — КЕГГ”. Yеаст. 17 (1): 48—55. дои:10.1002/(СИЦИ)1097-0061(200004)17:1<48::АИД-YЕА2>3.0.ЦО;2-Х.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Armarego 2003, стр. 370.
- ^ Guthrie, J. P. Hydrolysis of esters of oxy acids: pKa values for strong acids. Can. J. Chem. 1978, 56, 2342-2354.
- ^ Eckert, F.; Leito, I.; Kaljurand, I.; Kütt, A.; Klamt, A.; Diedenhofen, M. (2009). „Prediction of Acidity in Acetonitrile Solution with COSMO-RS”. J. Comput. Chem. 30: 799—810. doi:10.1002/jcc.21103.
Literatura
уреди- Armarego, Wilfred (2003). Purification of Laboratory Chemicals. Elsevier Science. стр. 370. ISBN 0-7506-7571-3.