Фумарна киселина
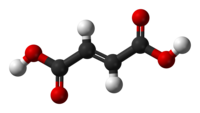
Fumarna kiselina (trans-butendionska kiselina) je hemijsko jedinjenje sa formulom HO2CCH=CHCO2H.[2][3] Ovo belo kristalno jedinjenje je jedna od dve izomerne nezasićene dikarboksilne kiseline. Druga je maleinska kiselina. U fumarnoj kiselini su karboksilne grupe u trans (E) položaju, dok su u maleinskoj kiselini u cis (Z). Fumarna kiselina ima ukus sličan voću. Soli i estri su poznati kao fumarati. Dimetil fumarat znatno redukuje progresiju invaliditeta kod obolelih od multiple skleroze.

| |
| |
| Nazivi | |
|---|---|
| IUPAC naziv
(E)-Butendionska kiselina
| |
| Drugi nazivi
trans-1,2-Etilendikarboksilna kiselina
2-Butendionska kiselina trans-butendionska kiselina Alomaleinska kiselina Boletinska kiselina Donitinska kiselina Liheniska kiselina | |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.404 |
| EC broj | 203-743-0 |
| E-brojevi | E297 (konzervansi) |
| KEGG[1] | |
| UNII | |
| |
| Svojstva | |
| C4H4O4 | |
| Molarna masa | 116,07 g/mol |
| Agregatno stanje | Bela čvrsta materija |
| Gustina | 1,635 g/cm³ |
| Tačka topljenja | 287 °C |
| 0,63 g/100 mL | |
| Kiselost (pKa) | pka1 = 3.03, pka2 = 4.44 |
| Opasnosti | |
EU klasifikacija (DSD)
|
Iritant (Xi) |
| R-oznake | R36 |
| S-oznake | (S2) S26 |
| NFPA 704 | |
| Srodna jedinjenja | |
Srodne karboksilne kiseline
|
maleinska kiselina sukcinska kiselina krotonska kiselina |
Srodna jedinjenja
|
fumaril hlorid fumaronitril dimetil fumarat gvožđe(II) fumarat |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Референце уреди
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ Morrison Robert Thornton; Boyd Robert Neilson (2006). Organic chemistry. Engelwood Cliffs, New Jersey: Prentice Hall. ISBN 8120307658.
Литература уреди
Vidi još уреди
- Dermatologija
- Fotosinteza
- Maleinska kiselina, cis-izomer fumarne kiseline
