Допамин
Допамин је хемијска супстанца коју производи организам. У централном и периферном нервном систему делује као неуротрансмитер.[3][4] Делује и као хормон кога лучи хипоталамус, а који инхибира лучење пролактина из хипофизе. Из допамина се синтетише адреналин и норадреналин.

| |
| |
| Називи | |
|---|---|
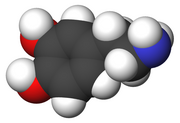
| IUPAC назив
4-(2-aminoethyl)benzene-1,2-diol
| |
| Други називи
2-(3,4-dihydroxyphenyl)ethylamine;
3,4-dihydroxyphenethylamine; 3-hydroxytyramine; DA; Intropin; Revivan; Oxytyramine | |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.000.101 |
| MeSH | Dopamine |
| |
| |
| Својства | |
| C8H11NO2 | |
| Моларна маса | 153,18 g/mol |
| Тачка топљења | 128 °C (262 °F; 401 K) |
| 60.0 g/100 ml | |
| Опасности | |
| R-ознаке | R36/37/38 |
| S-ознаке | S26 S36 |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
У популарној култури и медијима, допамин се често приказује као главна хемикалија задовољства, али тренутно мишљење у фармакологији је да допамин уместо тога даје мотивациони значај;[5] другим речима, допамин сигнализира перципирану мотивациону истакнутост; (тј. пожељност или аверзивност) исхода, што заузврат покреће понашање организма ка постизању тог исхода или даље од њега.[6]
Распрострањеност
уредиУ мозгу постоје три значајна система која луче допамин.
- Црна супстанца (лат. Substantia nigra). Допамински неурони из ове структуре инхибишу неуроне у пругастом телу (лат. Corpus striatum). Дегенерација ових допаминских влакана изазива Паркинсонову болест.
- Лимбички систем (мезолимбичке структуре). Допаминске влакна из мезолимбичких структура протежу се до мирисне квржице (лат. Tuberculum olfactorium), амигдалоидног једра (лат. Corus amygaloideum), чеоног режња, цингуларног режња, лат. Nucleus accumbens... Ова влакна играју улогу и настанку осећаја еуфорије, задовољства, ситости... О овом систему се говори и као о систему за награду. Многе хемијске супстанце као: никотин, дроге, алкохол... активирају овај систем и тако изазивањем осећаја еуфорије могу изазвати зависност.
- Једра тубероинфудибуларног дела хипоталамуса такође луче допамин. Допамин доспева у хипофизу и ту инхибира лучење пролактина. У овом случају допамин делује као хормон.
- У неким периферним неуронима нпр. у бубрезима такође је откривен допамин.
Синтеза
уредиДопамин заједно са адреналином и норадреналином припада групи неуротрансмитера познатих као катехоламини. Сви катехоламини настају из аминокиселине тирозин.
У нервним завршецима налазе се ензими који из тирозина синтетишу катехоламине. Тирозин се у неуроне транспортује из спољашње средине, мада се може произвести у нервним ћелијама из аминокиселине фенилаланин.
Прво се врши хидроксилација тирозина уз помоћ ензима тирозинхидроксилаза до 3,4 дихидроксифенилаланина Л-(ДОПА). Затим се ДОПА под утицајем ензима декарбоксилаза ароматичних аминокиселина преводи у допамин. У норадренергичким и адренеричким неуронима реакција може ићи даље, јер је допамин супстрат за ове неуротрансмитере.
Синтетисани допамин се пакује и складишти у синаптичке везикуле. Путем егзоцитозе долази до ослобађања допамина у синаптичку пукотину, а допамин везује за синаптичке рецепоре.
Рецептори
уредиПостоји 5 врста рецептора за допамин (Д1-Д5). Допамин, као и допамински агонисти-бромокриптин, апоморфин се лакше везују за рецепторе Д2, Д3, Д4 него за Д1 и Д2. Агонисти су супстанце са истим дејством као и главна супстанца.[10][11]
Д1 и Д2 рецептори активирају Г протеин и аденилат циклазу што доводи до даљих промена (делују ексцитаторно). Д2, Д3, Д4 рецептори такође активирају Г протеин, али сад се аденилат циклаза инхибира и отварају калијумови канали (делују инхибиторно).
Д1 рецептори се налазе у глатким мишићним ћелијама бубрежних артерија. Њиховом активацијом се ове артерије проширују, па се прокрвљеност бубрега повећава.
Д2 рецептори су претежно смештени у мозгу, поготово у: пругастом телу и хипофизи. Такође у лимбичком систему се активацијом ових рецептора изазива еуфорија. Још неке функције се везују за ове рецепторе као нпр. ентиеметичко дејство (сузбијају мучнину)... Д2 рецептори се налазе такође и на допаминергичким неуронима чиме се лучење допамина путем ауторегулације смањује.
Инактивација
уредиДопамин се одстрањује из синаптичке пукотине реапсорпцијом у пресинаптичке завршетке. Овај транспорт врши се активно, као котранспорт са јонима натријума.
Ресорбовани допамин се разграђује у цитоплазми неурона или поново складишти у везикуле. У разградњи допамина учествују два ензима: катехол-О-метилтрансфераза (КОМТ) и моноаминиоксидаза-А (МАО)-А. Његовом разградњом настају дихидроксифенилсирћетна киселина и хемованилинска киселина. Оне се излучују мокраћом и мерење њихове концентрације у мокраћи служи за дијагнозу неких болести система катехоламина.
Болести изазване поремећајем допаминских система
уредиКод шизофреније и разних психоза је активност допаминергичких неурона у лимбичком систему повећана. Лекови који инхибирају ове рецепторе (неуроне) користе се за лечење шизофреније (неуролептици).
Настаје услед пропадања неурона који луче допамин у црној супстанци. Карактерише се тремором, поремећајима хода, мимике, повећаним тонусом мишића (ригор), нестабилношћу, вегетативним симптомима...
Многе дроге активирају допаминске рецепторе. Тиме се изазива еуфорија и изазива зависност (пре свега психичка).
Види још
уредиРеференце
уреди- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Кораћевић, Даринка; Бјелаковић, Гордана; Ђорђевић, Видосава (2000). Биохемија. савремена администрација. ISBN 978-86-387-0622-8.
- ^ David L. Nelson; Michael M. Cox (2005). Principles of Biochemistry (IV изд.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ^ Malenka RC; Nestler EJ; Hyman SE (2009). Sydor A; Brown RY, ур. Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd изд.). New York: McGraw-Hill Medical. стр. 147—48, 366—67, 375—76. ISBN 978-0-07-148127-4.
- ^ Puglisi-Allegra, Stefano; Ventura, Rossella (2012). „Prefrontal/Accumbal catecholamine system processes high motivational salience”. Frontiers in Behavioral Neuroscience. 6: 31. PMC 3384081 . PMID 22754514. doi:10.3389/fnbeh.2012.00031 ..
- ^ Broadley KJ (2010). „The vascular effects of trace amines and amphetamines”. Pharmacol. Ther. 125 (3): 363—375. PMID 19948186. doi:10.1016/j.pharmthera.2009.11.005.
- ^ Lindemann L, Hoener MC (2005). „A renaissance in trace amines inspired by a novel GPCR family”. Trends Pharmacol. Sci. 26 (5): 274—281. PMID 15860375. doi:10.1016/j.tips.2005.03.007.
- ^ Wang X, Li J, Dong G, Yue J (2014). „The endogenous substrates of brain CYP2D”. Eur. J. Pharmacol. 724: 211—218. PMID 24374199. doi:10.1016/j.ejphar.2013.12.025.
- ^ Rummel, Forth Henschler (2001). Pharmakologie und toxikologie. Urban&Fischer. ISBN 978-3-437-42520-2.
- ^ Guyton, Arthur C.; Hall, John E. (1999). Medicinska fiziologija. Beograd: Savremena administracija. ISBN 978-86-387-0778-2.
Литература
уреди- Кораћевић, Даринка; Бјелаковић, Гордана; Ђорђевић, Видосава (2000). Биохемија. савремена администрација. ISBN 978-86-387-0622-8.
- Rummel, Forth Henschler (2001). Pharmakologie und toxikologie. Urban&Fischer. ISBN 978-3-437-42520-2.
- Guyton, Arthur C. John E. Hall (1999). Медицинска физиологија. савремена администрација Београд.
Спољашње везе
уреди- Biochemistry of Parkinson's Disease Архивирано на сајту Wayback Machine (7. фебруар 2009) (језик: енглески)
- neuroscience Архивирано на сајту Wayback Machine (19. мај 2006) (језик: енглески)
| Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |