Неутрон
У физици, неутрон је субатомска честица, симбол n или n0, без наелектрисања и са масом од 940 MeV/c 2 (1.6749 х 10-27 kg, мало већом од масе протона). Његов Спин је 1/2. Неутрон је саставни део језгра сваког атома осим најраспрострањенијег изотопа водоника, чије се језгро састоји само од једног протона. Како се протони и неутрони слично понашају унутар језгра, и сваки има масу од приближно једне јединице атомске масе, они се називају нуклеонима.[5] Њиова својства и интеракције описује нуклеарна физика.
 | |
| Класификација | Барион |
|---|---|
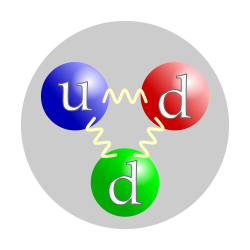
| Композиција | 1 горњи кварк, 2 |доња кварка |
| Статистике | Субатомска честица, Фермион |
| Интеракције | Гравитација, слаба, јака, електромагнетна |
| Симбол | n, n0, N0 |
| Античестица | Антинеутрон |
| Теорије | Ернест Радерфорд[1] (1920) |
| Откривен | Џејмс Чедвик[2] (1932) |
| Маса | 1,674927471(21)×10−27 kg[3] 939,5654133(58) MeV/c2[3] 1,00866491588(49) u[3] |
| Средњи полуживот | 881,5(15) s (слободан) |
| Наелектрисање | 0 e (−2±8)×10−22 e (експериментални лимити)[4] |
| Електрични диполни моменат | < 2,9×10−26 e⋅cm (експериментални горњи лимит) |
| Електрична поларизабилност | 1,16(15)×10−3 fm3 |
| Магнетни момент | −0,96623650(23)×10−26 J·T−1[3] −1,04187563(25)×10−3 μB[3] −1,91304273(45) μN[3] |
| Магнетна поларизабилност | 3,7(20)×10−4 fm3 |
| Спин | 1/2 |
| Изоспин | −1/2 |
| Парност | +1 |
| Кондензован | I(JP) = 1/2(1/2+) |
Хемијска и нуклеарна својства нуклеуса су одређена бројем протона, који се назива атомски број, и бројем неутрона, званим неутронски број. Атомски масени број је укупни број нуклеона. На пример, угљеник има атомски број 6, и његов широко заступљени изотоп угљеник-12 има 6 неутрона,[6] док његов ретки изотоп угљеник-13 има 7 неутрона. Неки елементи се јављају у природи са само једним стабилним изотопом, као што је флуор. Други елементи имају више стабилних изотопа, као што је калај са десет стабилних изотопа.
Унутар нуклеуса, протони и неутрони су међусобно везани путем нуклеарне силе. Неутрони су неопходни за стабилизацију језгра. Једини изузетак је једнопротонски атом водоника. Неутрони се изобилно формирају у нуклеарној фисији и фузији. Они су примарни доприносилац нуклеосинтези хемијских елемената унутар звезда путем фисије, фузије и процеса неутронског заробљавања.
Неутрон је есенцијалан у продукцији нуклеарног горива. У деценији након што је неутрон открио Џејмс Чедвик 1932. године,[7] неутрони су кориштени за увођење разних типова нуклеарних трансмутација. Са открићем нуклеарне фузије 1938. године,[8] брзо је схваћено да, ако догађај фисије производи неутроне, сваки од тих неутрона може да изазове даље догађаје фисије, итд., у каскади познатој као нуклеарна ланчана реакција.[9] Ови догађаји и налази су довели до првог самоодрживог нуклеарног реактора (Чикашка камара-1, 1942) и првог нуклеарног оружја (Тринити, 1945).
Слободни неутрони, мада директно не јонизују атоме, узрокују јонизујућу радијацију. Као такви они могу да буду биолошки хазард, у зависности од дозе.[9] Мали природни флукс „неутронске позадине” слободних неутрона постоји на Земљи, узрокован засипањем космичким зрачењем, и природном радиоактивношћу спонтано физионих елемената у Земљиној кори.[10] Наменски неутронски извори као што су неутронски генератори, истраживачки реактори и спалациони извори узрокују ослобађање слободних неутрона за употребу у ирадијацији и у експериментима неутронског расејавања.
Особине уреди
Ван језгра неутрони су нестабилни и имају време полу-распада од око 15 минута. Распадају се на протон, електрон и антинеутрино. Исти распад, бета распад, се одиграва у неким језгрима. Унутар језгра неутрон и протон разменом пиона преобраћају се један у другога. Неутрон је класификован као барион, и састоји се од два down кварка и једног up кварка. Антиматеријски еквивалент неутрона је антинеутрон.[9]
Изотопи хемијских елемента одређују се бројем неутрона у атомском језгру. На пример, изотоп угљеника, угљеник-12, 12C, има 6 протона и 6 неутрона, угљеник-13, 13C, 6 протона и 7 неутрона а угљеник-14, 14C, 6 протона и 8 неутрона.
Маса уреди
Маса неутрона се не може директно одредити помоћу масене спектрометрије услед недостатка електричног набоја. Међутим, пошто се масе протона и деутерона могу мерити помоћу масеног спектрометра, маса неутрона се може извести путем одузимања масе протона од деутеронске масе, при чему је разлика маса неутрона плус енергија везивања деутеријума (изражена као позитивно емитована енергија). Ова каснија се може директно мерити путем мерења енергије ( ) појединачног 0,7822 MeV гама фотона емитованог кад су неутрони заробљени протонима (то је егзотермни процес који се одвија са неутронима нулте енергије), плус мала количина одскочне кинетичке енергије ( ) деутерона (око 0,06% укупне енергије).
Енергија гама зрака се може мерити са великом прецизношћу помоћу техника дифракције X-зрака, што су први пут извели Бел и Елиот 1948. године. Најбоље модерне (1986) вредности за масу неутрона помоћу ове технике су произвели Грин, et al.[11] На овај начин је одређена маса неутрона од:
- mнеутрон= 1,008644904(14) u
Вредност масе неутрона у MeV је мање прецизно позната, услед мање прецизности конверзије u у MeV:[12]
- mнеутрон= 939,56563(28) MeV/c2.
Још један метод за одређивање масе неутрона је базиран на бета распаду неутрона. У том методу се мери меменат резултирајућег протона и електрона.
Електрични набој уреди
Укупан електрични набој неутрона је 0 e. Ова нулта вредност је експериментално тестирана, и садашњи експериментални лимит за набој неутрона је −2(8)×10−22 e,[4] или −3(13)×10−41 C. Ова вредност је конзистентна са нулом, имајући у виду експерименталне неизвесности (наведене у заградама). У поређењу с тим, наелектрисање протона је +1 e.
Магнетни моменат уреди
Мада је неутрон неутрална честица, магнетни моменат неутрона није једнак нули. На неутрон не утичу електрична поља, али он подлеже утицају магнетних поља. Магнетни моменат неутрона је индикација његове кваркне подструктуре и унутрашње дистрибуције набоја.[13] Вредност неутронског магнетног момента су први пут директно мерили Луис Алварез и Феликс Блох у Берклију (Калифорнија), 1940. године,[14] користећи проширену верзију метода магнетне резонанце који је развио Раби. Алварез и Блох су одредили да је магнетни моменат неутрона μn= −1,93(2) μN, где је μN нуклеарни магнетон.
Енергије неутрона уреди
Енергија неутрона, често називана и температура неутрона, одређује кинетичку енергију слободног неутрона, обично у јединици Електронволт. Термин температура потиче од принципа на који се неутрон успорава, тј. врући, термички и хладни неутрони се модерирају у средини одређене температуре.
Са повећањем температуре, повећава се и кинетичка енергија слободног неутрона. Кинетичка енергија, брзина и таласна дужина неутрона везани су де Бројевом једначином.
- Брзи неутрони имају енергију већу од 1 eV, 0,1 MeV или 1 MeV, у зависности од дефиниције.
- Спори неутрони имају енергију испод 1 eV.
- Епитермички неутрони имају енергију између 0,025 до 1 eV.
- Врући неутрони имају енергију око 2 eV.
- Термички неутрони имају просечну енергију око 0,025 eV.
- Хладни неутрони имају енергију између 5x10-5 eV до 0.025 eV.
- Веома хладни неутрони имају енергију од 2x10-7 eV до 5x10-5 eV.
- Ултра хладни неутрони имају енергије мање од 2x10-7 eV.
Интеракције уреди
Неутрон учествује у свим облицима интеракција: електромагнетној, нуклеарној слабој, нуклеарној јакој и гравитационој интеракцији.
Мада је, издалека гледано, неутрон неутрална честица у његовој унутрашњости постоји расподела позитивног и негативног наелектрисања што се испо Карактеристика неутрона која га највише разликује од осталих обичних субатомских честица је његова електронеутралност. Ово својство неутрона је одложило њихово отткривање, чини их веома продорним, чини да их није могуће директно посматрати, и чини их веома важним чиниоцима нуклеарних промена.
Детекција неутрона уреди
Када се каже детекција честице, мисли се на тражење трага јонизације али то не функционише код неутрона директно, с обзиром да спада у честице које се не могу детектовати директно. Неутрони који се у еластичном судару одбију од атом неког елемента могу да проузрокују стварање трагова јонизације који се затим детекују, али искуство показује да ови експерименти нису једноставни за извођење. Други начин детковања неутрона, који се чешће користи, је када се допусти да неутрон интерагује са језгром атома.
Детекција се састоји у трансформацији енергије ослобођене у реакцији у електрични импулс. За ову сврху су корисни елементи Хелијум-3, Литијум-6, Бор-10, Уранијум-233, Уранијум-235, Нептунијум-237 и Плутонијум-239.
Сврха неутрона уреди
Неутрон је веома важан фактор у већини нуклеарних реакција. На пример, апсорпција неутрона често доводи до неутронове активације, укључујући радиоактивност. Знања о неутронима и њиховом понашању игра битну улогу у развоју нуклеарне технологије, нуклеарних реактора и оружја.
Хладни, термални и врући неутрони односно озрачивање помоћу њих, је примењено у испитивању чврсте материју, где се користи одбијање неутрона о елементе. Неутрони могу дубински да реагују са материјом с којом долазе у додир. Брзи неутрони се користе за детекцију воде у чврстим телима. Када дође до реакције између неутрона и молекула воде, неутрон изгуби скоро целу своју енергију. Мерењем ове енергије, с којом се успорени неутрон враћа до чврсте материје након реакције са водоником, може се установити где се тачно вода налази у чврстој материји.
Заштита од снопа неутрона уреди
Изложеност неутронима може да буде хазардан тј. опасан, с обзиром да интеракицја неутрона са молекулама у организму може да доведе до разарања и оштећења молекула и атома, а такође може изазвати настанак других облика радијације. Треба, значи, избегавати излагање снопу неутрона, држати се што даље од извора неутрона, и свести излагање на минимум. Када су у питању други типови радијације, као што су алфа честице, бета честице и гама зраци, материјали са вишим атомским бројевима и већом густином су довољни да нас заштите. Обично се користи олово. Овакав приступ, наравно, не важи и за неутроне. Као што је већ напоменуто, неутрон већи део енергије губи у реакцији са водоником, па је та особина искоришћена за заштиту пред зрачењем снопом неутрона.
Референце уреди
- ^ Ernest Rutherford. Chemed.chem.purdue.edu. Приступљено 2012-08-16.
- ^ 1935 Nobel Prize in Physics. Nobelprize.org. Приступљено 2012-08-16.
- ^ а б в г д ђ Mohr, P.J.; Taylor, B.N. and Newell, D.B. (2014), "The 2014 CODATA Recommended Values of the Fundamental Physical Constants" (Web Version 7.0). The database was developed by J. Baker, M. Douma, and S. Kotochigova. (2014). National Institute of Standards and Technology, Gaithersburg, Maryland 20899.
- ^ а б Olive, K.A.; (Particle Data Group); et al. (2014). „Review of Particle Physics” (PDF). Chin. Phys. C. 38 (9): 090001. Bibcode:2014ChPhC..38i0001O. S2CID 260537282. doi:10.1088/1674-1137/38/9/090001.
- ^ Thomas, A.W.; Weise, W. (2001), The Structure of the Nucleon, Wiley-WCH, Berlin, ISBN 978-3-527-40297-7
- ^ „Table of Isotopic Masses and Natural Abundances” (PDF). 1999.
- ^ Chadwick, James (1932). „Possible Existence of a Neutron”. Nature. 129 (3252): 312. Bibcode:1932Natur.129Q.312C. S2CID 4076465. doi:10.1038/129312a0.
- ^ Hahn, O.; Strassmann, F. (1939). „Über den Nachweis und das Verhalten der bei der Bestrahlung des Urans mittels Neutronen entstehenden Erdalkalimetalle ("On the detection and characteristics of the alkaline earth metals formed by irradiation of uranium with neutrons")”. Naturwissenschaften. 27 (1): 11—15. Bibcode:1939NW.....27...11H. S2CID 5920336. doi:10.1007/BF01488241. Непознати параметар
|name-list-style=игнорисан (помоћ) - ^ а б в Glasstone, Samuel; Dolan, Philip J., ур. (1977), The Effects of Nuclear Weapons, Third Edition, U.S. Dept. of Defense and Energy Research and Development Administration, U.S. Government Printing Office, ISBN 978-1-60322-016-3
- ^ Carson, M. J.; et al. (2004). „Neutron background in large-scale xenon detectors for dark matter searches”. Astroparticle Physics. 21 (6): 667—687. Bibcode:2004APh....21..667C. S2CID 17887096. arXiv:hep-ex/0404042 . doi:10.1016/j.astropartphys.2004.05.001.
- ^ Greene, GL; et al. (1986). „New determination of the deuteron binding energy and the neutron mass”. Phys. Rev. Lett. 56 (8): 819—822. Bibcode:1986PhRvL..56..819G. PMID 10033294. doi:10.1103/PhysRevLett.56.819.
- ^ Byrne, J. Neutrons, Nuclei, and Matter, Dover Publications, Mineola. Byrne, James (2011). Neutrons, Nuclei and Matter: An Exploration of the Physics of Slow Neutrons. New York. стр. 18—19. ISBN 978-0-486-48238-5.
- ^ Gell, Y.; Lichtenberg, D. B. (1969). „Quark model and the magnetic moments of proton and neutron”. Il Nuovo Cimento A. Series 10. 61 (1): 27—40. Bibcode:1969NCimA..61...27G. S2CID 123822660. doi:10.1007/BF02760010.
- ^ Alvarez, L. W; Bloch, F. (1940). „A quantitative determination of the neutron magnetic moment in absolute nuclear magnetons”. Physical Review. 57 (2): 111—122. Bibcode:1940PhRv...57..111A. doi:10.1103/physrev.57.111.
Литература уреди
- Byrne, James (2011). Neutrons, Nuclei and Matter: An Exploration of the Physics of Slow Neutrons. Mineola, New York: Dover Publications. ISBN 978-0-486-48238-5..
- Macura, Slobodan; Radić-Perić, Jelena (2004). Atomistika. Beograd: Fakultet za fizičku hemiju Univerziteta u Beogradu/Službeni list. стр. 504..
- Abraham Pais, Inward Bound, Oxford. . Oxford University Press. 1986. ISBN 978-0-19-851997-3. Недостаје или је празан параметар
|title=(помоћ). - Sin-Itiro Tomonaga (1997). The Story of Spin. The University of Chicago Press.
- Herwig Schopper, Weak interactions and nuclear beta decay, Publisher, North-Holland Pub. Co., 1966.