Glukonska kiselina
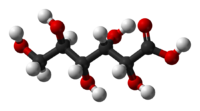
Glukonska kiselina je organsko jedinjenje sa molekulskom formulom C6H12O7 i strukturnom formulom HOCH2(CHOH)4COOH. Ona je jedan od 16 stereoizomera 2,3,4,5,6-pentahidroksiheksanske kiseline.

| |
| |
| Nazivi | |
|---|---|
| IUPAC naziv
D-Glukonska kiselina
| |
| Drugi nazivi
Dekstronska kiselina
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.007.639 |
| E-brojevi | E574 (regulator kiselosti, ...) |
| |
| Svojstva | |
| C6H12O7 | |
| Molarna masa | 196,16 g/mol |
| Agregatno stanje | Bezbojni kristali |
| Tačka topljenja | 131 °C (268 °F; 404 K) |
| Dobra | |
| Kiselost (pKa) | 3.86[3] |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
U vodenim rastvorima na neutralnom pH, glukonska kiselina formira glukonatni jon. Soli glukonske kiseline su poznate kao „glukonati“. Glukonska kiselina, glukonatne soli, i glukonatni estri su široko rasprostranjeni u prirodi zato što proizilaze iz oksidacije glukoze. Neki lekovi se da unose putem injekcija u obliku glukonata.
Hemijska struktura
уредиHemijska struktura glukonske kiseline se sastoji od lanca sa šest ugljenika za koje je vezano pet hidroksilnih grupa i terminalna karboksilna grupa. U vodenom rastvoru, glukonska kiselina postoji u ravnoteži sa cikiličnim estrom glukono delta-laktonom.
Rasprostranjenost i upotreba
уредиGlukonska kiselina se prirodno javlja u voću, medu, kombuča čaju, i vinu. Kao prehrambeni aditiv (E574[4]), ona je regulator kiselosti. Ona se takođe koristi u sredstivima za čišćenje, gde ona rastvara mineralne depozite posebno u alkalinom rastvoru. Glukonatni anjon formira helate sa Ca2+, Fe2+, Al3+, i drugim metalima. Horas Terhun Herik je razvio proces za proizvodnju soli putem fermentacije 1929.[5]
Kalcijum glukonat u obliku gela se koristi za tretiranje opekotina uzrokovanih fluorovodoničnom kiselinom;[6][7] kalcijum glukonatne injekcije se mogu koristiti u ozbiljnijim slučajevima da bi se izbegla nekroza unutrašnjih tkiva.[8] Kinin glukonat je so glukonske kiseline i kinina, koja se koristi za intramaskularne injekcije u lečenju malarije. Cink glukonatne injekcije se koriste pri kastraciji mužjaka pasa.[9] Injekcije gvožđe glukonata su bile predlagane za tretiranje anemije.[10]
Reference
уреди- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Bjerrum, J., et al. Stability Constants, Chemical Society, London, 1958.
- ^ Current EU approved additives and their E Numbers. Food Standards Agency
- ^ „All Chemistry”. Time magazine. 13. 5. 1929. Архивирано из оригинала 03. 06. 2011. г. Приступљено 12. 07. 2010.
- ^ el Saadi MS, Hall AH, Hall PK, Riggs BS, Augenstein WL, Rumack BH (1989). „Hydrofluoric acid dermal exposure”. Vet Hum Toxicol. 31 (3): 243—7. PMID 2741315.
- ^ Roblin I, Urban M, Flicoteau D, Martin C, Pradeau D (2006). „Topical treatment of experimental hydrofluoric acid skin burns by 2.5% calcium gluconate”. J Burn Care Res. 27 (6): 889—94. PMID 17091088. S2CID 3691306. doi:10.1097/01.BCR.0000245767.54278.09.
- ^ Thomas, D.; Jaeger, U.; Sagoschen, I.; Lamberti, C.; Wilhelm, K. (2009). „Intra-Arterial Calcium Gluconate Treatment After Hydrofluoric Acid Burn of the Hand”. CardioVascular and Interventional Radiology. 32 (1): 155—158. PMID 18506520. S2CID 34140904. doi:10.1007/s00270-008-9361-1.
- ^ Levy, Julie K.; Crawford, P. Cynda; Appel, Leslie D.; Clifford, Emma L. (2008). „Comparison of intratesticular injection of zinc gluconate versus surgical castration to sterilize male dogs”. American Journal of Veterinary Research. 69 (1): 140—143. PMID 18167099. S2CID 29860157. doi:10.2460/ajvr.69.1.140.
- ^ Paul Reznikoff and Walther F. Goebel (1937), The preparation of ferrous gluconate and its use in the treatment of hypochromic anelia in rats. Journal of Pharmacology and Experimental Thereapy, volume 59 issue 2, page 182.