Метан
Метан (CH4), познат и као блатни гас је најпростији засићени угљоводоник (алкан). Уколико владају нормални услови он је безбојан гас. У природи метан настаје услед бескисеоничног распада органских материја (нпр. у мочварама). Метан је главни састојак земног гаса. Користи се као гас за грејање и као сировина за добијање органских једињења. Запаљен гори светлим модрикастим пламеном, а његовим сагоревањем у присуству кисеоника настаје угљен-диоксид и вода. Нерастворан је у води, а у смеши са ваздухом врло експлозиван. Релативно велика количина метана на Земљи даје му статус алтернативног, атрактивног извора енергије. Међутим, пошто је на нормалној температури и притиску у гасовитом стању, метан је веома тешко транспортовати из његових налазишта. Као гас, обично се превози путем гасовода или цистернама утечњен као течност на температури испод -162 °C (као LNG - liquefied natural gas).
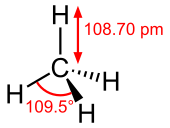
| |||
| |||
| Називи | |||
|---|---|---|---|
| Преферисани IUPAC назив
Метан[1] | |||
| Системски IUPAC назив
Карбан (није препоручен[1]) | |||
Други називи
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| 3DMet | B01453 | ||
| Бајлштајн | 1718732 | ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.739 | ||
| EC број | 200-812-7 | ||
| Гмелин Референца | 59 | ||
| KEGG[2] | |||
| MeSH | Methane | ||
| RTECS | PA1490000 | ||
| UN број | 1971 | ||
| |||
| |||
| Својства | |||
| CH4 | |||
| Моларна маса | 16,04 g·mol−1 | ||
| Агрегатно стање | Безбојни гас | ||
| Мирис | Без мириса | ||
| Густина |
| ||
| Тачка топљења | −182,5 °C; −296,4 °F; 90,7 K | ||
| Тачка кључања | −161,50 °C; −258,70 °F; 111,65 K[6] | ||
| 22,7 mg·L−1 | |||
| Растворљивост | Растворан у етанолу, диетил етру, бензену, толуену, метанолу, ацетону и није растворан у води | ||
| log P | 1,09 | ||
| kH | 14 nmol·Pa−1·kg−1 | ||
| Конјугована киселина | Метанијум | ||
| Конјугована база | Метил анјон | ||
| Магнетна сусцептибилност | −12,2×10−6 cm³·mol−1 | ||
| Структура | |||
| Td | |||
| Облик молекула (орбитале и хибридизација) | Тетраедар | ||
| Диполни момент | 0 D | ||
| Термохемија | |||
| Специфични топлотни капацитет, C | 35,69 J·(K·mol)−1 | ||
Стандардна моларна
ентропија (S |
186,25 J·(K·mol)−1 | ||
Стандардна енталпија
стварања (ΔfH |
−74,87 kJ·mol−1 | ||
Стд енталпија
сагоревања (ΔcH⦵298) |
−891,1 до −890,3 kJ·mol−1 | ||
| Опасности[7] | |||
| ГХС пиктограми | 
| ||
| ГХС сигналне речи | Опасност | ||
| H220 | |||
| P210 | |||
| NFPA 704 | |||
| Тачка паљења | −188 °C (−306,4 °F; 85,1 K) | ||
| 537 °C (999 °F; 810 K) | |||
| Експлозивни лимити | 4,4–17% | ||
| Сродна једињења | |||
Сродна алкани
|
|||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |||
| Референце инфокутије | |||
Молекул метана има облик тетраедра. Атом угљеника с има sp3 хибридизацију. Остале орбитале граде хемијску везу са четири атома водоника. Све четири везе су подједнаке (углови између веза износе 109°28') и веома су мало поларизоване, што је заједно са недостатком слободних електронских парова велике постојаности овог једињења. Метан може да учествује само у реакцијама типичним за алкане (нпр: сагоревање).
Метан има потенцијално деловање као стакленички гас са високим потенцијалом за глобално затопљење са индексом од 72 (уз просек од 20 година) односно индексом 25 (уз просек од 100 година)[9]. Метан се у атмосфери оксидује, производећи угљен-диоксид и воду. Због тога, метан у атмосфери има полувреме постојања од око седам година.
Распрострањеност метана у Земљиној атмосфери у току 1998 године је процењена на 1745 ppb (милијардити део, parts per billion), а процењује се да се у 1750. години у атмосфери налазило око 700 ppb. Метан може задржавати и до 20 пута више топлоте од угљен-диоксида. У истом периоду (1750—1998) количина CO2 у атмосфери је порасла са 278 на 365 ppm. Топлотни ефект због овог повећања количине метана је око једне трећине од истог ефекта повећања CO2[10]. Поред тога, постоје огромне али непознате количине метана у облику метан хидрата на дну океана. Земљина кора такође садржи огромне количине метана. Велике количине се произведу анаеробним путем метаногенезе. Остали извори метана су вулканске ерупције и ферментацијом унутар стоке (крава, оваца, коња и других животиња).
Историја
уредиРеч метан вероватно потиче из старогрчког језика. Већ се у време античке Грчке знало о запаљивом гасу. Тако су у Малој Азији постојала места извора метана. Вулканско подручје, у којем су пронађени такви гасови, је добило име по овом гасу.
Метан је био познат и алхемичарима у средњем веку као саставни део гасова који настају при распадању, а имао је и име мочварни гас. Метан је открио Томас Ширли 1667. године. Џозеф Пристли је открио 1772. године да метан настаје при процесима распадања. Алесандро Волта га је изоловао између 1776. и 1778. године док је студирао мочварни гас из језера Мађоре. Године 1856. Марселин Бертело је први синтетизирао метан из угљен-дисулфида и водоник-сулфида.
Добијање
уредиЛабораторијски метан се добија пржењем натријум октана са натријум хидроксидом:
- CH3COONa + NaOH → CH4 + Na2CO3
Друга метода је хидролиза алуминијум карбида:
- Al4C3 +12H2O → 3CH4 + 4Al(OH)3
Особине метана
уредиМетан је једна од основних компонената земног гаса, од око 87% по запремини. На собној температури и стандардном притиску, метан је безбојни гас, без мириса и укуса. Наводни мирис земног гаса, који се користи у домаћинству, је вештачки направљен као једна од сигурносних мера, додавањем одоранта, најчешће метантиола или етантиола. Метан има тачку кључања од око -161 °C при притиску од једне атмосфере. Као гас је лако запаљив, већ при мањим концентрацијама у ваздуху (5-15%). Течни метан није запаљив све док се не изложи великом притиску (обично 4-5 атмосфера).
Мешавина метана са ваздухом у размери 1:10 има експлозивно дејство. Настанак овакве смеше у рудницима је често разлог великих експлозија и смрти многих људи. Велике количине метана се налаза на планетама у облику мора (као што на земљи постоје мора воде, тако на неким планетама постоје мора метана)
Потенцијални ефекти на здравље
уредиМетан није отрован. Међутим, веома је запаљив и у смеси са ваздухом може бити експлозиван. Бурно реагује са оксидационим средствима, халогеним елементима и супстанцама које садрже халогене. Метан је асфиксиони гас, што значи да може истиснути кисеоник у затвореним просторијама, али су концентрације при којима он може експлодирати или запалити се, далеко ниже од концентрација на којима се може развити ризик од гушења. Највећа опасност од експлозије мешавине метана и ваздуха постоји у рудницима угља.
Хемија
уредиРеакције метана
уредиОсновне реакције у које ступа метан су: горење, халогенација и активација водоника. Генерално, реакције метана је доста тешко контролисати. На пример, врло тешко је доћи до делимичне оксидације метанола, јер се реакција обично наставља све до настанка угљен-диоксида и воде.
Сагоревање
уредиПри сагоревању метана, дешавају се бројне реакције:
Верује се да метан формира формалдехид (HCHO или H2CO). Формалдехид даје формил радикал (HCO), који даље формира угљен моноксид (CO). Овај процес се назива оксидативна пиролиза:
У току оксидативне пиролизе, H2 се оксидује дајући воду (H2O) отпуштајући топлоту. Ово се дешава веома брзо, обично за мање од једне милисекунде.
На крају, CO се оксидује дајући CO2 и отпушта још више топлоте. Овај процес је генерално спорији од других хемијских корака и обично траје неколико милисекунди.
Резултат горњих реакција је следећа тотална реакција:
- (g) и (l) означавају агрегатно стање: g - гас; l - течност
Активација водоника
уредиЈачине ковалентне везе између угљеника и водоника у молекулу метана су међу најснажнијим међу свим угљоводоницима, те је њихово кориштење у хемијским реакцијама ограничено. Поред високе границе активације за разбијање C-H веза, метан је и даље главни почетни материјал за алкане у областима истраживања и са изузетним индустријским значајем. У метановом молекулу везе затварају угао од 109,5 степени.
Реакције са халогенима
уредиМетан реагује са свим халогеним елементима, у датим условима и околностима:
где је X неки халогени елемент: флуор (F), хлор (Cl), бром (Br) или јод (I). Овај механизам за овај процес се назива халогенација слободним радикалима. Ако су метан и халогени елемент (X2) употребљени у еквимоларним количинама, могу се формирати CH2X2, CHX3 па чак и CX4. Користећи веће количине метана, смањује се производња CH2X2, CHX3, CX4, а више се формира CH3X.
Употреба
уредиГориво
уредиМетан је важан за производњу електричне енергије путем сагоревања као горива у гасним турбинама или парним бојлерима. У поређењу са фосилним горивима, сагоревањем метана се производи мање угљен-диоксида по јединици отпуштене топлоте. Са око 890,8 kJ/mol топлоте при сагоревању метана[11], иако је најједноставнији угљеноводоник, даје више топлоте по јединици масе него други комплекснији угљеноводоници. У многим насељима, метан се транспортује цевима до домаћинстава у сврху грејања. У овом контексту је обично познат као земни гас, а има енергетску вредност од око 39 MJ по m3.
Метан у облику компресованог природног гаса (CNG) се користи као погонско гориво, а сматра се да проузрокује мање загађење од других фосилних горива попут нафте и дизела[12].|first=Clayton B. NASA је вршила одређена истраживања о потенцијалу метана као ракетног горива[13]. Једна од предности метана је да је присутан у многим деловима сунчевог система, те би се потенцијално могао експлоатирати на површини других небеских тела, дајући гориво за путовање[14].
Тренутно се развијају мотори на метански погон који могу да развију потисак од 7.500 фунти, што је далеко мање од 7 милиона фунти неопходних да се лансира Спејс Шатле. Уместо тога, такви мотори би се могли користити за погон летелица са површине Месеца или слање роботских експедиција на друге планете сунчевог система[15].
Недавно, метан који настаје у рудницима угља је успешно искориштен у производњи електричне енергије[16].
Индустријска употреба
уредиМетан се користи у процесима хемијске индустрије а може се транспортовати у виду охлађеног текућег LNG (liquefied natural gas). Иако је као гас лакши од ваздуха, у течном, охлађеном стању је тежи од ваздуха због повећања густине. Путем гасовода се дистрибуирају велике количине природног гаса, у којем је метан главна компонента.
У хемијској индустрији, метан је један од главних ресурса у производњи водоника, метанола, сирћетне киселине и ацетатног анхидрида. При производњи ових супстанци, метан се прво конвертује у гас за синтезу, мешавину угљен моноксида и водоника деловањем паре. У том процесу, метан и пара реагују на високим температурама (700-1000 °C) уз никл као катализатор.
Однос угљен моноксида и водоника у гасу за синтезу може бити подешен преко реакције отклона воденог гаса на одређену вредност у зависности од намераване сврхе употребе.
Мање значајне хемикалије које се изводе из метана су ацетилен, добијен проласком метана кроз електрични лук, и хлорометани (хлорометан, метилен хлорид, хлороформ и угљен тетрахлорид, који се добијају реакцијом метана са хлором. Међутим, употреба ових хемикалија све више опада. Ацетилен је замењен јефтинијим супституентима, а кориштење хлорометана је упитно због ризика по здравље и загађење околине.
Извори метана
уредиПоља природног гаса
уредиНајвећи извор метана је његово издвајање из геолошких депозита познатих као поља природног плина. Углавном је повезан са другим угљоводоничним горивима, а понекад и са хелијумом и азотом. Метан под ниским притиском се формира при анаеробном разлагању органских материјала, те у природним изворима из великих дубина Земљине коре. Генерално, седименти који се налазе на већим дубинама и који су изложени вишим температурама од оних из којих настаје нафта, обично се претварају у природни гас. Метан се такође производи у већим количинама при распадању органског отпада на одлагалиштима смећа.
Алтернативни извори
уредиПоред поља гаса, алтернативни начин добијања метана је путем биогаса који се генерише ферментацијом органских материјала укључујући отпадне воде, смеће те друге отпадне материјале који садрже органске материје. Ферментацијом тих материјала у условима без присуства ваздуха (кисеоника) настаје, између осталих, метан. Метан хидрат (комбинација метана и леда, нађен је у огромним количинама на дну океана) потенцијални је извор метана у будућности. Метан настао преживањем крава чини око 16% светске годишње емисије метана у атмосферу[17]. Генерално, сектор сточарства (углавном краве, кокошке и свиње) производи око 37% метана којем је, директно или индиректно, узрок човек[18]. Ранија истраживања се пронашла бројне медицинске третмане и начине прилагођавања исхране стоке којима се помаже смањење производње метана код преживара[19][20][21].
Научни експерименти су дали различите резултате код испитивања да ли су живе биљке извор емисије метана[22][23][24].
Ванземаљски извори метана
уредиМетан је откривен или се претпоставља да постоји на бројим местима у сунчевом систему. Верује се да настаје у небиотичким процесима, уз изузетак на Марсу, где се претпоставља да га производе микроорганизми.
- Месец - откривени су трагови метана на површини[25]
- Марс - атмосфера садржи 10 ppb (милионити део) метана. У јануару 2009, научници из агенције NASA су објавили да су открили да се на Марсу често испушта метан у одређеним подручјима, што даје претпоставке о биолошкој активности испод површине планете[26]
- Јупитер - атмосфера садржи око 0,3% метана
- Сатурн - атмосфера садржи око 0,4% метана
- Уран - атмосфера садржи око 2,3% метана
- Аријел - сматра се да је метан један од састојака површинског леда на Аријелу
- Миранда
- Оберон - око 20% леда на површини Оберона је састављено од супстанци на бази метанских деривата
- Титаниа - око 20% леда на површини Титаније је састављено од органских супстанци повезаних с метаном
- Умбријел - метан је један од састојака површинског леда на Умбријелу
- Нептун - атмосфера садржи око 1,6% метана
- Плутон - спектроскопске анализе површине Плутона су доказале присуство метана[31][32]
Извори
уреди- ^ а б „Front Matter”. Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. стр. 3—4. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-FP001. „Methane is a retained name (see P-12.3) that is preferred to the systematic name ‘carbane’, a name never recommended to replace methane, but used to derive the names ‘carbene’ and ‘carbyne’ for the radicals H2C2• and HC3•, respectively.”
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ „Gas Encyclopedia”. Архивирано из оригинала 26. 12. 2018. г. Приступљено 7. 11. 2013.
- ^ Pubchem. „Methane”. pubchem.ncbi.nlm.nih.gov.
- ^ „Safety Datasheet, Material Name: Methane” (PDF). USA: Metheson Tri-Gas Incorporated. 4. 12. 2009. Архивирано из оригинала (PDF) 4. 6. 2012. г. Приступљено 4. 12. 2011.
- ^ „METHANE”. noaa.gov. NOAA Office of Response and Restoration, US GOV.
- ^ IPCC Fourth Assessment Report
- ^ „Radiative Forces of Climate Change”. Climate Change 2001: The Scientific Basis. IPCC. Архивирано из оригинала 15. 06. 2007. г. Приступљено 26. 05. 2008.
- ^ David R. Lide, ed., CRC Handbook of Chemistry and Physics, Internet Version 2005, http://www.hbcpnetbase.com Архивирано на сајту Wayback Machine (23. мај 2008), CRC Press, Boca Raton, FL, 2005, pp. 936
- ^ Cornell (29. 4. 2008). „Natural Gas Cars: CNG Fuel Almost Free in Some Parts of the Country”. Архивирано из оригинала 20. 01. 2019. г. Приступљено 14. 06. 2019.
- ^ Lunar Engines, Aviation Week & Space Technology, 171, 2 (13. juli 2009.), pp. 16
- ^ Methane Blast Архивирано на сајту Wayback Machine (30. август 2009), NASA, 4. maj 2007.
- ^ Green, V (septembar 2007). „Hit the Gas: NASA's methane rocket could make long distance space travel possible, on the cheap”. 271 (3). Popular Science magazine: 16—17.
- ^ A Global First: Coal Mine Turns Greenhouse Gas into Green Energy
- ^ Miller, G. Tyler. (2007). Sustaining the Earth: An Integrated Approach. U.S.A: Thomson Advantage Books. стр. 160.
- ^ „Livestock's Long Shadow-Environmental Issues and Options”. Приступљено 27. 10. 2009.
- ^ California Cows Fail Latest Emissions Test
- ^ New Zealand Tries to Cap Gaseous Sheep Burps
- ^ „Research on use of bacteria from the stomach lining of kangaroos (who don't emit methane) to reduce methane in cattle”. Архивирано из оригинала 28. 08. 2009. г. Приступљено 14. 06. 2019.
- ^ Hamilton JT, McRoberts WC, Keppler F, Kalin RM, Harper DB (2003). „Chloride methylation by plant pectin: an efficient environmentally significant process”. Science. 301 (5630): 206—9.
- ^ "Methane Emissions? Don't Blame Plants" Архивирано на сајту Wayback Machine (12. март 2009), ScienceNOW, 14. januar 2009.
- ^ Plants do emit methane after all Архивирано на сајту Wayback Machine (8. октобар 2008), New Scientist, 2. decembar 2007.
- ^ Stern, S.A. (1999). „The Lunar atmosphere: History, status, current problems, and context”. Rev. Geophys. 37: 453—491.
- ^ Mars Vents Methane in What Could Be Sign of Life, Washington Post, 16. januar 2009.
- ^ H. B. Niemann; et al. (2005). „The abundances of constituents of Titan's atmosphere from the GCMS instrument on the Huygens probe”. Nature. 438 (7069): 779—784.
- ^ Waite, J. H.; et al.; (2006); Cassini Ion and Neutral Mass Spectrometer: Enceladus Plume Composition and Structure, Science, vol. 311, br. 5766, pp. 1419-1422
- ^ Broadfoot, A L.; Bertaux, S K.; Dessler, J E.; et al. (15. 12. 1989). „Ultraviolet Spectrometer Observations of Neptune and Triton”. Science. 246 (4936): 1459—1466.
- ^ Miller, Ron; Hartmann, William K. (2005). The Grand Tour: A Traveler's Guide to the Solar System (3. изд.). Tajland: Workman Publishing. стр. 172-73. ISBN 978-0-7611-3547-0.
- ^ Owen, Tobias C.; Roush, Ted L.; et al. (1993). „Surface Ices and the Atmospheric Composition of Pluto”. Science. 261 (5122): 745—748.
- ^ „Pluto”. SolStation. 2006. Приступљено 28. 3. 2007.
Литература
уреди- „Front Matter”. Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. стр. 3—4. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-FP001. „Methane is a retained name (see P-12.3) that is preferred to the systematic name ‘carbane’, a name never recommended to replace methane, but used to derive the names ‘carbene’ and ‘carbyne’ for the radicals H2C2• and HC3•, respectively.”
Спољашње везе
уреди- Methane at The Periodic Table of Videos (University of Nottingham)
- International Chemical Safety Card 0291
- Gas (Methane) Hydrates -- A New Frontier – United States Geological Survey
- Catalytic conversion of methane to more useful chemicals and fuels: a challenge for the 21st century – Catalysis Today
- CDC – Handbook for Methane Control in Mining


