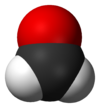
Формалдехид
Формалдехид или метанал (HCHO) је гасовито једињење растворљиво у води и најједноставнији алдехид (R-CHO).[14] Тривијално име ове супстанце потиче од њене сличности и односа са формичном киселином. Обично се чува растворен у води под називом формалин (37% формалдехида и око 15% метанола у води), или у облику чврстог полимера - параформалдехида (параформ).
| |||

| |||
| Називи | |||
|---|---|---|---|
| Преферисани IUPAC назив
Формалдехид[1] | |||
| Системски IUPAC назив
Метанал[1] | |||
| Други називи
Метил алдехид
Метилен гликол Метилен оксид Формалин (водени раствор) Формол Карбонил хидрид | |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| 3DMet | B00018 | ||
| Бајлштајн | 1209228 | ||
| ChEBI | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.002 | ||
| EC број | 200-001-8 | ||
| Е-бројеви | E240 (конзерванси) | ||
| Гмелин Референца | 445 | ||
| KEGG[2] | |||
| MeSH | Formaldehyde | ||
| RTECS | LP8925000 | ||
| UNII | |||
| UN број | 2209 | ||
| |||
| |||
| Својства[9] | |||
| CH2O | |||
| Моларна маса | 30,03 g·mol−1 | ||
| Агрегатно стање | безбојни гас | ||
| Густина | 0,8153 g/cm³ (−20 °C)[5] | ||
| Тачка топљења | −92 °C (−134 °F; 181 K) | ||
| Тачка кључања | −19 °C (−2 °F; 254 K)[5] | ||
| 400 g dm−3 | |||
| log P | 0.350 | ||
| Напон паре | < 1 atm[6] | ||
| Киселост (pKa) | 13,27 [7][8] | ||
| Магнетна сусцептибилност | -18.6·10−6 cm³/mol | ||
| Диполни момент | 1.85 D | ||
| Структура | |||
| C2v | |||
| Облик молекула (орбитале и хибридизација) | Тригонална планарна | ||
| Фармакологија | |||
| QP53AX19 (WHO) | |||
| Опасности | |||
| Безбедност приликом руковања | MSDS | ||
ЕУ класификација (DSD)
|
Toxic (T) Corrosive (C) Carc. Cat. 1 | ||
| R-ознаке | R23/24/25 R34 R43 R45 | ||
| S-ознаке | (S1/2) S26 S36/37/39 S45 S51 S53 S60 | ||
| NFPA 704 | |||
| Тачка паљења | 64 °C (147 °F; 337 K) | ||
| 430 °C (806 °F; 703 K) | |||
| Експлозивни лимити | 7–73% | ||
| Смртоносна доза или концентрација (LD, LC): | |||
LD50 (средња доза)
|
100 mg/kg (орално, пацов)[12] | ||
LC50 (средња концетрација)
|
333 ppm (миш, 2 h) 815 ppm (пацов, 30 min)[13] | ||
LCLo (најнижа објављена)
|
333 ppm (мачка, 2 h)[13] | ||
| Границе изложености здравља у САД (NIOSH): | |||
PEL (дозвољено)
|
TWA 0.75 ppm ST 2 ppm (као формалдехид и формалин)[10][11] | ||
REL (препоручено)
|
Ca TWA 0.016 ppm C 0.1 ppm [15-минута][10] | ||
IDLH (тренутна опасност)
|
Ca [20 ppm][10] | ||
| Сродна једињења | |||
Сродна алдехиди
|
Ацеталдехид Бутиралдехид | ||
Сродна једињења
|
метанол мравља киселина | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |||
| Референце инфокутије | |||
Најчешће се примењује у индустрији пластичних маса,[15] бакелита и коже и као дезинфекционо средство. Формалдехид је важан прекурзор многих других материјала и хемијских једињења. Године 1996, инсталирани капацитет производње формалдехида је био процењен на 8,7 милиона тона годишње.[14] Он се првенствено користи у производњи индустријских резина, нпр. за иверицу и превлаке.
С обзиром на његову широку употребу, токсичност и нестабилност, формалдехид представља значајну опасност за људско здравље.[16] Године 2011, Национални токсиколошки програм САД је описао формалдехид као материју за коју је „познато да је канцерогена за људе”.[17][18][19]
Форме формалдехида уреди
Формалдехид је сложенији од многих једноставних једињења угљеника у смислу да поприма неколико различитих облика. Ова једињења се често могу користити наизменично и могу се међусобно конвертовати.
- Као гас, молекуларни формалдехид је безбојан и има карактеристични оштар, иритантан задах. Стабилан је на око 150 °C, али се полимеризује када се кондензује у течност. Након кондензације, гас прелази у разне друге облике формалдехида (са различитим хемијским формулама) који су од веће практичне вриједности.
- Један важан дериват је циклични тримерни метаформалдехид (1,3,5-триоксан) са формулом (CH2O)3. То је бела чврста супстанца која се раствара без деградације у органским растварачима.
- Такође постоји и линеарни полимер који се зове параформалдехид, са формулом HO(CH2O)nH. Ово једињење такође постоји у равнотежи са различитим олигомерима (кратким полимерима), у зависности од концентрације и температуре. Засићени водени раствор, од око 40% формалдехида по запремини или 37% по маси, назива се „100% формалин”.
Кад се раствори у води, формалдехид исто тако формира хидрат, метандиол, са формулом H2C(OH)2. Ово једињење такође постоји у равнотежи са разним олигомерима (кратким полимерима), у зависности од концетнрације и температуре. Засићени водени раствор, са око 40% формалдехида по запремини или 37% по маси, се назива „100% формалин”. Мала количина стабилизатора, као што је метанол, се обично додаје да би се потиснула оксидација и полимеризација. Типични комерцијални формалин може да садржи 10–12% метанола и разне маталне нечистоће. Име је давно формулисано из једног старог трговачког имена, „Формалин”.[20]
„Формалдехид“ је први пут коришћен као генерички заштитни знак 1893. године након претходног трговачког назива, „формалин“.[21]
- Главни облици формалдехида
-
Мономерни формалдехид (предмет овог чланка)
-
Триоксан је стабилан циклични тример формалдехида.
-
Параформалдехид је уобичајен облик формалдехида за индустријску примену.
-
Метандиол, преовлађујућа врста у разблаженим воденим растворима формалдехида
Структура и везивање уреди
Молекуларни формалдехид садржи централни атом угљеника са двоструком везом за атом кисеоника и једноструком везом за сваки атом водоника. Ова структура је резимирана кондензованом формулом H2C=O.[22] Молекул је раван, у облику слова Y и његова молекуларна симетрија припада C2v групи тачака.[23] Прецизна молекуларна геометрија гасовитог формалдехида одређена је дифракцијом гасних електрона[22][24] и микроталасном спектроскопијом.[25][26] Дужина везе је 1,21 Å за везу угљеник-кисеоник[22][24][25][26][27] и око 1,11 Å за везу угљеник-водоник,[22][24][25][26] док је угао везе H–C–H 117°,[25][26] близу угла од 120° који се налази у идеалном тригоналном планарном молекулу.[22] Нека побуђена електронска стања формалдехида су пре пирамидална него планарна као у основном стању.[27]
Заступљеност уреди
Процеси у горњим слојевима атмосфере доприносе са до 90% укупног формалдехида у животној средини. Формалдехид је интермедиер оксидације (или сагоревања) метана, као и других једињења угљеника, нпр. у шумским пожарима, аутомобилским издувним гасовима, и дуванском диму. Кад се формира у атмосфери дејством сунчеве светлости и кисеоника на атмосферски метан и друге угљоводонике, он постаје део смога. Формалдехид је исто тако детектован у свемиру (погледајте испод).
Формалдехид и његови адукти су свеприсутни у живим организмима. Он се формира при метаболизму ендогених аминокиселина и присутан је у људском крвотоку, као и код других примата, у концентрацијама од приближно 0,1 mmol/l.[28] Експерименти у којима су животиње изложене атмосфери која садржи изотопски обележени формалдехид су демонстрирали да чак и код намерно изложених животиња, највећи део формалдехид-ДНК адуката је присутан у нереспираторним ткивима, и изведен је из ендогено формираног формалдехида.[29]
Формалдехид се не акумулира у животној средини, већ се разлаже у току неколико часова дејством сунчеве светлости или бактерија присутних у земљишту или води. Људи брзо метаболизују формалдехид, конвертујући га у форминску киселину, тако да се не акумулира у телу.[30]
Међузвездани формалдехид уреди
Формалдехид је био први полиатомски органски молекул који је откривен у међузвезданом медијуму.[31] Од његовог почетног откривања 1969. године, он је уочен у многим областима наше галаксије. Услед широко распрострањеног интереса за међузвездани формалдехид, он је недавно детаљно проучаван, што је довело до идентификације нових вангалактичких извора.[32] Предложени механизам формирања путем хидрогенације CO леда је приказан испод.[33]
- H + CO → HCO
- HCO + H → CH2O (константа брзине = 9,2×10−3 s−1)
Присуство формалдехида је користан индикатор за астрохемичаре, услед његове ниске реактивности у гасној фази и чињенице да су 110←111 и 211←212 K-дублетни прелази прилично јасни.
Дана 11. августа 2014, астрономи су по први пут објавили студије спроведене користећи ALMA интерферометар, у којима су дате детаљне дистрибуције HCN, HNC, H2CO, и прашине унутар кома комета C/2012 F6 (Lemmon) и C/2012 S1 (ISON).[34][35]
Синтеза и индустријска производња уреди
Лабораторијска синтеза уреди
Формалдехид је први пријавио 1859. године руски хемичар Александар Бутлеров (1828–1886).[36] У свом раду, Бутлеров је формалдехид назвао „диоксиметилен“ (метилен диоксид) [страна 247] јер је његова емпиријска формула била нетачна (C4H4O4). Коначно га је идентификовао Август Вилхелм фон Хофман, који је први најавио производњу формалдехида пропуштањем метанолне паре у ваздуху преко вруће платинасте жице.[37][38] Уз модификације, Хофманов метод остаје основа данашње индустријске руте.
Путеви добијања формалдехида из растова укључују оксидацију метанола или метил јодида.[39]
Индустрија уреди
Формалдехид се индустријски производи каталитичком оксидацијом метанола. Најчешћи катализатори су метално сребро, гвожђе(III) оксид,[40] гвожђе молибден оксиди [нпр. гвожђе(III) молибдат] са површином обогаћеном молибденом,[41] или оксиди ванадијума. У уобичајеном формокс процесу, метанол и кисеоник реагују на око 250–400°C у присуству оксида гвожђа у комбинацији са молибденом и/или ванадијумом за производњу формалдехида према хемијској једначини:[14]
- 2 CH3OH + O2 → 2 CH2O + 2 H2O
Катализатор на бази сребра обично делује на вишој температури, око 650 °C. Две хемијске реакције на њему истовремено производе формалдехид: она приказана горе и реакција дехидрогенације:
- CH3OH → CH2O + H2
У принципу, формалдехид би могао настати оксидацијом метана, али овај пут није индустријски одржив јер се метанол лакше оксидира од метана.[14]
Биохемија уреди
Формалдехид се производи на неколико начина употребом ензимске катализе.[42] Аминокиселина серин је извор природног формалдехида према овој реакцији, која производи глицин.[43]
- HOCH2CH(NH2)CO2H → CH2O +H2C(NH2)CO2H
Ову реакцију катализује серин хидроксиметилтрансфераза, ензим који садржи PLP.
Формалдехид такође могу да произведу метилотрофни микроби из метанола кроз реакцију:
- CH3OH → CH2O + 2e- + 2H+
Ову реакцију катализује ензим метанол дехидрогеназа. Други путеви до формалдехида укључују оксидативне деметилације. Формалдехид се катаболише алкохолном дехидрогеназом.
Органска хемија уреди
Формалдехид је градивни блок у синтези многих других једињења од специјализованог и индустријског значаја. Он манифестује већину хемијских својстава других алдехида, али је реактивнији.
Полимеризација и хидратација уреди
Гасни формалдехид се полимеризује на активним местима зидова посуда, али механизам реакције је непознат.[44] Мале количине хлороводоника (или бор трифлуорида, или калајног хлорида) присутне у гасовитом формалдехиду обезбеђују каталитички ефекат и убрзавају полимеризацију.[45] Мономерни CH2O је гас и ретко се среће у лабораторији.
Формалдехид у воденим растворима, за разлику од неких других малих алдехида (којима су потребни специфични услови за олигомеризацију кроз алдолну кондензацију) олигомеризује се спонтано у уобичајеном стању. Тример 1,3,5-триоксан ((CH
2O)
3) је типичан олигомер. Изоловани су многи циклични олигомери других величина. Слично томе, формалдехид се хидратизује да би се добио геминални диол метандиол, који се даље кондензује и формира олигомере HO(CH2O)nH са хидрокси-завршним деловима. Полимер се назива параформалдехид. Што је већа концентрација формалдехида - то се више равнотежа помера ка полимеризацији. Разблаживање водом или повећање температуре раствора, као и додавање алкохола (као што су метанол или етанол) смањује ту тенденцију.
Оксидација и редукција уреди
Формалдехид се лако оксидује атмосферским кисеоником у мрављу киселину. Из тог разлога, комерцијални формалдехид је обично контаминиран мрављом киселином. Формалдехид се може хидрогенисати у метанол.
У Канизаровој реакцији, формалдехид и база реагују да би произвели мрављу киселину и метанол, реакцијом диспропорционисања.
Хидроксиметилација и хлорометилација уреди
Формалдехид реагује са многим једињењима, што доводи до хидроксиметилације:
- X-H + CH2O → X-CH2OH
(X = R2N, RC(O)NR', SH). Добијени деривати хидроксиметила обично даље реагују. Дакле, амини дају хексахидро-1,3,5-триазине:
- 3 RNH2 + 3 CH2O → (RNCH2)3 + 3 H2O
Слично томе, када се комбинује са водоник сулфидом, формира тритиан:[46]
- 3 CH2O + 3 H2S → (CH2S)3 + 3 H2O
У присуству киселина, учествује у реакцијама електрофилне ароматске супституције са ароматичним једињењима које резултирају хидроксиметилованим дериватима:
- ArH + CH2O → ArCH2OH
Када се спроводе у присуству хлороводоника, производ је хлорометилно једињење, као што је описано у Бланковој хлорометилацији. Ако је арен богат електронима, као у фенолима, долази до сложених кондензација. Са 4-супституисаним фенолима добијају се каликсарени.[47] Фенол доводи до полимера.
Друге реакције уреди
Многе аминокиселине реагују са формалдехидом.[42] Цистеин се претвара у тиопролин.
Употребе уреди
Индустријске примене уреди
Формалдехид је уобичајени претходник сложенијих једињења и материјала. Приближним редоследом величине потрошње, производи добијени од формалдехида укључују уреа формалдехидну смолу, меламинску смолу, фенол формалдехидну смолу, полиоксиметиленске пластике, 1,4-бутандиол и метилен дифенил диизоцијанат.[14] Текстилна индустрија користи смоле на бази формалдехида као финишере како би се тканине учиниле отпорним на гужвање.[48]
Када се третира фенолом, уреом или меламином, формалдехид производи, респективно, тврду термореактивну фенол формалдехидну смолу, уреа формалдехидну смолу и меламинску смолу. Ови полимери су трајни лепкови који се користе у шперплочи и теписима. Такође се од њих праве пене да би се направила изолација или се изливају у обликоване производе. Производња формалдехидних смола чини више од половине потрошње формалдехида.
Формалдехид је исто тако прекурсор полифункционалних алкохола као што је пентаеритритол, који се користи за прављење боја и експлозива. Остали деривати формалдехида укључују метилен дифенил диизоцијанат, важну компоненту у полиуретанским бојама и пенама, и хексамин, који се користи у фенол-формалдехидним смолама, као и у експлозивном RDX.
Кондензација са ацеталдехидом даје пентаеритритол, хемикалију неопходну за синтезу PETN-а, снажног експлозива.[49] Кондензација са фенолима даје фенол-формалдехидне смоле.
Специјализоване примене уреди
Дезинфекционо средство и биоцид уреди
Водени раствор формалдехида може бити користан као дезинфекционо средство јер убија већину бактерија и гљивица (укључујући њихове споре). Користи се као адитив у производњи вакцина за инактивацију токсина и патогена.[50] Средства ослобађања формалдехида се користе као биоциди у производима за личну негу као што је козметика. Иако су присутна у нивоима који се иначе не сматрају штетним, познато је да изазивају алергијски контактни дерматитис код извесних сензибилизираних особа.[51]
Акваристи користе формалдехид као третман за паразите Ichthyophthirius multifiliis и Cryptocaryon irritans.[52] Формалдехид је један од главних дезинфекционих средстава који се препоручују за уништавање антракса.[53]
Формалдехид је такође одобрен за употребу у производњи сточне хране у САД. То је антимикробни агенс који се користи за одржавање комплетне сточне хране или састојака хране за животиње са негативним салмонелом до 21 дан.[54]
Формалдехид се обично користи за дезинфекцију (путем фумигације, прскалица и саоница за прскање) објеката за смештај живине и свиња, мрестилишта јаја, просторија, железничких вагона, кућица за печурке, алата и опреме. Формалдехид је вредан упаковани конзерванс у индустрији хране и пића.[55]
Фиксатор ткива и средство за балзамирање уреди
Формалдехид чува или фиксира ткиво или ћелије. Процес укључује унакрсно повезивање примарних амино група. Европска унија је забранила употребу формалдехида као биоцида (укључујући балзамирање) према Директиви о биоцидним производима (98/8/EC) због његових канцерогених својстава.[56][57] Земље са јаком традицијом балзамирања лешева, као што су Ирска и друге земље са хладнијим временом, изразиле су забринутост. Упркос извештајима који говоре супротно,[58] није донета одлука о укључивању формалдехида у Анекс I Директиве о биоцидним производима за тип производа 22 (течности за балзамирање и таксидермисте) према подацима из септембар 2009. године.[59]
Унакрсно повезивање засновано на формалдехиду се користи у геномским експериментима ChIP-on-chip или ChIP-секвенцирање, где су протеини који се везују за ДНК унакрсно повезани са својим сродним местима везивања на хромозому и анализирани да би се утврдило који гени су регулисани тим протеинима. Формалдехид се такође користи као денатурирајући агенс у РНК гел електрофорези, спречавајући РНК да формира секундарне структуре. Раствор 4% формалдехида фиксира узорке патолошког ткива на око један mm на сат на собној температури.
Тестирање на дрогу уреди
Формалдехид и 18 M (концентрована) сумпорна киселина чине Маркизов реагенс — који може да идентификује алкалоиде и друга једињења.
Фотографија уреди
У фотографији, формалдехид се користи у ниским концентрацијама за стабилизацију процеса Ц-41 (негативни филм у боји) у завршном кораку прања,[60] као и у кораку пре избељивања процеса Е-6, како би завршно прање не би било неопходно.
Безбедност уреди
С обзиром на његову широку употребу, токсичност и испарљивост, формалдехид представља значајну опасност по људско здравље.[16][61] Године 2011, амерички Национални токсиколошки програм описао је формалдехид као материју за коју се „за коју се зна да је канцерогена за људе“.[17][18][19]
Хронична инхалација уреди
Забринутост је повезана са хроничном (дуготрајном) изложеношћу удисањем, што се може десити услед термичког или хемијског разлагања смола на бази формалдехида и формирања формалдехида који је резултат сагоревања разних органских једињења (на пример, издувних гасова). Како се формалдехидне смоле користе у многим грађевинским материјалима, то је један од чешћих загађивача ваздуха у затвореном простору.[62] У концентрацијама изнад 0,1 ppm у ваздуху, формалдехид може да иритира очи и слузокожу.[63] Формалдехид који се удише у овој концентрацији може да изазове главобољу, пецкање у грлу и отежано дисање, и може подстаћи или погоршати симптоме астме.[64][65]
CDC сматра формалдехид системским отровом. Тровање формалдехидом може изазвати трајне промене у функцијама нервног система.[66]
Једна канадска студија из 1988. године о кућама са изолацијом од уреа-формалдехидне пене открила је да нивои формалдехида од чак 0,046 ppm имају позитивну корелацију са иритацијом очију и носа.[67] Преглед студија из 2009. године показао је снажну повезаност између изложености формалдехиду и развоја астме у детињству.[68]
Теорија за карциногенезу формалдехида је предложена 1978. године.[69] Године 1987, Агенција за заштиту животне средине Сједињених Држава (EPA) га је класификовала као вероватни канцероген за људе, а након више студија СЗО Међународна агенција за истраживање рака (IARC) 1995. га је такође класификовала као вероватни карциноген за људе. Даље информације и процена свих познатих података навели су IARC да поново класификује формалдехид као познати хумани канцероген[70] који је повезан са раком синуса носа и раком назофаринкса.[71] Студије из 2009. и 2010. такође су показале позитивну корелацију између изложености формалдехиду и развоја леукемије, посебно мијелоидне леукемије.[72][73] Назофарингеални и синоназални карциноми су релативно ретки, са комбинованом годишњом инциденцом у Сједињеним Државама од < 4.000 случајева.[74][75] Око 30.000 случајева мијелоидне леукемије јавља се у Сједињеним Државама сваке године.[76][77] Неки докази сугеришу да изложеност формалдехиду на радном месту доприноси настанку синоназалног карцинома.[78] Професионалци који су били изложени формалдехиду у свом занимању, као што су радници у погребној индустрији и балзамери, показали су повећан ризик од леукемије и рака мозга у поређењу са општом популацијом.[79] Други фактори су важни у одређивању индивидуалног ризика за развој леукемије или рака назофаринкса.[78][80][81] У квасцу је утврђено да формалдехид ремети путеве за поправку ДНК и ћелијски циклус.[82]
У стамбеном окружењу, изложеност формалдехиду долази са више рута. Формалдехид се може емитовати из третираних дрвених производа, као што су шперплоча или иверица, али се производи бојама, лаковама, завршним обрадама подова и пушењем цигарета.[83] У јулу 2016. године, Америчка агенција за заштиту животне средине објавила је предобјавну верзију свог коначног правила о стандардима за емисију формалдехида за композитне дрвне производе.[84] Ова нова правила утичу на произвођаче, увознике, дистрибутере и трговце на мало производа који садрже композитно дрво, укључујући плоче од влакана, иверице и различите ламиниране производе, који морају да испуњавају строжије захтеве за евидентирање и обележавање.[85]
| Аудио-записи | |
|---|---|
| „Епизода 202: Где су нестале све FEMA камп приколице? Праћење токсичности од настанка до бума“, Дестилације, 2. септембар 2015, Институт за историју науке | |
| Видео-записи | |
| Где су нестале све камп приколице?, Видео Мариел Кар (видеограф) & Ник Шапиро (истраживач), 2015, Институт за историју науке |
Америчка EPA не дозвољава више од 0,016 ppm формалдехида у ваздуху у новим зградама изграђеним за ту агенцију.[86] Студија Америчке агенције за заштиту животне средине је утврдила да је једна просечна нова кућа имала 0,0766 ppm када је потпуно нова и 0,0456 ppm након 30 дана.[87] Федерална агенција за ванредне ситуације (FEMA) је такође објавила ограничења за нивое формалдехида у камп приколицама које је купила та агенција.[88] ЕПА препоручује употребу пресованих производа од пресованог дрвета са фенолом уместо смоле урее како би се ограничила изложеност формалдехиду, пошто су производи од пресованог дрвета који садрже формалдехидне смоле често значајан извор формалдехида у кућама.[71]
Очи су најосетљивије на излагање формалдехиду: Најнижи ниво на коме многи људи могу да почну да осећају мирис формалдехида креће се између 0,05 и 1 ppm. Максимална вредност концентрације на радном месту је 0,3 ppm.[89] У контролисаним студијама у комори, појединци почињу да осећају иритацију очију на око 0,5 ppm; 5 до 20 процената пријавило је иритацију ока при 0,5 до 1 ppm; а већа сигурност за сензорну иритацију се јавља при 1 ppm и више. Док су неке агенције користиле ниво од чак 0,1 ppm као праг за иритацију, стручни панел је открио да би ниво од 0,3 ppm заштитио од скоро свих иритација. Заправо, стручни панел је открио да би ниво од 1,0 ppm избегао иритацију ока – најосетљивију крајњу тачку – код 75–95% свих људи који су били изложени.[90]
На нивое формалдехида у грађевинском окружењу утичу бројни фактори. То укључује моћ присутних производа који емитују формалдехид, однос површине материјала који емитују према запремини простора, факторе животне средине, старост производа, интеракције са другим материјалима и услове вентилације. Формалдехид се емитује из разних грађевинских материјала, намештаја и потрошачких производа. Три производа који емитују највеће концентрације су влакнасте плоче средње густине, шперплоча од тврдог дрвета и иверица. Фактори околине као што су температура и релативна влажност могу подићи нивое, јер формалдехид има висок притисак паре. Нивои формалдехида у грађевинским материјалима су највиши када се зграда први пут отвори, јер материјали имају мање времена за испуштање гаса. Нивои формалдехида се временом смањују како се извори потискују.
У операционим салама, формалдехид се производи као нуспродукт електрохирургије и присутан је у хируршком диму, излажући хирурге и здравствене раднике потенцијално небезбедним концентрацијама.[91]
Нивои формалдехида у ваздуху могу се узорковати и тестирати на неколико начина, укључујући импингер, третирани сорбент и пасивне мониторе.[92] Национални институт за безбедност и здравље на раду САД (NIOSH) има методе мерења под нумеричким бројевима 2016, 2541, 3500 и 3800.[93]
У јуну 2011, дванаесто издање Извештаја о канцерогенима (RoC) Националног токсиколошког програма (NTP) променило је листни статус формалдехида са „разумно се очекује да буде канцероген за људе“ у „познато да је канцероген за људее“.[17][18][19] Истовремено, сазван је комитет Националне академије наука (NAS) који је издао независну ревизију нацрта америчке EPA IRIS процене формалдехида, пружајући свеобухватну процену утицаја на здравље и квантитативне процене ризика од штетних ефеката код људи.[94]
Акутна иритација и алергијска реакција уреди
За већину људи, иритација од формалдехида је привремена и реверзибилна, иако формалдехид може изазвати алергије и део је стандардне серије печ тестова. У периоду 2005–2006, био је седми најзаступљенији алерген у печ тестовима (9,0%).[95] Људима са алергијом на формалдехид се саветује да избегавају ослобађиваче формалдехида (нпр. кватернијум-15, имидазолидинил уреу и диазолидинил уреу).[96] Људи који пате од алергијских реакција на формалдехид имају тенденцију да испоље лезије на кожи у областима које су имале директан контакт са супстанцом, као што су врат или бутине (често због формалдехида који се ослобађа из обрађене одеће) или дерматитиса на лицу (типично од козметике).[51] Формалдехид је забрањен у козметици у Шведској и у Јапану.[97]
Друге руте уреди
Формалдехид се природно јавља и представља „есенцијални интермедијер у ћелијском метаболизму код сисара и људи.“[14] Према Америчком савету за хемију, „Формалдехид се налази у сваком живом систему — од биљака преко животиња до људи. Брзо се метаболише у телу, брзо се распада, није истрајан и не акумулира се у телу.“[98]
Дванаесто издање NTP Извештаја о канцерогенима примећује да „храна и вода садрже мерљиве концентрације формалдехида, али је значај гутања као извора изложености формалдехиду за општу популацију упитан“. Формалдехид у храни се углавном јавља у везаном облику, и формалдехид је нестабилан у воденом раствору.[19]
Код људи, гутање само 30 ml (1,0 US fl oz) 37% раствора формалдехида може изазвати смрт. Остали симптоми повезани са уносом таквог раствора укључују гастроинтестинално оштећење (повраћање, бол у стомаку) и систематско оштећење (вртоглавица).[66] Тестирање на формалдехид се врши путем крви и/или урина гасном хроматографијом-масеном спектрометријом. Друге методе укључују инфрацрвену детекцију, гасне детекторске цеви итд, од којих је течна хроматографија високих перформанси најосетљивија.[99]
Регулација уреди
Неколико чланака на вебу тврди да је формалдехид забрањен за производњу или увоз у Европску унију (ЕУ) према REACH (Регистрација, евалуација, ауторизација и ограничење хемијских супстанци) законодавству. То је погрешно схватање, јер формалдехид није наведен у Анексу I уредбе (ЕЗ) бр. 689/2008 (пропис о извозу и увозу опасних хемикалија), нити на листи приоритета за процену ризика. Међутим, формалдехид је забрањен за употребу у одређеним видовима примене (конзерванси за системе за хлађење и прераду течности, слимициди, конзерванси за флуидну обраду метала, и антивегетативни производи) према Директиви о биоцидним производима.[100][101] У ЕУ максимална дозвољена концентрација формалдехида у готовим производима је 0,2%, а сваки производ који прелази 0,05% мора да садржи упозорење да производ садржи формалдехид.[51]
У Сједињеним Државама, Конгрес је 7. јула 2010. усвојио закон који се односи на употребу формалдехида у шперплочи од тврдог дрвета, иверици и плочама од влакана средње густине. Предлог закона је ограничио дозвољену количину емисија формалдехида из ових производа од дрвета на 0,09 ppm и захтева од компанија да испуне овај стандард до јануара 2013. године.[102] Коначно правило америчке ЕПА специфицира максималну емисију од „0,05 ppm формалдехида за шперплочу од тврдог дрвета, 0,09 ppm формалдехида за иверицу, 0,11 ppm формалдехида за плоче од влакана средње густине и 0,13 ppm формалдехида за танке плоче средње густине.“[103]
Канадски Закон о заштити животне средине из 1999. године прогласио је формалдехид токсичном супстанцом.[104]
FDA предлаже забрану релаксатора за косу са формалдехидом због забринутости за изазивање рака.[105]
Загађивач у храни уреди
Скандали страха од хране су избили у Индонезији 2005. и у Вијетнаму 2007. у вези са додатком формалдехида у храну како би се продужио рок трајања. Године 2011, након четворогодишњег одсуства, индонежанске власти су откриле да се храна са формалдехидом продаје на тржиштима у бројним регионима широм земље.[106] У августу 2011. године, Пододељење за стоку и рибарство централне Џакарте пронашло је у најмање у два Карфор супермаркета чендол који садржи 10 делова на милион формалдехида.[107] Године 2014, власник две фабрике резанаца у Богору у Индонезији ухапшен је због употребе формалдехида у резанцима. Заплењено је 50 kg формалдехида.[108] Храна за коју се зна да је контаминирана укључивала је резанце, слану рибу и тофу. Причало се да су пилетина и пиво такође контаминирани. У неким местима, као што је Кина, произвођачи још увек илегално користе формалдехид као конзерванс у храни, што људе излаже конзумацији формалдехида.[109] Почетком 1900-их, америчке фабрике млека су га често додавале у флаше за млеко као метод пастеризације због недостатка знања и забринутости[110] у вези са токсичношћу формалдехида.[111][112]
Године 2011, у Након Ратчасими, Тајланд, камиони труле пилетине за продају третирани су формалдехидом у шта је била умешана „велика мрежа“, укључујући 11 кланица којима управља криминална група.[113] Године 2012, пронађена је пошиљка риба вредна 1 милијарду рупија (скоро 100.000 америчких долара) увезене из Пакистана у Батам, Индонезија, контаминирана формалдехидом.[114]
Контаминација хране формалином је пријављена у Бангладешу, у продавницама и супермаркетима који продају воће, рибу и поврће које је третирано формалином да би остало свеже.[115] Међутим, 2015. године, у Парламенту Бангладеша усвојен је Закон о контроли формалина који предвиђа доживотну казну затвора као максималну казну, као и максималну казну од 2.000.000 БДТ, али не мање од 500.000 БДТ за увоз, производњу или складиштење формалина без дозволе.[116]
Формалдехид је био једна од хемикалија коришћених у индустријализованој производњи хране у 19. веку коју је истраживао др Харви В. Вајли са својим чувеним 'Отровним одредом' као део америчког Министарства пољопривреде. Ово је довело до Закона о чистој храни и лековима из 1906. године, значајног догађаја у раној историји регулације хране у Сједињеним Државама.
Референце уреди
- ^ а б Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. стр. 908. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-FP001.
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б Formaldehyde (PDF) Архивирано на сајту Wayback Machine (13. јун 2018), SIDS Initial Assessment Report, International Programme on Chemical Safety
- ^ Spence, Robert, and William Wild. "114. The vapour-pressure curve of formaldehyde, and some related data." Journal of the Chemical Society (Resumed) (1935): 506-509
- ^ „PubChem Compound Database; CID=712”. Nacionalni centar za biotehnološke informacije. Приступљено 8. 7. 2017.
- ^ http://chemistry.stackexchange.com/questions/12232/acidity-of-aldehydes
- ^ Weast, Robert C., ур. (1981). CRC Handbook of Chemistry and Physics (62nd изд.). Boca Raton, FL: CRC Press. стр. C—301, E—61. ISBN 0-8493-0462-8.
- ^ а б в NIOSH Џепни водич хемијских хазарда. „#0293”. Nacionalni institut za bezbednost i zdravlje na radu (NIOSH).
- ^ NIOSH Џепни водич хемијских хазарда. „#0294”. Nacionalni institut za bezbednost i zdravlje na radu (NIOSH).
- ^ http://chem.sis.nlm.nih.gov/chemidplus/rn/50-00-0
- ^ а б „Formaldehyde”. Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ а б в г д ђ „Formaldehyde”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. 2005. doi:10.1002/14356007.a11_619.
- ^ Read, J. (1935), Text-Book of Organic Chemistry, London: G Bell & Sons.
- ^ а б „Formaldehyde”, Formaldehyde, 2-Butoxyethanol and 1-tert-Butoxypropan-2-ol (PDF), IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 88, Lyon, France: International Agency for Research on Cancer, 2006, стр. 39—325, ISBN 978-92-832-1288-1 „Formaldehyde (gas)”, Report on Carcinogens, Eleventh Edition (PDF), U.S. Department of Health and Human Services, Public Health Service, National Toxicology Program, 2005
- ^ а б в Harris, Gardiner (10. 6. 2011). „Government Says 2 Common Materials Pose Risk of Cancer”. New York Times. Приступљено 11. 6. 2011.
- ^ а б в National Toxicology Program (10. 6. 2011). „12th Report on Carcinogens”. National Toxicology Program. Архивирано из оригинала 8. 6. 2011. г. Приступљено 11. 6. 2011.
- ^ а б в г National Toxicology Program (10. 6. 2011). „Report On Carcinogens – Twelfth Edition – 2011” (PDF). National Toxicology Program. Приступљено 11. 6. 2011.
- ^ Merriam-Webster, Merriam-Webster's Collegiate Dictionary, Merriam-Webster, Архивирано из оригинала 10. 10. 2020. г., Приступљено 28. 03. 2019.
- ^ Formalin, Merriam-Webster, Inc., 15. 1. 2020, Приступљено 18. 2. 2020
- ^ а б в г д Wells, A. F. (1984). Structural Inorganic Chemistry (5th изд.). Oxford University Press. стр. 915–917, 926. ISBN 978-0-19-965763-6.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (II изд.). Oxford: Butterworth-Heinemann. стр. 1291. ISBN 0080379419.
- ^ а б в Chuichi, Kato; Shigehiro, Konaka; Takao, Iijima; Masao, Kimura (1969). „Electron Diffraction Studies of Formaldehyde, Acetaldehyde and Acetone”. Bull. Chem. Soc. Jpn. 42 (8): 2148—2158. doi:10.1246/bcsj.42.2148 .
- ^ а б в г William M. Haynes, ур. (2012). CRC Handbook of Chemistry and Physics (93rd изд.). CRC Press. стр. 9–39. ISBN 978-1439880500.
- ^ а б в г Duncan, J. L. (1974). „The ground-state average and equilibrium structures of formaldehyde and ethylene”. Mol. Phys. 28 (5): 1177—1191. Bibcode:1974MolPh..28.1177D. doi:10.1080/00268977400102501.
- ^ а б Smith, Michael B.; March, Jerry (2007). March's Advanced Organic Chemistry (6th изд.). John Wiley & Sons. стр. 24–25, 335. ISBN 978-0-471-72091-1.
- ^ „Review of the Formaldehyde Assessment in the National Toxicology Program 12th Report on Carcinogens”. стр. 91.
- ^ „Review of the Formaldehyde Assessment in the National Toxicology Program 12th Report on Carcinogens”. стр. 95.
- ^ „Formaldehyde Is Biodegradable, Quickly Broken Down in the Air By Sunlight or By Bacteria in Soil or Water”. Formaldehyde Panel of the American Chemistry Council. Приступљено 22. 4. 2017.
- ^ Zuckerman, B.; Buhl, D.; Palmer, P.; Snyder, L. E. (1970). „Observation of interstellar formaldehyde”. Astrophys. J. 160: 485—506. Bibcode:1970ApJ...160..485Z. doi:10.1086/150449.
- ^ Mangum, Jeffrey G.; Darling, Jeremy; Menten, Karl M.; Henkel, Christian (2008). „Formaldehyde Densitometry of Starburst Galaxies”. Astrophys. J. 673 (2): 832—46. Bibcode:2008ApJ...673..832M. arXiv:0710.2115 . doi:10.1086/524354.
- ^ Woon, David E. (2002). „Modeling Gas-Grain Chemistry with Quantum Chemical Cluster Calculations. I. Heterogeneous Hydrogenation of CO and H2CO on Icy Grain Mantles”. Astrophys. J. 569 (1): 541—48. Bibcode:2002ApJ...569..541W. doi:10.1086/339279.
- ^ Zubritsky, Elizabeth; Neal-Jones, Nancy (11. 8. 2014). „RELEASE 14-038 - NASA's 3-D Study of Comets Reveals Chemical Factory at Work”. NASA. Приступљено 12. 8. 2014.
- ^ Cordiner, M. A.; et al. (11. 8. 2014). „Mapping the Release of Volatiles in the Inner Comae of Comets C/2012 F6 (Lemmon) and C/2012 S1 (ISON) Using the Atacama Large Millimeter/Submillimeter Array”. The Astrophysical Journal. 792 (1): L2. Bibcode:2014ApJ...792L...2C. arXiv:1408.2458 . doi:10.1088/2041-8205/792/1/L2. Приступљено 12. 8. 2014.
- ^ Butlerow, A (1859). Ueber einige Derivate des Jodmethylens [On some derivatives of methylene iodide]. Annalen der Chemie und Pharmacie. 111. стр. 242—252.
- ^ See: A. W. Hofmann (14 October 1867) „Zur Kenntnis des Methylaldehyds”. ([Contributions] to our knowledge of methylaldehyde), Monatsbericht der Königlich Preussischen Akademie der Wissenschaften zu Berlin (Monthly Report of the Royal Prussian Academy of Sciences in Berlin), vol. 8, pages 665–669. Reprinted in:
- A.W. Hofmann, (1868) „Annalen der Chemie und Pharmacie”. Zur Kenntnis des Methylaldehyds., (Annals of Chemistry and Pharmacy), vol. 145, no. 3, pages 357–361.
- A.W. Hofmann (1868) „Zur Kenntnis des Methylaldehyds”., Journal für praktische Chemie (Journal for Practical Chemistry), vol. 103, no. 1, pages 246–250. However, it was not until 1869 that Hofmann determined the correct empirical formula of formaldehyde. See: A.W. Hofmann (5 April 1869) Beiträge zur Kenntnis des Methylaldehyds., Monatsbericht der Königlich Preussischen Akademie der Wissenschaften zu Berlin, vol. ?, pages 362–372. Reprinted in:
- Hofmann, A.W. (1869). „Beiträge zur Kenntnis des Methylaldehyds”. Journal für Praktische Chemie. 107 (1): 414—424. doi:10.1002/prac.18691070161.
- A.W. Hofmann (1869) "Beiträge zur Kenntnis des Methylaldehyds," Berichte der Deutschen Chemischen Gesellschaft (Reports of the German Chemical Society), vol. 2, pages 152–159.
- ^ Read, J. (1935). Text-Book of Organic Chemistry. London: G Bell & Sons.
- ^ Hooker, Jacob M.; Schönberger, Matthias; Schieferstein, Hanno; Fowler, Joanna S. (2008). „A Simple, Rapid Method for the Preparation of [11C]Formaldehyde”. Angewandte Chemie International Edition. 47 (32): 5989—5992. PMC 2522306 . PMID 18604787. doi:10.1002/anie.200800991.
- ^ Wang, Chien-Tsung; Ro, Shih-Hung (2005-05-10). „Nanocluster iron oxide-silica aerogel catalysts for methanol partial oxidation”. Applied Catalysis A: General (на језику: енглески). 285 (1): 196—204. ISSN 0926-860X. doi:10.1016/j.apcata.2005.02.029.
- ^ Dias, Ana Paula Soares; Montemor, Fátima; Portela, Manuel Farinha; Kiennemann, Alain (2015-02-01). „The role of the suprastoichiometric molybdenum during methanol to formaldehyde oxidation over Mo–Fe mixed oxides”. Journal of Molecular Catalysis A: Chemical (на језику: енглески). 397: 93—98. ISSN 1381-1169. doi:10.1016/j.molcata.2014.10.022.
- ^ а б Kamps, Jos J. A. G.; Hopkinson, Richard J.; Schofield, Christopher J.; Claridge, Timothy D. W. (2019). „How formaldehyde reacts with amino acids”. Communications Chemistry. 2. S2CID 207913561. doi:10.1038/s42004-019-0224-2.
- ^ Pham, Vanha N.; Bruemmer, Kevin J.; Toh, Joel D. W.; Ge, Eva J.; Tenney, Logan; Ward, Carl C.; Dingler, Felix A.; Millington, Christopher L.; Garcia-Prieto, Carlos A.; Pulos-Holmes, Mia C.; Ingolia, Nicholas T.; Pontel, Lucas B.; Esteller, Manel; Patel, Ketan J.; Nomura, Daniel K.; Chang, Christopher J. (2023). „Formaldehyde regulates S -adenosylmethionine biosynthesis and one-carbon metabolism”. Science. 382 (6670): eabp9201. doi:10.1126/science.abp9201.
- ^ Boyles, James G.; Toby, Sidney (јун 1966). „The mechanism of the polymerization of gaseous formaldehyde”. Journal of Polymer Science Part B: Polymer Letters. 4 (6): 411—415. Bibcode:1966JPoSL...4..411B. doi:10.1002/pol.1966.110040608.
- ^ Bevington, J. C.; Norrish, R. G. W. (1951-03-07). „The catalyzed polymerization of gaseous formaldehyde”. Proceedings of the Royal Society of London. Series A. Mathematical and Physical Sciences (на језику: енглески). 205 (1083): 516—529. Bibcode:1951RSPSA.205..516B. ISSN 0080-4630. S2CID 95395629. doi:10.1098/rspa.1951.0046.
- ^ Bost, R. W.; Constable, E. W. (1936). „sym-Trithiane”. Org. Synth. 16: 81.; Coll. Vol., 2, стр. 610
- ^ Gutsche, C. D.; Iqbal, M. (1993). „p-tert-Butylcalix[4]arene”. Org. Synth.; Coll. Vol., 8, стр. 75
- ^ „Formaldehyde in Clothing and Textiles FactSheet”. NICNAS. Australian National Industrial Chemicals Notification and Assessment Scheme. 2013-05-01. Архивирано из оригинала 2019-03-19. г. Приступљено 2014-11-12.
- ^ Schurink, H. B. J. (1925). „Pentaerythritol”. Org. Synth. 4: 53.; Coll. Vol., 1, стр. 425
- ^ „Ingredients of Vaccines - Fact Sheet”. Center for Disease Control. Архивирано из оригинала 2019-04-21. г. Приступљено 2018-08-04. „Formaldehyde is used to inactivate bacterial products for toxoid vaccines, (these are vaccines that use an inactive bacterial toxin to produce immunity.) It is also used to kill unwanted viruses and bacteria that might contaminate the vaccine during production. Most formaldehyde is removed from the vaccine before it is packaged.”
- ^ а б в De Groot, Anton C; Flyvholm, Mari-Ann; Lensen, Gerda; Menné, Torkil; Coenraads, Pieter-Jan (2009). „Formaldehyde-releasers: relationship to formaldehyde contact allergy. Contact allergy to formaldehyde and inventory of formaldehyde-releasers”. Contact Dermatitis. 61 (2): 63—85. PMID 19706047. S2CID 23404196. doi:10.1111/j.1600-0536.2009.01582.x. hdl:11370/c3ff7adf-9f21-4564-96e0-0b9c5d025b30 .
- ^ Francis-Floyd, Ruth (април 1996). „Use of Formalin to Control Fish Parasites”. Institute of Food and Agricultural Sciences, University of Florida. Архивирано из оригинала 27. 5. 2012. г.
- ^ „Disinfection, decontamination, fumigation, incineration”, Anthrax in Humans and Animals. 4th edition (на језику: енглески), World Health Organization, 2008, Приступљено 2023-11-20
- ^ „§573.460 Formaldehyde”. U.S. Government Publishing Office. 2019-04-19. Архивирано из оригинала 2017-05-05. г. Приступљено 2016-07-09.
- ^ „Registered Formaldehyde”. BrainerdChemical.com. 17. 11. 2023. Приступљено 17. 11. 2023.
- ^ Directive 98/8/EC of the European Parliament and of the Council of 16 February 1998 concerning the placing of biocidal products on the market. OJEU L123, 24.04.1998, pp. 1–63. (consolidated version to 2008-09-26 (PDF))
- ^ Commission Regulation (EC) No 2032/2003 of 4 November 2003 on the second phase of the 10-year work programme referred to in Article 16(2) of Directive 98/8/EC of the European Parliament and of the Council concerning the placing of biocidal products on the market, and amending Regulation (EC) No 1896/2000. OJEU L307, 24.11.2003, p. 1–96. (consolidated version to 2007-01-04 (PDF))
- ^ Patel, Alkesh (2007-07-04). „Formaldehyde Ban set for 22 September 2007”. WebWire. Архивирано из оригинала 2018-12-12. г. Приступљено 2012-05-19.
- ^ „European chemical Substances Information System (ESIS) entry for formaldehyde”. Архивирано из оригинала 2014-01-01. г. Приступљено 2009-09-01.
- ^ „Process C-41 Using Kodak Flexicolor Chemicals - Publication Z-131”. Kodak. Архивирано из оригинала 2016-06-15. г. Приступљено 2009-09-01.
- ^ "Formaldehyde (gas)", Report on Carcinogens, Eleventh Edition (PDF), U.S. Department of Health and Human Services, Public Health Service, National Toxicology Program, 2005
- ^ „Indoor Air Pollution in California” (PDF). Air Resources Board, California Environmental Protection Agency. јул 2005. стр. 65—70. Архивирано из оригинала (PDF) 2019-03-01. г. Приступљено 2012-05-19.
- ^ „Formaldehyde”. Occupational Safety and Health Administration. август 2008. Архивирано из оригинала 2019-04-11. г. Приступљено 2009-09-01.
- ^ „Formaldehyde Reference Exposure Levels”. California Office Of Health Hazard Assessment. децембар 2008. Архивирано из оригинала (PDF) 2019-03-23. г. Приступљено 2012-05-19.
- ^ „Formaldehyde and Indoor Air”. Health Canada. 2012-03-29. Архивирано из оригинала 2019-04-23. г. Приступљено 2019-04-23.
- ^ а б „Formaldehyde | Medical Management Guidelines | Toxic Substance Portal | ATSDR”. Centres for Disease Control and Prevention. Приступљено 2021-08-25.
- ^ Broder, I; Corey, P; Brasher, P; Lipa, M; Cole, P (1991). „Formaldehyde exposure and health status in households”. Environmental Health Perspectives. 95: 101—4. PMC 1568408 . PMID 1821362. doi:10.1289/ehp.9195101.
- ^ McGwin, G; Lienert, J; Kennedy, JI (новембар 2009). „Formaldehyde Exposure and Asthma in Children: A Systematic Review”. Environmental Health Perspectives. 118 (3): 313—7. PMC 2854756 . PMID 20064771. doi:10.1289/ehp.0901143.
- ^ Lobachev, AN (1978). „РОЛЬ МИТОХОНДРИАЛЬНЫХ ПРОЦЕССОВ В РАЗВИТИИ И СТАРЕНИИ ОРГАНИЗМА. СТАРЕНИЕ И РАК” [Role of mitochondrial processes in the development and aging of organism. Aging and cancer] (PDF) (на језику: руски). VINITI. Архивирано из оригинала (PDF) 2013-06-06. г. Приступљено 2012-08-01.
- ^ IARC Monographs on the Evaluation of Carcinogenic Risks to Humans - VOLUME 88 - Formaldehyde, 2-Butoxyethanol and 1-tert-Butoxypropan-2-ol (PDF). IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. WHO Press. 2006. ISBN 92-832-1288-6. Архивирано из оригинала (PDF) 2018-07-12. г. Приступљено 2019-04-23.
- ^ а б „Formaldehyde and Cancer Risk”. National Cancer Institute. 2011-06-10. Архивирано из оригинала 2019-01-23. г.
- ^ Zhang, Luoping; Steinmaus, Craig; Eastmond, Eastmond; Xin, Xin; Smith, Smith (2009). „Formaldehyde exposure and leukemia: A new meta-analysis and potential mechanisms” (PDF). Mutation Research/Reviews in Mutation Research. 681 (2–3): 150—168. PMID 18674636. doi:10.1016/j.mrrev.2008.07.002. Архивирано из оригинала (PDF) 2014-03-27. г. Приступљено 2013-05-22.
- ^ Zhang, Luoping; Freeman, Laura E. Beane; Nakamura, Jun; Hecht, Stephen S.; Vandenberg, John J.; Smith, Martyn T.; Sonawane, Babasaheb R. (2010). „Formaldehyde and Leukemia: Epidemiology, Potential Mechanisms, and Implications for Risk Assessment”. Environmental and Molecular Mutagenesis. 51 (3): 181—191. PMC 2839060 . PMID 19790261. doi:10.1002/em.20534.
- ^ „Key Statistics for Nasopharyngeal Cancer”. American Cancer Society. Архивирано из оригинала 2019-01-11. г. Приступљено 2019-04-22.
- ^ Turner JH, Reh DD (јун 2012). „Incidence and survival in patients with sinonasal cancer: a historical analysis of population-based data”. Head Neck. 34 (6): 877—85. PMID 22127982. S2CID 205857872. doi:10.1002/hed.21830.
- ^ „Key Statistics for Chronic Myeloid Leukemia”. American Cancer Society. Архивирано из оригинала 2019-04-23. г. Приступљено 2019-04-22.
- ^ „What are the key statistics about acute myeloid leukemia?Key Statistics for Acute Myeloid Leukemia (AML)”. American Cancer Society. Архивирано из оригинала 2019-04-23. г. Приступљено 2019-04-22.
- ^ а б „Risk Factors for Nasopharyngeal Cancer”. American Cancer Society. 24. 9. 2018. Архивирано из оригинала 10. 12. 2016. г. Приступљено 17. 9. 2019.
- ^ Butticè, Claudio (2015). „Solvents”. Ур.: Colditz, Graham A. The SAGE Encyclopedia of Cancer and Society (Second изд.). Thousand Oaks: SAGE Publications. стр. 1089—1091. ISBN 9781483345734. doi:10.4135/9781483345758.n530.
- ^ „Risk Factors for Acute Myeloid Leukemia (AML)”. American Cancer Society. 2018-08-21. Архивирано из оригинала 2019-04-23. г.
- ^ „Risk Factors for Chronic Myeloid Leukemia”. American Cancer Society. 2018-06-19. Архивирано из оригинала 2018-12-12. г.
- ^ Ogbede, J. U., Giaever, G., & Nislow, C. (2021). A genome-wide portrait of pervasive drug contaminants. Scientific reports, 11(1), 12487. https://doi.org/10.1038/s41598-021-91792-1
- ^ Dales, R; Liu, L; Wheeler, AJ; Gilbert, NL (2008). „Quality of indoor residential air and health”. Canadian Medical Association Journal. 179 (2): 147—52. PMC 2443227 . PMID 18625986. doi:10.1503/cmaj.070359.
- ^ „Formaldehyde Emission Standards for Composite Wood Products”. EPA. 8. 7. 2016. Архивирано из оригинала 2018-12-24. г. Приступљено 2019-04-24.
- ^ Passmore, Whitney; Sullivan, Michael J. (2016-08-04). „EPA Issues Final Rule on Formaldehyde Emission Standards for Composite Wood Products”. The National Law Review. Womble Carlyle Sandridge & Rice, PLLC. Архивирано из оригинала 2018-06-19. г. Приступљено 2016-08-24 — преко Google News.
- ^ „Testing for Indoor Air Quality, Baseline IAQ, and Materials”. Environmental Protection Agency. Архивирано из оригинала 15. 10. 2006. г.
- ^ M. Koontz, H. Rector, D. Cade, C. Wilkes, and L. Niang. 1996. Residential Indoor Air Formaldehyde Testing Program: Pilot Study. Report No. IE-2814, prepared by GEOMET Technologies, Inc. for the USEPA Office of Pollution Prevention and Toxics under EPA Contract No. 68-D3-0013, Washington, DC
- ^ Evans, Ben (2008-04-11). „FEMA limits formaldehyde in trailers”. The Boston Globe. Архивирано из оригинала 15. 6. 2010. г. Приступљено 2008-09-04.
- ^ „Formaldehyde CAS 50-00-0” (PDF). United Nations Environment Programme. Архивирано из оригинала (PDF) 2019-03-28. г. Приступљено 2019-04-25.
- ^ „Formaldehyde and Facts About Health Effects” (PDF). Formaldehyde Epidemiology, Toxicology and Environmental Group, Inc. август 2002. Архивирано из оригинала (PDF) 2011-05-11. г.
- ^ Carroll, Gregory T.; Kirschman, David L. (2023). „Catalytic Surgical Smoke Filtration Unit Reduces Formaldehyde Levels in a Simulated Operating Room Environment”. ACS Chemical Health & Safety (на језику: енглески). 30 (1): 21—28. ISSN 1871-5532. doi:10.1021/acs.chas.2c00071.
- ^ „When Sampling Formaldehyde, The Medium Matters”. Galson Labs. Архивирано из оригинала 2011-03-23. г.
- ^ „NIOSH Pocket Gide to Chemical Hazards: Formaldehyde”. National Institute for Occupational Safety and Health, CDC. 2018-11-29. Архивирано из оригинала 2019-03-28. г.
- ^ Addendum to the 12th Report on Carcinogens (PDF) National Toxicology Program, U.S. Department of Health and Human Services. Retrieved 06-13-2011
- ^ Zug KA, Warshaw EM, Fowler JF, Maibach HI, Belsito DL, Pratt MD, Sasseville D, Storrs FJ, Taylor JS, Mathias CG, Deleo VA, Rietschel RL, Marks J (2009). „Patch-test results of the North American Contact Dermatitis Group 2005-2006”. Dermatitis. 20 (3): 149—60. PMID 19470301. S2CID 24088485. doi:10.2310/6620.2009.08097.
- ^ „Formaldehyde allergy”. DermNet NZ. New Zealand Dermatological Society. 2002. Архивирано из оригинала 2018-09-23. г. Приступљено 2019-04-25.
- ^ Hayashida, Mike. „The Regulation of Cosmetics in Japan” (PDF). Архивирано из оригинала (PDF) 2019-04-14. г. Приступљено 2019-04-25.
- ^ „Formaldehyde occurs naturally and is all around us” (PDF).
- ^ Ngwa, Moise (2010-10-25). „formaldehyde testing” (PDF). Cedar Rapids Gazette. Архивирано из оригинала (PDF) 2018-10-25. г. Приступљено 2012-05-19.
- ^ „European Union Bans formaldehyde/formalin within Europe” (PDF). European Commission's Environment Directorate-General. 2007-06-22. стр. 1—3. Архивирано из оригинала (PDF) 2013-04-27. г. Приступљено 2012-05-19.
- ^ „ESIS (European Chemical Substances Information System)”. European Commission Joint Research Centre Institute for Health and Consumer Protection. фебруар 2009. Архивирано из оригинала 1. 1. 2014. г. Приступљено 19. 5. 2012.
- ^ „S.1660 - Formaldehyde Standards for Composite Wood Products Act”. GovTrack. 2010-08-25. Архивирано из оригинала 2019-04-29. г. Приступљено 2019-04-29.
- ^ „Formaldehyde Emission Standards for Composite Wood Products”. Regulations.gov. United States Federal Register. 12. 12. 2016. Архивирано из оригинала 10. 8. 2019. г. Приступљено 21. 12. 2019. „The emission standards will be 0.05 ppm formaldehyde for hardwood plywood, 0.09 ppm formaldehyde for particleboard, 0.11 ppm formaldehyde for medium-density fiberboard, and 0.13 ppm formaldehyde for thin medium-density fiberboard.”
- ^ „Health Canada - Proposed residential indoor air quality guidelines for formaldehyde”. Health Canada. април 2007. Архивирано из оригинала 2013-05-30. г.
- ^ „View Rule”. www.reginfo.gov. Приступљено 2023-10-21.
- ^ „Formaldehyde-laced foods reemerge in Indonesian markets”. antaranews.com. 2011-08-10. Архивирано из оригинала 2018-10-25. г.
- ^ „Formaldehyde-Tainted Rice Drinks Found at Carrefour Markets”. Jakarta Globe. 2011-08-22. Архивирано из оригинала 2012-09-28. г.
- ^ „BPOM Uncovers Two Formaldehyde-Tainted Noodle Factories in Bogor”. Jakarta Globe. 2014-10-12. Архивирано из оригинала 2015-08-01. г.
- ^
- Tang, Xiaojiang; Bai, Yang; Duong, Anh; Smith, Martyn T.; Li, Laiyu; Zhang, Luoping (2009). „Formaldehyde in China: Production, consumption, exposure levels, and health effects”. Environment International. 35 (8): 1210—1224. ISSN 0160-4120. PMID 19589601. doi:10.1016/j.envint.2009.06.002.
- see references cited on p. 1216 above
- „Municipality sees red over bad blood processing”. China Daily. 2011-03-18. Архивирано из оригинала 2018-10-24. г.
- ^ Blum, Deborah, 1954- (2018-09-25). The poison squad : one chemist's single-minded crusade for food safety at the turn of the twentieth century. Go Big Read (Program). New York, New York. ISBN 9781594205149. OCLC 1024107182.
- ^ „Was Death in the Milk?”. The Indianapolis News. 1900-07-31. стр. 5. Архивирано из оригинала 2018-11-17. г. Приступљено 2014-08-20 — преко Newspapers.com.
- ^ „Wants New Law Enacted. Food Inspector Farnsworth Would Have Use of Formaldehyde in Milk Stopped”. The Topeka Daily Capital. 1903-08-30. стр. 8. Архивирано из оригинала 2018-11-17. г. Приступљено 2014-08-20 — преко Newspapers.com.
- ^ „Illegal business 'being run by a gang'”. The Nation. 2011-06-16. Архивирано из оригинала 2011-06-16. г.
- ^ „Import of formaldehyde fish from Pakistan foiled in Batam”. The Jakarta Post. 2012-02-23. Архивирано из оригинала 2018-12-16. г.
- ^ „Trader Fined for Selling Fish Treated with Formalin”. The Daily Star. 2009-08-31. Архивирано из оригинала 2019-04-29. г.
- ^ „Formalin Control Bill 2015 passed”. ntv online. 2015-02-16. Архивирано из оригинала 2018-03-23. г. Приступљено 2015-03-04.
Литература уреди
- Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. стр. 908. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-FP001.
Спољашње везе уреди
- Интернационална карта хемијске безбедности 0275 (гас)
- Интернационална карта хемијске безбедности 0695 (раствор)
- NIOSH Џепни водич хемијских хазарда. „#0293”. Nacionalni institut za bezbednost i zdravlje na radu (NIOSH).
- Формалдехид из ChemSub онлајн
- Водич за превенцију — Формалдехид на радном месту (ПДФ) Архивирано на сајту Wayback Machine (10. новембар 2010) од ИРССТ
- Формалдехид према Националном институту за безбедност и здравље на раду САД
- IPCS Водич за здравље и безбедност 57: Formaldehyde
- IPCS Критеријуми здравља животне средине 89: Formaldehyde
- SIDS Иницијални извештај о процени for Formaldehyde Организације за економску сарадњу и развој (OECD)
- Формалдехид додат на листу „Познатих карциногена“ упркос лобирању хемијске индустрије
- Да ли поседујете Фемину приколицу после Катрине? Проверите свој ВИН број#
- Дакле, живите у једној од Феминих Катрининих приколица ... Шта можете да урадите?
- Формалдехид у бази података о својствима пестицида (PPDB)