Plutonijum
Plutonijum (Pu, lat. plutonium) je hemijski element iz grupe aktinoida.[2] Ime je dobio po patuljastoj planeti Plutonu.
 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Opšta svojstva | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ime, simbol | plutonijum, Pu | |||||||||||||||||||||||||||||||||||||||||||||||
| Izgled | srebrnasto beo, potamnjuje do tamno sive na vazduhu | |||||||||||||||||||||||||||||||||||||||||||||||
| U periodnome sistemu | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
| Atomski broj (Z) | 94 | |||||||||||||||||||||||||||||||||||||||||||||||
| Grupa, perioda | grupa N/D, perioda 7 | |||||||||||||||||||||||||||||||||||||||||||||||
| Blok | f-blok | |||||||||||||||||||||||||||||||||||||||||||||||
| Kategorija | aktinoid | |||||||||||||||||||||||||||||||||||||||||||||||
| Rel. at. masa (Ar) | 244,0642053(56)[1] | |||||||||||||||||||||||||||||||||||||||||||||||
| Maseni broj | 244 (najstabilniji izotop) | |||||||||||||||||||||||||||||||||||||||||||||||
| El. konfiguracija | ||||||||||||||||||||||||||||||||||||||||||||||||
po ljuskama | 2, 8, 18, 32, 24, 8, 2 | |||||||||||||||||||||||||||||||||||||||||||||||
| Fizička svojstva | ||||||||||||||||||||||||||||||||||||||||||||||||
| Tačka topljenja | 912,5 K (639,4 °C, 1182,9 °F) | |||||||||||||||||||||||||||||||||||||||||||||||
| Tačka ključanja | 3505 K (3228 °C, 5842 °F) | |||||||||||||||||||||||||||||||||||||||||||||||
| Gustina pri s.t. | 19,816 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||
| tečno st., na t.t. | 16,63 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||
| Toplota fuzije | 2,82 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Toplota isparavanja | 333,5 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Mol. topl. kapacitet | 35,5 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||
Napon pare
| ||||||||||||||||||||||||||||||||||||||||||||||||
| Atomska svojstva | ||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativnost | 1,28 | |||||||||||||||||||||||||||||||||||||||||||||||
| Energije jonizacije | 1: 584,7 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Atomski radijus | 159 pm | |||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentni radijus | 187±1 pm | |||||||||||||||||||||||||||||||||||||||||||||||
| Ostalo | ||||||||||||||||||||||||||||||||||||||||||||||||
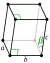
| Kristalna struktura | monoklinična | |||||||||||||||||||||||||||||||||||||||||||||||
| Brzina zvuka | 2260 m/s | |||||||||||||||||||||||||||||||||||||||||||||||
| Topl. širenje | 46,7 µm/(m·K) (na 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||
| Topl. vodljivost | 6,74 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||
| Elektrootpornost | 1,460 µΩ·m (na 0 °C) | |||||||||||||||||||||||||||||||||||||||||||||||
| Magnetni raspored | paramagnetičan | |||||||||||||||||||||||||||||||||||||||||||||||
| Jangov modul | 96 GPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Modul smicanja | 43 GPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Poasonov koeficijent | 0,21 | |||||||||||||||||||||||||||||||||||||||||||||||
| CAS broj | 7440-07-5 | |||||||||||||||||||||||||||||||||||||||||||||||
| Istorija | ||||||||||||||||||||||||||||||||||||||||||||||||
| Imenovanje | po patuljastoj planeti Plutonu, koji je imenovan po klasičnom bogu podzemlja Plutonu | |||||||||||||||||||||||||||||||||||||||||||||||
| Otkriće | Glen T. Siborg, Artur Val, Džozef Kenedi, Edvin Makmilan (1940–1) | |||||||||||||||||||||||||||||||||||||||||||||||
| Glavni izotopi | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
Plutonijum je radioaktivan metal iz grupe aktinoida.[3] prvi put dobijen i ispitan od strane američkog hemičara Glena Siborga 1941. godine. Naučnici su iskoristili uranijum, koji su bombardovali jezgrima deuterijuma (izotop vodonika). Plutonijum je veoma reaktivan. Ako dugo stoji na vazduhu prekriva se zlatnim slojem oksida. Javlja se u 6 alotropskih modifikacija i gradi jedinjenja u kojima se javlja sa četiri oksidaciona broja. Poznato je 15 izotopa plutonijuma čije se atomske mase kreću između 232 i 246. Zbog visokog stepena radioaktivnosti smrtonosan je za čoveka čak i u minimalnim količinama. Opasniji je od uranijuma zbog manje kritične mase.
Prema svom rednom broju, on je najteži element koji se nalazi u prirodi. Međutim, u prirodi se nalazi samo u tragovima unutar veoma starih stena. Tragovi ovog elementa se javljaju među rudama uranijuma. Veće količine ovog elementa dobijaju se veštački, pretežno u atomskim centralama i reaktorima. Kao jedan od malobrojnih hemijskih elemenata podložnih fisiji, igra veoma važnu ulogu za proizvodnju nuklearnog oružja. Na primer, osnovni reaktivni materijal u atomskoj bombi bačenoj 9. augusta 1945. na Nagasaki bio je plutonijum. Ovaj element nastaje tokom rada nuklearnih reaktora iz uranijumskih šipki nuklearnog goriva.
Istorija
urediPlutonijum su otkrili američki naučnici Glen T. Siborg, Artur Val, Džozef Kenedi, Majkl Kefola i Edvin Makmilan. Oni su 14. decembra 1940. izveli eksperiment u ciklotronu, bombardujući metu od uranijuma 238U atomima deuterijuma dobivši tako izotop 238Pu. Pri tom eksperimentu, najpre je napravljen uzorak 238U u obliku oksida U3O8 u tankom sloju na ploči od bakra. U ovoj reakciji emitovana su dva neutrona. Ukratko nakon toga, nastao je neptunijum kao međuproizvod, koji se odmah raspao na 238Pu. Nedvosmisleni dokaz o dobijanju elementa 94 dao je Arhur Val 23/24. februara 1941. godine.[4][5]
Drugi izotop plutonijuma dobijen je bombardovanjem brzim neutronima:
- Navedena vremena su vremena poluraspada.
Novootkrivenom elementu je dato ime u martu 1942. godine po u to vreme najudaljenijoj otkrivenoj planeti Plutonu, a koja je opet dobila ime po istoimenom božanstvu iz rimske mitologije: ...nazvan po planeti koja sledi nakon Neptuna, a u aspektu užasavajućeg delovanja plutonijumske atomske bombe daleko više mu odgovara izvođenje iz imena Plutona, božanstva podzemlja.[6] Prema tome, tri dotad najteža poznata elementa, uranijum, neptunijum i plutonijum dobili su imena prema istoimenim planetama: Uranu, Neptunu i Plutonu. Prva merljiva količina plutonijuma od oko 4 µg dobijena je u avgustu/septembru 1942. kada ju je izolovala grupa naučnika Baris Kaningam, Majkl Kefola i Luis Verner.[7] Otkriće je držano u tajnosti tokom Drugog svetskog rata. Sa prvom proizvodnjom plutonijuma u većem obimu otpočelo se u okvirima američkog projekta „Menhetn”. Prva eksplozija atomske bombe kojoj je svedočilo čovečanstvo bio je test „Triniti”, čija je osnova bio plutonijum 239Pu, kao i za bombu Debeljko ((jezik: engleski)) koja je u avgustu 1945. razorila japanski grad Nagasaki. Džozef Hamilton je izvodio testove na dobrovoljcima, dajući im plutonijum, a zbog ogromne otrovnosti ovog elementa danas su takvi testovi zabranjeni.
Čak i pre otkrića plutonijuma, u Nemačkoj je Karl Fridrih fon Vajceker nagovijestio da je u nuklearnim reaktorima moguć nastanak novog elementa eka-renijuma (tj. 239Eka Re).[8] Osim njega, Fridrih Georg Houtermans je takođe 1942. predvideo teoretsko postojanje nekog transuranijumskog elementa u svom tajnom izvještaju. Međutim u okvirima nacističkog uranijumskog projekta, prema današnjim saznanjima, do kraja Drugog svetskog rata nije došlo do sinteze plutonijuma.[9]
Osobine
urediFizičke
urediPri normalnim uslovima temperature i pritiska, plutonijum je srebrnasto-sjajni teški metal, veoma velike gustine (19,86 g/cm3[10]). Kao i svi aktinoidi, on takođe postoji samo u vidu radioaktivnih izotopa. On se zagrejava sam od sebe, tako da na primer 100 grama plutonijuma emituje oko 0,2 vata toplote (odnosi se na izotop 239Pu).[11] U poređenju s drugim metalima, plutonijum je vrlo slab provodnik toplote i električne struje. Metal se kristalizuje nezavisno od temperature u ukupno šest alotropskih modifikacija. One se jednim delom znatno razlikuju po svojoj gustini. Na sobnoj temperaturi stabilna modifikacija α-Pu je monoklinska. Kod plutonijuma pri višim temperaturama javlja se vrlo redak slučaj anomalije gustine, jer ona raste pri prelasku iz δ' modifikacije u ε modifikaciju. Pri njegovom topljenju, slično kao kod vode, gustina mu raste.[12] Istopljeni plutonijum ima najvišu viskoznost od svih elemenata u tečnom stanju.[13] Međutim, i pored neuobičajeno visoke magnetne susceptibilnosti za metale i tendencije usmeravanja pri niskim temperaturama, plutonijum ne pokazuje usmeravanje u širokim rasponima temperature pa se stoga može smatrati da je paramagnetičan.[12] Ipak, tačna merenja ometa stalno odavanje toplote uzrokovano radioaktivnim raspadom plutonijuma 239Pu. Iz istog razloga nemoguće je postići temperature plutonijuma bliske apsolutnoj nuli.
Modifikacija pri atmosferskom pritisku Opis
fazeStabilan u
temperaturnom područjuGustina (temperatura) Kristalni sistem Braveova rešetka Prostorna grupa α-Pu[14] 0 K – 395 K 19,77 g/cm³ (293 K) monoklinski primitivna P21/m (br. 11) β-Pu[15] 395 K – 479 K 17,7 g/cm³ (395 K) monoklinski centrirana po bazi I2/m (br. 12 poz. 3) γ-Pu[16] 479 K – 592 K 17,14 g/cm³ (479 K) ortoromgični plošno centrirana Fddd (br. 70) δ-Pu[17] 592 K – 730 K 15,9 g/cm³ (592 K) monoklinski centrirana po bazi Cm (br. 8) δ'-Pu[18] 730 K – 749 K 16,0 g/cm³ (730 K) tetragonalni prostorno centrirana I4/mmm (br. 139) ε-Pu[19] 749 K – 914 K 16,5 g/cm³ (749 K) kubnni prostorno centrirana Im m tečni[20] 914 K – 3503 K 16,63 g/cm³ (914 K) — — —
Osim navedenih, poznate su i modifikacije pri visokom pritisku, koje se dobiju iz α-Pu pri pritisku iznad 40 GPa, a kristaliziraju se u prostornoj grupi P63.[21]
Hemijske
urediPlutonijum je neplemeniti, veoma reaktivni metal. Izložen vazduhu, brzo reaguje s kiseonikom i vlagom. Pri tome metal postaje mat i prevlači se tamnim, plavo-crnim slojem oksida, dok dužim stajanjem na vazduhu stvara se tamniji, sivo-zeleni, praškasti sloj oksida koji lako skida.[22] Pri zagrejavanju, metal reaguje sa većinom nemetala i vodom. Međutim na sobnoj temperaturi, plutonijum ne napadaju ni bazini rastvori, niti voda. U koncentriranoj azotnoj kiselini on nije rastvorljiv zbog pasivizacije svoje površine.[11] Plutonijum se rastvara u hlorovodoničnoj i azotnoj kiselini ali uz dodatak fluorida. U tom slučaju, joni fluorida se poništavaju i onemogućavaju pasiviziranje metala koje se inače javlja napadanjem čiste azotne kiseline. Hemijske osobine plutonijuma uglavnom su slične kao i kod ostalih aktinoida. Kao i kod većine ovih elemenata, njegove hemijske osobine su pod znatnim uticajem njegove snažne radioaktivnosti, a zbog zagrejavanja metala i emitovanja jakog radioaktivnog zračenja, njegove veze sa drugim elementima vrlo lako pucaju.
Ovaj element može da gradi celi niz jedinjenja u kojima se može nalaziti u oksidacionim stanjima od +3 do +7, što znači da plutonijum zajedno s neptunijem gradi najviša oksidaciona stanja među svim aktinoidima. Najstabilniji je u oksidacionom stanju +4. U vodenim rastvorima, joni plutonijuma imaju karakteristične boje. Tako na primer jon Pu3+ je ljubičast, jon Pu4+ smeđ, PuVO2+ roze boje, PuVIO22+ narandžast, a PuVIIO23+ zelen.[23]
Izotopi
urediDo danas je izmereno i ispitano 20 izotopa i 15 nuklearnih izomera plutonijuma, čiji maseni brojevi se kreću od 228 do 247.[24] Vremena poluraspada se kreću od 37 · 10−12 sekundi za izomer 236m1Pu do oko 80 miliona godina za izotop 244Pu. „Najdugovječniji” izotopi sa vremenima poluraspada dužim od 11 dana imaju masene brojeve između 236 i 244. Jedini izuzetak među njima je 243Pu čije vreme poluraspada iznosi kraće od 5 sati.[24] Neki od izotopa se smatraju početnim tačkama za određene radioaktivne lance raspada.
- Izotop 236Pu se raspada preko torijumovog niza. On ima vreme poluraspada od 2,858 godine,[24] a raspada se α-raspadom na svoj „međuproizvod”, izotop 232U, koji se dalje sa vremenom poluraspada od 68,9 godina opet raspada na 228Th, što predstavlja glavni niz raspada. Ovaj izotop se dobija u veoma malim količinama u nuklearnim reaktorima koji rade na bazi uranijuma.
- Izotop 237Pu putem zahvata elektrona tokom vremena poluraspada od 45,2 dana[24] pretvara se u izotop neptunijuma 237Np sa verovatnoćom od 99,9958%, što predstavlja glavnu polaznu tačku neptunijumovog niza. Ostalih 0,0042% atoma ovog izotopa raspada se α-raspadom do uranijuma 233U, koji se takođe raspada neptunijumovim nizom.
- 238Pu je izotop koji se raspada α-raspadom sa vremenom poluraspada od 87,7 godina.[24] Najpre prelazi u uranijum 234U te se dalje raspada nizom raspada uranijum-radijumovim nizom.
- 239Pu je najčešće proizvedeni izotop plutonijuma. Ima vreme poluraspada od 24.110 godina[24] i pretežno se raspada emitujući α-zrake do uranijuma 235U. Dalji raspad odvija se putem uranijum-aktinijumovog niza, za prirodnu radioaktivnost, počev od izotopa 235U. Samo 3 · 10−10 % atoma ovog izotopa raspada se spontanim raspadom.
- Izotop 240Pu s vremenom poluraspada od 6.564 godine[24] raspada do 236U emitujući α-zračenje. Taj izotop uranijuma se raspada s vremenom poluraspada od 23,4 miliona godina do prirodnog izotopa torijuma 232Th. Dalji raspad odvija se duž torijumovog niza.
- Izotop 241Pu se često označava kao početak neptunijumovog niza, jer (pri produženju niza) se nalazi pre neptunijuma. On se raspada sa vremenom poluraspada od 14,35 godina[24] i verovatnoćom od 99,9975% putem β-raspada na izotop americijuma 241Am, dok se s verovatnoćom od samo 0,0025% raspada α-raspadom na uranijum 237U. Dalje se americijum 241Am α-raspadom i uranijum237U raspadaju do istog dugoživećeg izotopa neptunijuma 237Np.
- Plutonijum 242Pu se raspada istim lancem raspada kao i izotop 238Pu. Međutim, dok 238Pu dolazi u niz raspada kao sporedni lanac na 234U, izotop 242Pu stoji još više pre uranijuma 238U. Plutonijum 242Pu se raspada α-raspadom na 238U, predstavljajući početak prirodnog uranijum-radijumovog niza. Sa vremenom poluraspada od 375 hiljada godina,[24] 242Pu je najdugovečniji izotop plutonijuma nakon 244Pu.
- 243Pu ima relativno kraće vreme poluraspada od 4,956 sati.[24] Ovaj izotop najpre β-zračenjem prelazi u americijum 243Am, koji dalje prelazi u neptunijum 239Np a ovaj dalje se raspada na plutonijum 239Pu. Na taj način ovaj izotop predstavlja produžetak uranijum-aktinijumovog niza.
- Izotop plutonijuma 244Pu smatra se jedinim izotopom plutonijuma koji se, uslovno, može pronaći u prirodi.[25] Njegovo vreme poluraspada je veoma dugo i iznosi oko 80 miliona godina.[24] On je početna tačka torijumovog niza, a koji se zbog toga ponegde zove i plutonijum-torijumov niz. Izotop 244Pu se raspada α-raspadom na 240U, ovaj dvostrukim β-raspadom preko neptunijuma 240Np do 240Pu, a ovaj opet se putem daljnjeg dvostrukog α-raspada preko 236U do torijuma 232Th. Nakon izotopa torijuma sledi raspad duž torijumovog niza.
Reference
uredi- ^ Meija, J.; et al. (2016). „Atomic weights of the elements 2013 (IUPAC Technical Report)”. Pure and Applied Chemistry. 88 (3): 265—291. doi:10.1515/pac-2015-0305.
- ^ Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. izd.). Prentice Hall. ISBN 978-0-13-175553-6.
- ^ Parkes, G.D. & Phil, D. (1973). Melorova moderna neorganska hemija. Beograd: Naučna knjiga.
- ^ G. T. Seaborg; E. McMillan; J. W. Kennedy; A. C. Wahl (1946). „Radioactive Element 94 from Deuterons on Uranium”. Physical Review. 69 (7–8): 366–367. doi:10.1103/PhysRev.69.367.
- ^ J. W. Kennedy; G. T. Seaborg; E. Segrè; A. C. Wahl (1946). „Properties of Element 94”. Physical Review. 70 (7–8): 555—556. doi:10.1103/PhysRev.70.555.
- ^ Holleman 2007, str. 1948.
- ^ B. B. Cunningham; L. B. Werner (1949). „The First Isolation Of Plutonium”. Journal of the American Chemical Society. 71 (5): 1521—1528. doi:10.1021/ja01173a001.
- ^ „Carl Friedrich von Weizsäcker: Eine Möglichkeit der Energiegewinnung aus Uran 238, 17. Juli 1940”. Geheimdokumente zum deutschen Atomprogramm 1938–1945. Deutsches Museum. Pristupljeno 13. 12. 2016.
- ^ Markus Becker (19. 3. 2009). „Nuklear-Forensik: "Heisenberg-Würfel" verrät Details über Hitlers Atomprogramm”. Spiegel Online. Pristupljeno 13. 12. 2016.
- ^ Holleman 2007, str. 2149.
- ^ a b Norman N. Greenwood; Alan Earnshaw (1988). Chemie der Elemente (1 izd.). Weinheim: VCH Verlagsgesellschaft. ISBN 3-527-26169-9.
- ^ a b „Plutonium: An Element at odds with itself” (pdf). Los Alamos Science. 2000. Pristupljeno 19. 10. 2017.
- ^ „Plutonium – Element mit vielen Facetten”. kernchemie.de (na jeziku: nemački). Pristupljeno 19. 10. 2017.
- ^ W. H. Zachariasen; F. H. Ellinger (1963). „The Crystal Structure of alpha Plutonium Metal”. Acta Cryst. 16: 777—783. doi:10.1107/S0365110X63002012.
- ^ W. H. Zachariasen; F. H. Ellinger (1963). „The Crystal Structure of beta Plutonium Metal”. Acta Cryst. 16: 369—375. doi:10.1107/S0365110X63000992.
- ^ W. H. Zachariasen (1955). „Crystal Chemical Studies of the 5f-Series of Elements. XXIV. The Crystal Structure and Thermal Expansion of γ-Plutonium”. Acta Cryst. 8: 431—433. doi:10.1107/S0365110X55001357.
- ^ K. T. Moore; P. Söderlind; A. J. Schwartz; D. E. Laughlin (2006). „Symmetry and Stability of δ Plutonium: The Influence of Electronic Structure”. Physical Review Letters. 96 (20): 206402/1—206402/4. doi:10.1103/PhysRevLett.96.206402.
- ^ F. H. Ellinger: Crystal structure of delta' plutonium and the thermal expansion characteristics of delta, delta' and epsilon plutonium, u: Journal of Metals. 8, 1956, str. 1256–1259.
- ^ J. B. Ball, J. A. Lee, P. G. Mardon, J. A. L. Robertson: Determination de quelques proprietes physiques du plutonium metal. u: Memoires Scientifiques de la Revue de Metallurgie. 57, 1960, str. 49–56.
- ^ David R. Lide, ur. (2009). „Magnetic Susceptibility of the Elements and Inorganic Compounds”. CRC Handbook of Chemistry and Physics (90 izd.). Boca Raton, FL: CRC Press/Taylor and Francis. str. 4—145. ISBN 9781420090840.
- ^ S. Dabos-Seignon; J. P. Dancausse; R. Gering; S. Heathman; U. Benedict (1993). „Pressure induced phase transition in α-Pu”. Journal of Alloys and Compounds. 190: 237—242. doi:10.1016/0925-8388(93)90404-B.
- ^ Georg Brauer (1978). Handbuch der Präparativen Anorganischen Chemie. 2 (3 izd.). Stuttgart: Enke. str. 1293. ISBN 3-432-87813-3.
- ^ Holleman 2007, str. 1956.
- ^ a b v g d đ e ž z i j G. Audi; O. Bersillon; J. Blachot; A. H. Wapstra (2003). „The NUBASE evaluation of nuclear and decay properties” (PDF). 729. Nuclear Physics A.: 105—110. doi:10.1016/S0375-9474(97)00482-X. Arhivirano iz originala (pdf) 20. 7. 2011. g. Pristupljeno 11. 2. 2017.
- ^ D. C. Hoffman; F. O. Lawrence; J. L. Mewherter; F. M. Rourke (1971). „Detection of Plutonium-244 in Nature”. Nature. 234: 132—134. doi:10.1038/234132a0.
Literatura
uredi- Asimov, Isaac (1988). „Nuclear Reactors”. Understanding Physics. New York: Barnes & Noble Publishing. ISBN 0-88029-251-2.
- Bernstein, Jeremy (2007). Plutonium: a History of the World's most Dangerous Element. Washington, D.C.: Joseph Henry Press. ISBN 978-0-309-10296-4. OCLC 76481517.
- Clark, Ronald (1961). The Birth of the Bomb: The Untold Story of Britain's Part in the Weapon That Changed the World. London: Phoenix House. OCLC 824335.
- Eagleson, Mary (1994). Concise Encyclopedia Chemistry. Berlin: Walter de Gruyter. ISBN 978-3-11-011451-5.
- Emsley, John (2001). „Plutonium”. Nature's Building Blocks: An A–Z Guide to the Elements. Oxford (UK): Oxford University Press. ISBN 0-19-850340-7.
- Gosling, F. G. (1999). The Manhattan Project: Making the Atomic Bomb (PDF). Oak Ridge: United States Department of Energy. ISBN 0-7881-7880-6. DOE/MA-0001-01/99. Arhivirano iz originala (PDF) 24. 2. 2009. g. Pristupljeno 15. 2. 2009.
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd izd.). Oxford (UK): Butterworth-Heinemann. ISBN 0-7506-3365-4.
- Heiserman, David L. (1992). „Element 94: Plutonium”. Exploring Chemical Elements and their Compounds. New York (NY): TAB Books. str. 337–340. ISBN 0-8306-3018-X.
- Hoddeson, Lillian; Henriksen, Paul W.; Meade, Roger A.; Westfall, Catherine L. (1993). Critical Assembly: A Technical History of Los Alamos During the Oppenheimer Years, 1943–1945. New York: Cambridge University Press. ISBN 0-521-44132-3. OCLC 26764320.
- Hunner, Jon (2004). Inventing Los Alamos. ISBN 978-0-8061-3891-6.
- Hurst, D. G.; Ward, A. G. (1956). Canadian Research Reactors (PDF). Ottawa: Atomic Energy of Canada Limited. OCLC 719819357. Pristupljeno 6. 2. 2015.
- Jha, D. K. (2004). Nuclear Energy. Discovery Publishing House. ISBN 81-7141-884-8.
- Kaku, Michio; Trainer, Jennifer (1983). Nuclear Power, Both Sides: The Best Arguments for and Against the Most Controversial Technology. W. W. Norton & Company. ISBN 9780393301281. Pristupljeno 8. 12. 2013.
- Kay, A. E. (1965). plutonium 1965. Taylor & Francis.
- Lide, David R., ur. (2006). Handbook of Chemistry and Physics (87th izd.). Boca Raton: CRC Press, Taylor & Francis Group. ISBN 0-8493-0487-3.
- Magurno, B. A.; Pearlstein, S., ur. (1981). Proceedings of the conference on nuclear data evaluation methods and procedures. BNL-NCS 51363. (PDF). II. Upton: Brookhaven National Laboratory. Pristupljeno 6. 8. 2014.
- Martin, James E. (2000). Physics for Radiation Protection. Wiley-Interscience. ISBN 0-471-35373-6.
- McLaughlin, Thomas P.; Monahan, Shean P.; Pruvost, Norman L. (2000). A Review of Criticality Accidents (PDF). Los Alamos: Los Alamos National Laboratory. LA-13638. Pristupljeno 6. 2. 2015.
- Miner, William N.; Schonfeld, Fred W. (1968). „Plutonium”. Ur.: Clifford A. Hampel. The Encyclopedia of the Chemical Elements. New York (NY): Reinhold Book Corporation. str. 540–546. LCCN 68029938.
- Moody, Kenton James; Hutcheon, Ian D.; Grant, Patrick M. (2005). Nuclear forensic analysis. CRC Press. ISBN 0-8493-1513-1.
- Rhodes, Richard (1986). The Making of the Atomic Bomb. New York: Simon & Schuster. ISBN 0-671-65719-4.
- Seaborg, G. T.; Seaborg, E. (2001). Adventures in the Atomic Age: From Watts to Washington. Farrar, Straus and Giroux. ISBN 0-374-29991-9.
- Sklar, Morty (1984). Nuke-Rebuke: Writers & Artists Against Nuclear Energy & Weapons. The Contemporary anthology series. The Spirit That Moves Us Press.
- Stockholm International Peace Research Institute (2007). SIPRI Yearbook 2007: Armaments, Disarmament, and International Security. Oxford University Press. ISBN 978-0-19-923021-1.
- Till, C. E.; Chang, Y. I. (2011). Plentiful Energy: The Story of the Integral Fast Reactor, the Complex History of a Simple Reactor Technology, with Emphasis on Its Scientific Basis for Non-specialists. Charles E. Till and Yoon Il Chang. ISBN 978-1-4663-8460-6.
- Wahlen, R. K. (1989). History of 100-B Area (PDF). Richland, Washington: Westinghouse Hanford Company. WHC-EP-0273. Arhivirano iz originala (PDF) 27. 3. 2009. g. Pristupljeno 15. 2. 2009.
- Welsome, Eileen (2000). The Plutonium Files: America's Secret Medical Experiments in the Cold War. New York: Random House. ISBN 0-385-31954-1.
Spoljašnje veze
uredi- „Alsos Digital Library for Nuclear Issues - Plutonium”. Washington and Lee University. Arhivirano iz originala 3. 2. 2009. g. Pristupljeno 15. 2. 2009.
- Sutcliffe, W. G.; et al. (1995). „A Perspective on the Dangers of Plutonium”. Lawrence Livermore National Laboratory. Arhivirano iz originala 29. 9. 2006. g.
- Johnson, C. M.; Davis, Z.S. (1997). „Nuclear Weapons: Disposal Options for Surplus Weapons-Usable Plutonium”. CRS Report for Congress # 97-564 ENR. Pristupljeno 15. 2. 2009.
- „Physical, Nuclear, and Chemical, Properties of Plutonium”. IEER. 2005. Pristupljeno 15. 2. 2009.
- Bhadeshia, H. „Plutonium crystallography”.
- Samuels, D. (2005). „End of the Plutonium Age”. Discover Magazine. 26 (11).
- Pike, J.; Sherman, R. (2000). „Plutonium production”. Federation of American Scientists. Arhivirano iz originala 3. 2. 2009. g. Pristupljeno 15. 2. 2009.
- „Plutonium Manufacture and Fabrication”.
- Ong, C. (1999). „World Plutonium Inventories”. Nuclear Files.org. Arhivirano iz originala 5. 8. 2014. g. Pristupljeno 15. 2. 2009.
- „Challenges in Plutonium Science”. Los Alamos Science. I & II (26). 2000. Pristupljeno 15. 2. 2009.
- „Plutonium”. Royal Society of Chemistry. Pristupljeno 6. 2. 2015.
- „Plutonium”. The Periodic Table of Videos. University of Nottingham. Pristupljeno 6. 2. 2015.